서 언
재료 및 방법
논문선정
화합물 선정
결 과
Phytochemical
Flavonoids
Steroids and Terpenoids
Organic Acids
함질소화합물과 기타 화합물
항염증 성분
고 찰
적 요
서 언
염증은 라틴어 “inflammare”(불타다, 炎)로부터 유래한 용어이다. 용어에서 직관적으로 알 수 있듯이 염증은 발열을 특징으로 하는 생체가 병원체, 외상, 독소 등 외부의 해로운 자극이나 조직 손상에 반응하여 발생하는 복잡한 생물학적 반응이다. 이 반응은 면역세포, 혈관계, 염증매개물질 등이 동원되어 조직의 항상성을 회복하려는 생리적 방어 기전이며, 일반적으로 발열, 발적, 부종, 통증 및 기능상실을 특징으로 한다(Abdulkhaleq et al., 2018; Medzhitov, 2008; Pan et al., 2011). 그러나 이러한 급성 염증 반응이 조절되지 않거나 만성화될 경우, 관절염, 염증성 장질환, 심혈관 질환, 신경퇴행성 질환 등 다양한 만성 염증성 질환의 병태생리에 중심적 역할을 하게 된다(Deng et al., 2022). 현재 염증을 치료하기 위해서 스테로이드 및 비스테로이드성 소염제(NSAIDs)를 사용하는 것이 효과적이지만 장기간 사용 시 위장관 손상, 간과 신장 기능 저하 등 부작용과 장기 복용의 한계로 인해, 부작용이 적고 다양한 생리활성을 지닌 천연물(natural products)에 대한 관심이 증가하고 있다. 특히 플라보노이드, 테르페노이드, 알칼로이드, 다당류 등 천연 유래 화합물들은 NF-κB, MAPK, NLRP3 inflammasome 등 염증 관련 경로를 조절함으로써 면역조절 및 항염증 활성을 나타내는 것으로 보고되고 있다(Deng et al., 2022; Goh et al., 2022; Hou et al., 2020; Venkatesha and Moudgil, 2023).
한의학의 본초학에서는 해표약(解表藥)은 외부의 사기(邪氣)를 인체가 감수하여 나타나는 현대의 급성염증으로 볼 수 있는 표증(表證)을 없애는 약이다. 또한 현대의 만성염증인 체내의 열(熱), 화(火)를 제거하여 내부의 열독을 다스리는 약을 청열약(淸熱藥)이라고 한다. 이와 같이 한국에서는 본초약물을 염증을 치료하는데 오랜 기간 사용해 왔던 역사를 가지고 있다. 이런 전통적으로 사용 역사가 긴 본초 약물 중에서 작두콩(Canavalia gladiata)의 씨는 명나라 이시진이 쓴 책인 본초강목과 현대 중국 약전에도 수재된 도두(刀豆)이다(Qian et al., 2025). 작두콩은 열대지방 원산으로 콩과에 속하는 일년생 덩굴성 식물이다. 그 콩깍지 모양이 작두를 닮아서 작두콩 또는 넓고 평평한 칼과 비슷하다고 도두(刀豆)라고 불린다(Joo et al., 2001). 본초강목(本草綱目)에 따르면 도두는 중초(中焦)를 따뜻하게 하고 기를 내리며, 배변을 촉진하고 트림을 멎게 하며, 신장을 보하고 원기를 보한다고 한다. 일본에서는 작두콩의 과일을 염증성 질환, 치주염, 중이염, 종기, 치질, 아토피 피부염 치료에 사용하며, 미성숙 과일을 절인 음식으로 만들어서 식용한다. 한국에서는 무좀이나 여드름 치료용 비누로 사용하거나 잎을 비염, 부비동염 등에 사용한다(Qian et al., 2025).
작두콩(C. gladiata)에 함유된 생리 활성 성분에는 플라보노이드, 테르펜, 유기산 유도체 등이 보고되어 있다. 이러한 화학물질들은 항산화, 항균, 항염증, 항혈관신생 등의 다양한 약리 특성을 나타낸다. 최근에 작두콩의 의학적이용과 화합물들에 대한 리뷰 논문이 발표되었지만 소개된 함유 화합물들 중 다수가 HPLC 분석 후 표준품과 머무름시간 비교, LC-MS, GC- MS 분석 후 표준품과 머무름시간과 MS 패턴비교를 통한 함유되었을 것으로 추정되는 화합물을 후보로 제시하는 정도의 정보제공으로 실제 작두콩에 함유된 성분과 차이가 있고, 활성에 대한 내용도 추출물에 의한 활성을 다루었다(Qian et al., 2025). 따라서 이 리뷰에서는 작두콩의 식품, 의약품으로서 심층적 활용을 위해서 실제 작두콩의 추출, 성분분리 및 정제, NMR 등을 중심으로 하는 분광학적인 구조 결정방법으로 함유 성분을 동정하고, 그 동정한 화합물들의 항염증 작용에 대한 자료를 제공하고자 한다.
재료 및 방법
논문선정
본 논문에서 다룬 문헌은 PubMed, Scopus, Web of Science, Google Scholar 등의 데이터베이스를 활용하여 2025년 5월까지 발행된 문헌을 대상으로 검색하였다. 주요 검색어는 “Canavalia gladiata”, “inflammation”, “anti-inflammatory”, “natural products”, “cytokines”, “herbal medicine” 등을 조합하여 사용하였다. 논문 선정 기준은 영문, 국문, 중문, 일문으로 작성된 논문, 염증 반응과 천연물 또는 생리활성 성분 간의 연관성을 다룬 연구로 하였다.
화합물 선정
작두콩을 추출하여 컬럼크로마토그래프법으로 분리, 정제 후 NMR 분석을 중심으로 한 분광학적 분석방법으로 화합물의 구조를 결정하고 동정한 화합물만을 선정하였다. 표준품과 추출물을 HPLC 분석하여 머무름 시간을 비교하거나 LC-MS, GC-MS로 추출물을 분석하여 머무름 시간과 MS 패턴의 유사성을 비교하여 추정한 화합물을 제외하였다.
결 과
Phytochemical
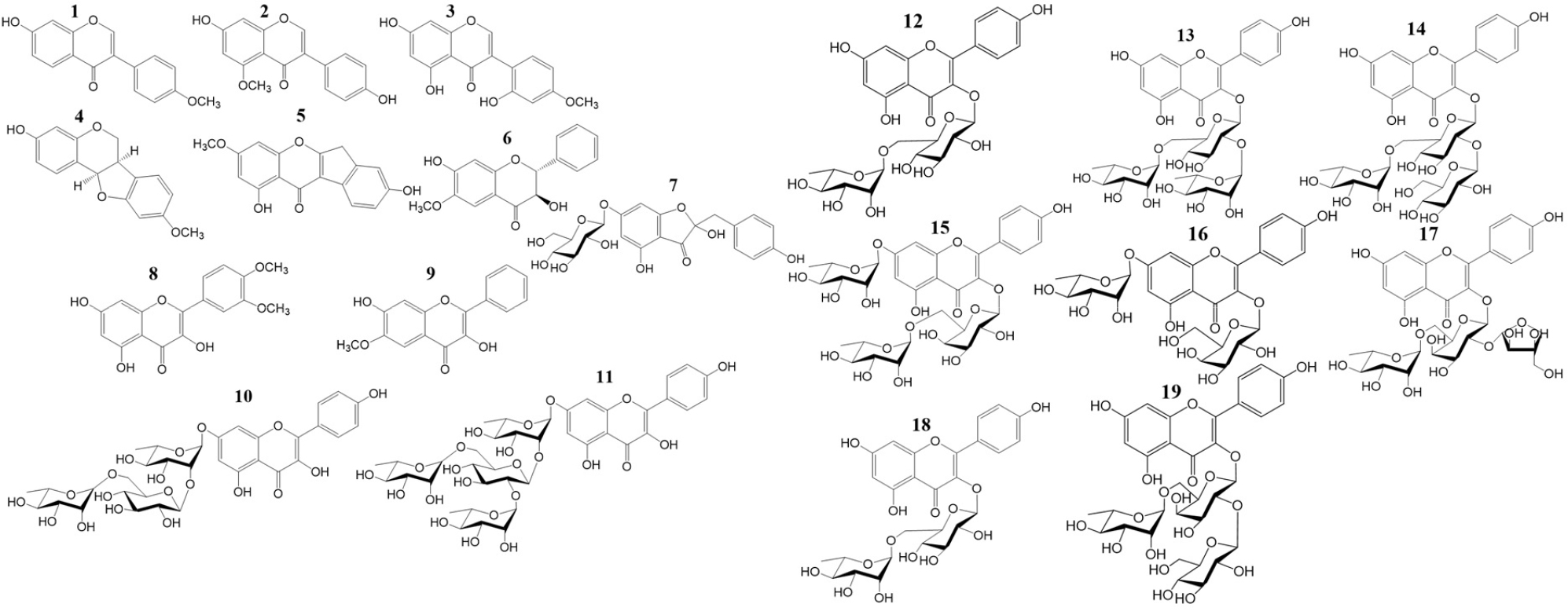
현재까지 연구 결과에 따르면 작두콩의 종자, 열매, 뿌리에서 flavonoids, terpenoids, steroid, orgaic acid, amine 등의 화합물이 분리, 정제, 구조 결정되었다. 각 화합물의 이름과 화학구조명은 Table 1에 표시하였다.
Table 1.
Phytochemical constituents and their structures in Canavalia gladiata.
| No. | Compound name | Compound class | Reference |
| 1 | formononetin | isoflavone | Vinh et al., 2024 |
| 2 | 5-methoxydaidzein | isoflavone | Vinh et al., 2024 |
| 3 | 2'-hydroxy biochanin A | isoflavone | Vinh et al., 2024 |
| 4 | medicarpin | isoflavone | Vinh et al., 2024 |
| 5 | sophorophenolone | isoflavone | Vinh et al., 2024 |
| 6 | 7-hydroxy-6-methoxydihydroflavonol | flavonol | Vinh et al., 2024 |
| 7 | maesopsin-6-O-ß-D-glucopyranoside | chalcone | Lü et al., 2024 |
| 8 | dillenetin | flavanonol | An et al., 2020 |
| 9 | gladiatin | flavanonol | Dinda et al., 2014 |
| 10 | kaempferol-7-O-[2-O-ß-D-glucopyranosyl-6-O-α-L-rhamnopyranosyl]-α-L-rhamnopyranoside | flavanonol | An et al., 2020 |
| 11 | kaempferol-7-O-α-L-dirhamnopyranosyl(1→2;1→6)-O-ß-D-glucopyranosyl(1→2)-O-α-L-rhamnopyranoside | flavanonol | An et al., 2020 |
| 12 | kaempferol-3-O-rutinoside | flavanonol | An et al., 2020 |
| 13 | kaempferol-3-O-(2,6-O-α-L-dirhamnopyranosyl)-ß-D-glucopyranoside | flavanonol | An et al., 2020 |
| 14 | kaempferol-3-O-[2-O-ß-D-glucopyranosyl-6-O-α-L-rhamnopyranosyl]-ß-D-glucopyranoside | flavanonol | An et al., 2020 |
| 15 | robinin | flavanonol | Murakami et al., 2000 |
| 16 | kaempferol-3-O-ß-D-galactopyranosyl-7-O-α-L-rhamnopyranoside | flavanonol | Murakami et al., 2000 |
| 17 | kaempferol 3-O-ß-D-apiofuranosyl-(1→2)-O-[α-L-rhamnopyranosyl-(1→6)]-ß-D-galactopyranoside | flavanonol | Lü et al., 2024 |
| 18 | biorobin | flavanonol | Lü et al., 2024 |
| 19 | kaempferol 3-O-ß-D-glucopyranosyl-(1→2)-O-[α-L-rhamnopyranosyl-(1→6)]-ß-D-galactopyranoside | flavanonol | Lü et al., 2024 |
| 20 | gladiatoside A1 | flavanonol | Murakami et al., 2000 |
| 21 | gladiatoside A2 | flavanonol | Murakami et al., 2000 |
| 22 | gladiatoside A3 | flavanonol | Murakami et al., 2000 |
| 23 | gladiatoside B1 | flavanonol | Murakami et al., 2000 |
| 24 | gladiatoside B2 | flavanonol | Murakami et al., 2000 |
| 25 | gladiatoside B3 | flavanonol | Murakami et al., 2000 |
| 26 | gladiatoside C1 | flavanonol | Murakami et al., 2000 |
| 27 | gladiatoside C2 | flavanonol | Murakami et al., 2000 |
| 28 | isoquercitrin | flavanonol | Lü et al., 2024 |
| 29 | quercetin 3-O-(6''-O-galloyl)-ß-D-glucoside | flavanonol | Lü et al., 2024 |
| 30 | rutin | flavanonol | Vinh et al., 2024 |
| 31 | isomyricitrin | flavanonol | Lü et al., 2024 |
| 32 | myricetin 3-O-rutinoside | flavanonol | Vinh et al., 2024 |
| 33 | dihydrophaseic acid | sesquiterpene | An et al., 2020 |
| 34 | caryophyllenic acid | sesquiterpene | An et al., 2020 |
| 35 | canavalioside | diterpene | Murakami et al., 2000 |
| 36 | canavalia gibberellin I | diterpene | Murofushi et al., 1969; Tamura et al., 1967 |
| 37 | canavalia gibberellin II | diterpene | Murofushi et al., 1969; Tamura et al., 1967 |
| 38 | gibberellin A59 | diterpene | Yokota and Takahashi, 1981 |
| 39 | ß-sitosterol | steroid | Vinh et al., 2024 |
| 40 | lupeol | triterpene | Li et al., 2007 |
| 41 | 3α-friedelinol | triterpene | Vinh et al., 2024 |
| 42 | kaikasaponin III | triterpene | Kinjo et al., 1997 |
| 43 | abrisaponin So1 | triterpene | Kinjo et al., 1997 |
| 44 | phaseoside IV | triterpene | Kinjo et al., 1997 |
| 45 | phaseoside V | triterpene | Kinjo et al., 1997 |
| 46 | gallic acid | organic acid | Li et al., 2007 |
| 47 | 4-O-methylgallic acid | organic acid | Jeon et al., 2005 |
| 48 | methyl gallate | organic acid | Li et al., 2007 |
| 49 | breynioside A | tannin | Lü et al., 2024 |
| 50 | 1,3,6-tri-O-galloyl ß-D-glucopyranoside | tannin | Lü et al., 2024 |
| 51 | 1,4,6-tri-O-galloyl ß-D-glucopyranoside | tannin | Kim et al., 2013 |
| 52 | 4-hydroxy-3-methoxyphenol-1-O-ß-D-(6'-O-galloyl) glucoside | tannin | Lü et al., 2024 |
| 53 | 1,6-di-O-galloyl ß-D-glucopyranoside | tannin | Li et al., 2007 |
| 54 | (2S,3S,4E,8E)-2-aminooctadeca-4,8-diene-1,3-diol 1-O-ß-D-glucopyranoside | amide | An et al., 2020 |
| 55 | (2S,3S,4E,8Z)-2-aminooctadeca-4,8-diene-1,3-diol 1-O-ß-D-glucopyranoside | amide | An et al., 2020 |
| 56 | N-(2-methoxy benzoyl) homoserine | amide | An et al., 2020 |
| 57 | ß-adenosine | nucleoside | Vinh et al., 2024 |
| 58 | trilinolein | triglyceride | An et al., 2020 |
| 59 | δ-tocopherol | phenolics | Li et al., 2007 |
| 60 | (3-ethenylphenyl)-1,2-ethanediol | phenylalcohol | Lü et al., 2024 |
Flavonoids
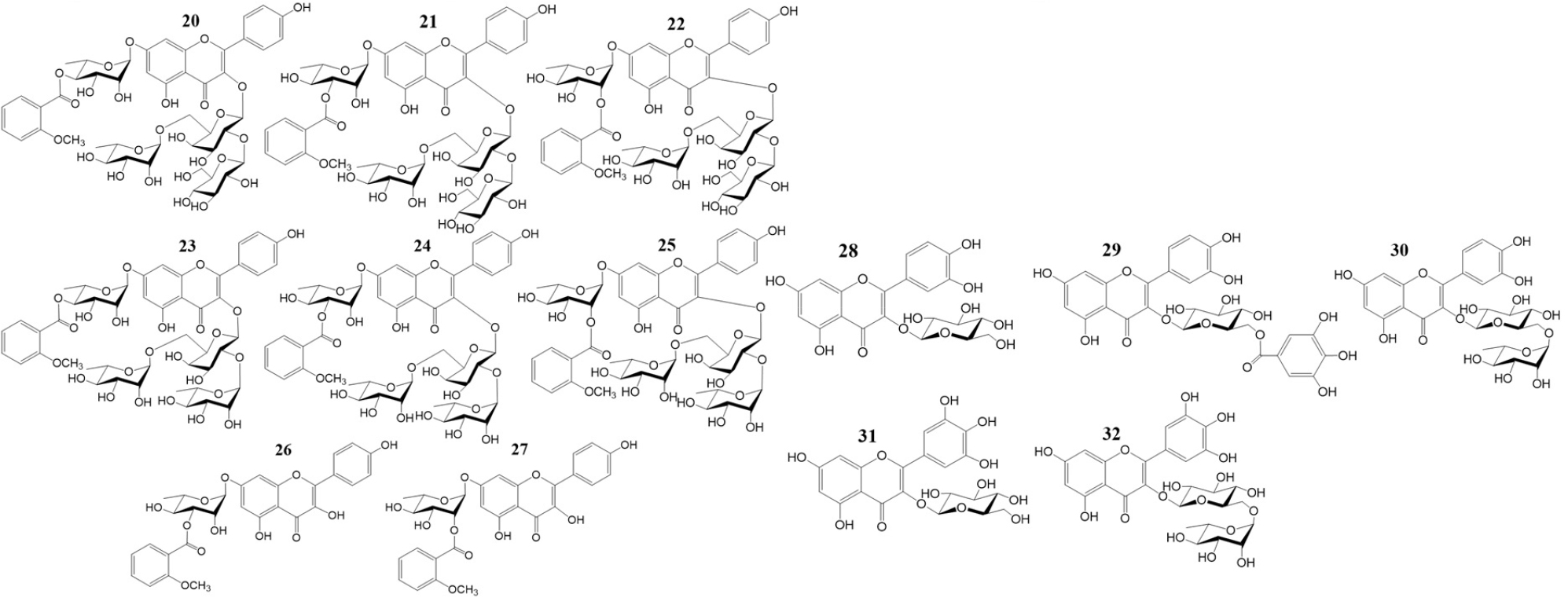
현재까지 작두콩에서 총 32종의 플라보노이드가 보고되었으며, 구조적으로는 flavonol, flavanonol, isoflavone, chalcone이다. Flavonol의 대부분은 배당체로 존재한다. 이들 중 세 개의 화합물은 quercetin을, 두 개의 화합물은 myricetin을, 스무 개의 화합물은 kaempferol을 모핵으로 가지고 있다. 당의 종류로는 glucopyranoside, rhamnopyranoside, galactopyranoside, apiofuranoside가 quercetin, myricetin, kaempferol의 C-3 또는 C-7 위치 그리고 C-3과 C-7 위치 양쪽 모두에 결합하고 있다. 최근에 C. gladiata의 각 부위에서 화학 구조적으로 특이한 flavonol들이 다수 보고되었다. 예를 들어, 작두콩 열매의 메탄올 추출물에서는 신규 화합물인 5-deoxyflavonol 구조를 가진 gladiatin (Dinda and Banik, 2014)이 분리되어 보고되었고, 작두콩 종자의 메탄올 추출물로부터 여덟 개의 새로운 아실화 플라보놀 배당체인 gladiatoside A1, A2, A3, B1, B2, B3, C1, C2가 함유되어 있음이 보고되었다(Murakami et al., 2000). 또한 종자의 메탄올 추출물에서는 신규 flavonol tetraglycoside인 kaempferol-7-O-α-L- dirhamnopyranosyl(1→2;1→6)-O-β-D-glucopyranosyl (1→2)-O-α-L-rhamnopyranoside가 보고되었다(An et al., 2020). Semi-preparative 액체크로마토그래피(HPLC), 컬럼 크로마토그래피를 사용하여 isoflavone인 formononetin과 flavonol 배당체인 myricetin 3-O-rutinoside가 열매 메탄올 추출물에서 최초로 분리되었다(Vinh et al., 2024). chalcone의 경우, 종자의 75% 에탄올 추출물에서 maesopsin-6-O-β-D-glucopyranoside가 최초로 보고되었다(Lü et al., 2024). flavonoid의 화학 구조는 Fig. 1과 Fig. 2에 표시하였다.
Steroids and Terpenoids
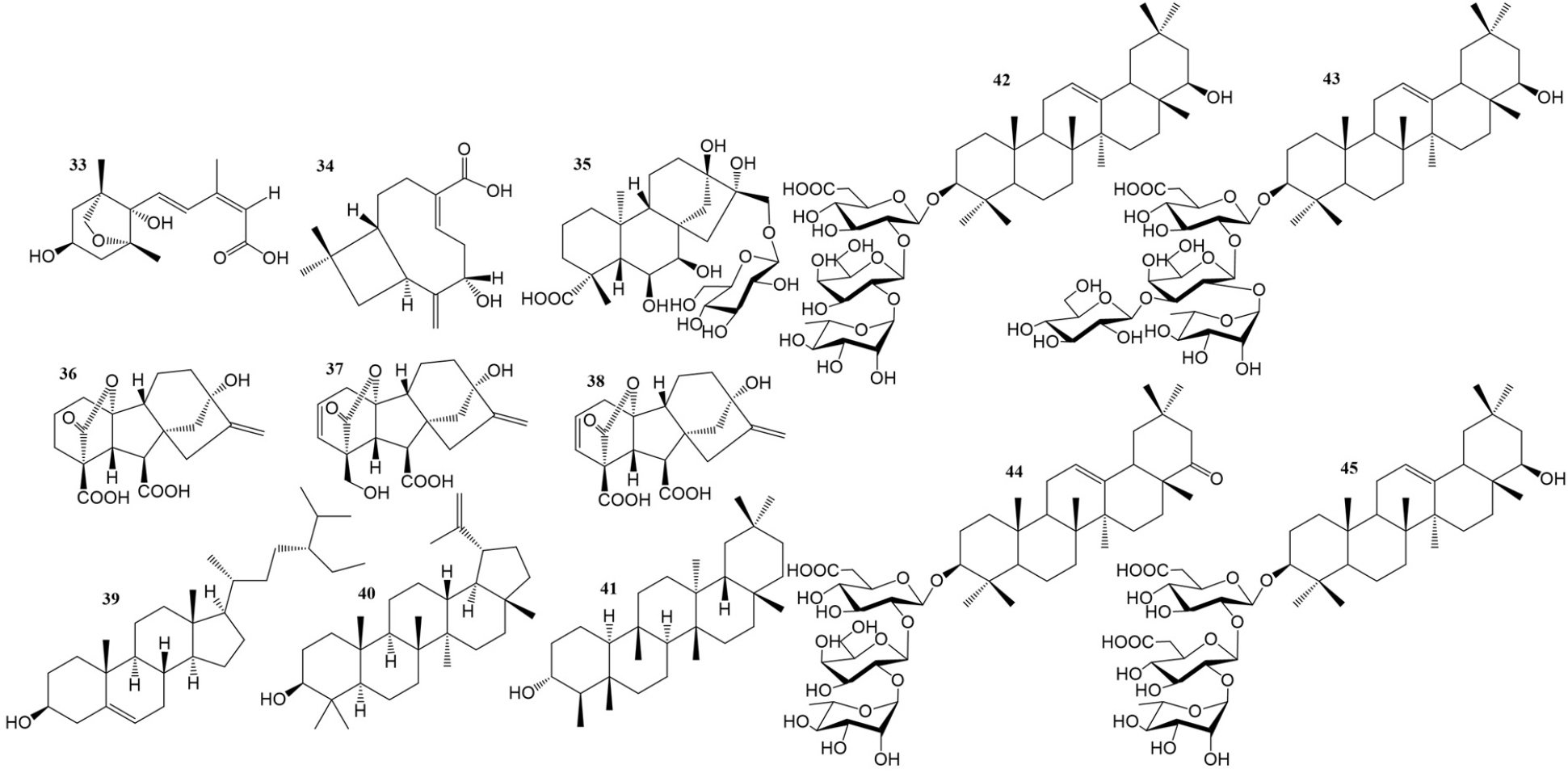
현재까지 작두콩에서 steroid 1종과 terpenoids 12종이 보고되었다. 이 화합물들은 구조적으로 sesquiterpene, diterpene, triterpene, steroid로 구분될 수 있다. 종자의 메탄올 추출물에서 발견된 신규 화합물인 (Z,1R,7S,9S)-7-hydroxy-11,11- dimethyl-8-methylenebicyclo[7.2.0]undec-4-ene-4-carboxylic acid는 caryophyllene 계열의 sesquiterpene이며, 기지 화합물인 dihydrophaseic acid는 apo-carotenoid 계열의 sesquiterpene이다(An et al., 2020). 또한, high- resolution mass, IR, NMR 스펙트럼을 이용하여 3종의 신규 gibbane 계열 diterpene인 canavalia gibberellin-I, canavalia gibberellin-II가 종자에서(Murofushi et al., 1969; Tamura et al., 1967), Gibberellin A59가 작두콩의 미숙 종자에서(Yokota and Takahashi, 1981) 보고되었다. 또한 종자 메탄올 추출물에서 신규 ent-kaurane 계열 diterpene 배당체인 canavalioside가 확인되었다(Murakami et al., 2000). 현재까지 보고된 모든 triterpene은 lupane (Li et al., 2007; Lü et al., 2024), friedelane (Vinh et al., 2024), oleanane 계열의 5환성 triterpene이다. 두 종의 신규 triterpene saponin인 phaseosides IV와 V, 기지 화합물인 abrisaponin Sol, kaikasaponin III도 뿌리에 함유되어 있음이 확인되었다(Kinjo et al., 1997). 또한 열매와 종자에서는 phytosteroid인 β-sitosterol이 함유되어 있음이 확인되었다(Li et al., 2007; Vinh et al., 2024). Steroid와 terpenoid의 화학 구조는 Fig. 3에 제시하였다.
Organic Acids
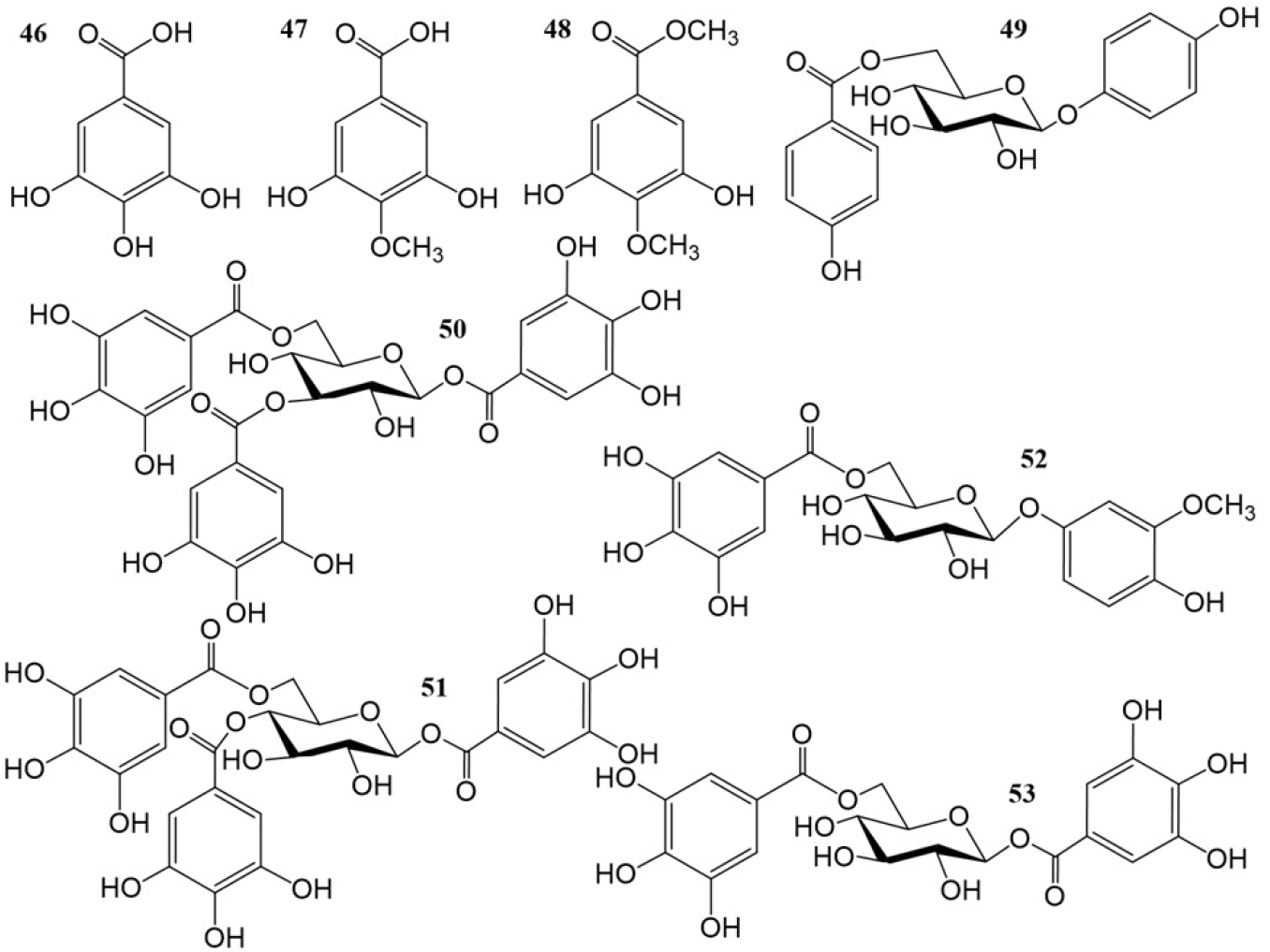
유기산은 작두콩 종자에 함유되어 있음이 보고되었으며 방향족산과 지방산 두 그룹으로 나눌 수 있다. 지방산은 주로 LC-MS 또는 GC-MS 분석 후 패턴 비교를 통해서 후보 화합물들이 제시되었다. 종자에 함유된 방향족산은 주로 gallic acid와 그 유도체이다(Jeon et al., 2005). 또한 종자의 메탄올 추출물에서 처음으로 함유된 것이 보고된 1,6-di-O-galloyl β- D-glucopyranoside, 1,4,6-tri-O-galloyl β-D-glucopyranoside, 1,3,6-tri-O-galloyl-β-D-glucopyranoside, 4- hydroxy-3-methoxyphenol-1-O-β-D-(6′-O-galloyl) glucoside, breynioside A는 가수분해형 탄닌으로 분류할 수 있다(Kim et al., 2013; Li et al., 2007; Lü et al., 2024). 그리고 gallic acid, methyl gallate도 종자의 메탄올 추출물에서 처음으로 확인되었다(Kim et al., 2013; Li et al., 2007). 유기산과 그 유도체들의 화학 구조는 Fig. 4에 표시하였다.
함질소화합물과 기타 화합물
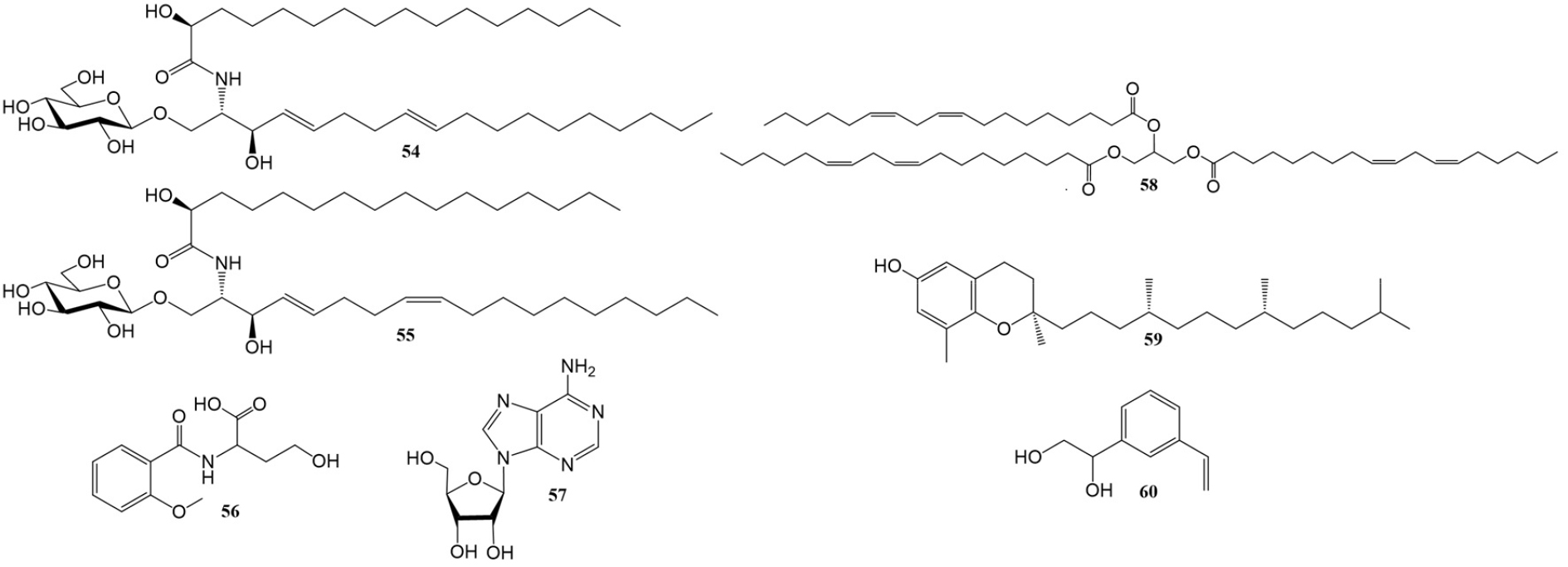
종자의 메탄올 추출물에서 amide인 (2S,3S,4E,8E)-2- aminooctadeca-4,8-diene-1,3-diol 1-O-β-D-glucopyranoside, (2S,3S,4E,8Z)-2-aminooctadeca-4,8-diene-1, 3-diol 1-O-β-D-glucopyranoside, N-(2-methoxy benzoyl) homoserine과(An et al., 2020; Vinh et al., 2024), 열매의 메탄올 추출물에서 purine nucleoside인 adenosine (Vinh et al., 2024), 종자의 메탄올 추출물에서 triglyceride인 trilinolein (An et al., 2020), 페놀유도체인 δ-tocopherol (Li et al., 2007), 종자의 에탄올 추출물에서 페닐알콜유도체인 (3-ethenylphenyl)-1,2-ethanediol (Lü et al., 2024)이 각각 보고되었다. 각 화합물들의 화학 구조는 Fig. 5에 표시하였다.
항염증 성분
β-Sitosterol
대표적인 식물성 스테로이드인 β-sitosterol은 여러 실험모델에서 유의미한 항염증 작용을 나타낸다고 알려져 있다. 여러 연구 결과에 따르면, β-sitosterol은 NF-κB 경로의 억제 및 NLRP3 인플라마좀 활성의 감소를 통해 keratinocytes와 macrophages에서 TNF-α, IL-1β, IL-6, IL-8과 같은 주요 염증성 cytokine의 분비를 부분적으로 억제한다(Chang et al., 2023; Fan et al., 2023; Liao et al., 2018). 동물 모델에서 β-sitosterol은 염증성 유전자 발현을 하향 조절하고 면역세포 유입을 제한함으로써 제브라피시와 생쥐에서 산화스트레스와 염증을 감소시키는 것으로 나타났다(Chang et al., 2023; Zhang et al., 2023b; Zhou et al., 2020). β-Sitosterol은 염증 과정에서 중요한 역할을 하는 5-리폭시게네이스(5-lipoxygenase)와 시클로옥시게네이스-2(cyclooxygenase-2)와 같은 효소를 억제하여 염증을 완화한다(Chakraborty et al., 2021). 또한, β-sitosterol은 TLR4/NF-κB 및 RIG-I/IFN/ STAT을 포함한 면역 신호 경로를 조절하고 항염증성 미세아교세포의 표현형을 촉진함으로써 급성 폐 손상, 신경병증성 통증, 건선양 피부 염증의 완화에 기여하는 것으로 밝혀졌다(Chang et al., 2023; Zheng et al., 2023; Zhou et al., 2020). β- Sitosterol의 항염증 활성은 또한 피부 흡수 개선 및 최소한의 장벽 손상과도 연관되어 있어 국소 요법용 후보물질로서 유망하다(Chang et al., 2023).
Medicarpin
Medicarpin은 isoflavonoid의 일종인 pterocarpan 화합물로 폐경 후 관절염 생쥐 모델에서 medicarpin은 TNF-α, IL-6, IL-17A와 같은 염증성 사이토카인과 염증성 TH17 세포의 증식을 억제하고, 항염증성 사이토카인인 IL-10을 증가시킴으로써 염증을 감소시키고 연골 파괴와 골 손실을 예방하였다(Mansoori et al., 2020). 뇌허혈 생쥐 모델에서는 medicarpin이 뇌 염증을 감소시키고, NF-κB 및 caspase 3의 활성을 억제하며, PI3K/Akt 경로를 통해 신경 보호 인자를 촉진함으로써 생존율과 신경학적 결과를 개선하였다(Chern et al., 2021). 또한 활성화된 미세아교세포에서 일산화질소 생성을 직접적으로 감소시켜 뇌에서 강력한 항염증 활성을 나타냈다(Chern et al., 2021). Dalbergia odorifera에서 분리된 medicarpin은 염증 반응의 주요 매개물질인 류코트리엔 C4 형성을 강력히 억제하는 것으로 밝혀졌으며, 류코트리엔 합성에 관여하는 효소인 5-리폭시게네이스에 대해 뚜렷한 활성을 보였다(Miller et al., 1989). 그러나 네팔 프로폴리스에서 유래한 플라보노이드를 대상으로 한 또 다른 연구에서는 medicarpin이 IL-33 신호 경로나 관련 사이토카인 발현을 억제하지 않아 그 항염증 효과가 경로 특이적일 수 있음을 시사하였다(Funakoshi-Tago et al., 2015). 이러한 연구 결과들은 medicarpin이 자가면역, 신경염증, 류코트리엔 매개 질환에서 항염증 작용제 후보로서의 잠재력을 지니고 있음을 시사한다(Chern et al., 2021; Mansoori et al., 2020; Miller et al., 1989).
Formononetin
Formononetin은 IL-6, IL-1β, TNF-α와 같은 염증성 사이토카인의 생성을 감소시키며, NF-κB, MAPK, JAK-STAT, PI3K-AKT를 포함한 주요 염증 경로를 in vitro와 in vivo에서 모두 억제한다(Ding et al., 2024; Dou et al., 2025; Jia et al., 2022; Yu et al., 2022; Zhang et al., 2023a). 추가적으로, 대식세포의 분극화 및 자가포식을 조절함으로써 항염증작용을 나타낸다(Chen et al., 2021; Xu et al., 2025). 뇌혈관 질환 모델에서, formononetin은 JAK2/STAT3 경로를 표적으로 하여 뇌 허혈-재관류 손상으로부터 보호하며(Yu et al., 2022), ESR1/NLRP3/Caspase-1 신호를 억제하여 천식에서 기도의 염증을 완화한다(Zhang et al., 2023a). 또한, PTEN/AKT/ NF-κB 경로를 조절하여 골관절염의 진행을 늦추는 것으로 나타났다(Jia et al., 2022). 그리고 급성 폐 손상 및 유방염에 있어서도 항산화 작용을 강화하고 장벽 무결성을 유지하여 염증을 감소시키는 효과가 있다(Chen et al., 2021; Xiang et al., 2022). 이러한 연구 결과는 formononetin이 다중 표적 기전 및 낮은 독성을 바탕으로 다양한 염증성 질환에 대한 치료제로서의 잠재력을 지니고 있음을 시사한다(Ding et al., 2024; Dou et al., 2025).
Rutin
Rutin은 메밀에 특히 다량으로 함유되는 플라보노이드로서(Kim et al., 2023) 염증 유발 사이토카인인 TNF-α, IL-1β, IL-6 등의 생성을 억제하며, NF-κB 및 마이토젠 활성화 단백질 키나아제(MAPK) 등 염증 반응의 중심 경로를 차단한다(Jang et al., 2025; Lee et al., 2024; Muvhulawa, et al., 2022). 또한 rutin은 비만세포의 탈과립을 억제하고 P2X7 수용체 활성을 저해함으로써 항염증 및 진통 효과를 높인다(Ye et al., 2023).
동물 모델 실험에서는 rutin이 염증성 장질환을 포함한 여러 염증성 질환의 증상을 완화하며, 질병 활성도 및 산화 스트레스를 감소시키고 장 점막 장벽 기능을 회복시키는 데 효과적임이 밝혀졌다(Wang et al., 2022; Zou et al., 2025). 특히 rutin의 생체이용률 및 항염증 효능을 향상시키기 위해 나노결정, 하이드로겔, 키토산 미세입자 등의 약물 전달 시스템이 개발되었으며, 이들 제형은 일반적인 rutin 단독 투여보다 우수한 염증 완화 및 조직 회복 효과를 나타낸다(Cosco et al., 2016; Hassan and Soliman, 2022; Wang et al., 2022; Yue et al., 2025). Rutin은 배당체 등 유도체와 항염증 비교 연구에서 유사한 항염증 효과를 가지며, 특별한 독성이 없는 점에서 임상 적용에 있어서 장점이 크다(Choi et al., 2021).
현재까지 보고된 연구 결과는 전임상 수준에 국한되어 있으나 rutin을 함유한 식품의 섭취 또는 의약품의 투여가 인체를 대상으로 한 임상 연구에서도 대사 및 염증 지표의 개선에 긍정적 영향을 미칠 가능성을 충분하게 보여주고 있다(Muvhulawa et al., 2022). 이상의 결과를 바탕으로, rutin은 다중 표적 작용 기전과 우수한 안전성을 토대로 염증성 질환의 예방 및 치료에 있어 유망한 식의약품 후보 물질로 간주될 수 있다(Jang et al., 2025; Lee et al., 2024; Muvhulawa et al., 2022; Zou et al., 2025).
Methyl gallate
Methyl gallate는 호중구의 집적을 억제하고 IL-1β, IL-6, TNF-α 및 프로스타글란딘과 같은 염증 매개물질의 생성을 감소시키며, 대식세포의 활성화 및 NF-κB와 MAPK와 같은 관련 신호 전달 경로를 억제함으로써 염증을 완화한다(Chae et al., 2010; Correa et al., 2016; Correa et al., 2020; Correa et al., 2022).
관절염 및 대장염 동물 모델에서 methyl gallate의 투여는 부종, 백혈구 침윤, 조직 손상의 감소를 초래하였으며, 그 효능은 표준 항염증 약물과 유사하지만 독성이 낮은 것으로 나타났다(Anzoise et al., 2018; Correa et al., 2016; Correa et al., 2022). 또한, methyl gallate는 장내 미생물 균총을 조절하고 TLR4/NF-κB 신호 경로를 억제하여 궤양성 대장염에 대한 보호 효과를 나타낸다(Zhou et al., 2022). 추가적으로, methyl gallate와 그 유도체는 COX-2 및 TNF-α의 유전자 발현을 감소시키는 잠재력을 보여 항관절염 특성을 더욱 강화한다(Sharanya et al., 2023). Methyl gallate의 나노미셀 제형은 관절염 모델에서 생체이용률과 항염증 작용을 강화시킨다(Pereira et al., 2023).
Kaempferol-3-O-rutinoside
Kaempferol-3-O-rutinoside는 플라보노이드 배당체로 리포폴리사카라이드(LPS)로 자극한 대식세포 모델에서 주요 염증 매개물질인 산화질소, 종양괴사인자-α(TNF-α), 인터루킨-6(IL-6) 등의 생성을 억제하고, 효과를 나타내는 농도에서 세포독성을 나타내지 않으면서 유도성 산화질소 합성효소(iNOS)와 사이클로옥시게나제-2(COX-2)의 발현을 저하시킨다(Hua et al., 2021; Hwang et al., 2019).
이 항염증 작용은 주로 NF-κB 및 MAPK 신호 전달 경로의 억제와 함께, TLR4/MyD88/NF-κB 축의 차단 및 AMPK/ SIRT1 경로의 조절에 의해 매개되며, 이것은 모두 염증 반응의 조절에 중요한 역할을 한다(Hu et al., 2021; Hua et al., 2021; Hwang et al., 2019; Ma et al., 2023). 추가로, kaempferol- 3-O-rutinoside는 혈관내피 성장인자-C(VEGF-C)와 결합하여 염증을 촉진하는 사이토카인의 분비를 추가적으로 줄여주고 대식세포의 이동을 억제함으로써 항염증 효과를 높여준다(Hu et al., 2021). 이러한 연구 결과는 kaempferol-3-O- rutinoside가 과도한 염증이나 만성 염증 관련 질환 치료제로 유망한 후보로 볼 수 있다(Hu et al., 2021; Hua et al., 2021; Hwang et al., 2019; Ma et al., 2023).
Lupeol
Lupeol은 펜타사이클릭 트리테르펜으로, 세포 및 동물 모델 모두에서 유의미한 항염 효과를 나타낸다. 연구 결과에 따르면 lupeol은 COX-2와 iNOS뿐만 아니라 TNF-α, IL-1β, IL-6 등의 염증 촉진 사이토카인의 생성을 억제하는 동시에, 세포 내 항산화 시스템에서 중요한 역할을 하는 단백질인 헴 옥시게나제-1(HO-1)과 핵 인자 적혈구 2 관련 인자 2(Nrf2)와 같은 항염증 경로를 활성화시키는 것으로 보고되었다(Fernández et al., 2001; Park et al., 2024; Zhu et al., 2016).
관절염, 대장염, 피부 상처 동물모델실험에서 lupeol이 염증을 줄여주었고, 항염증제와 비교할 때 동등하거나 더 우수한 효과를 나타내면서 부작용은 적은 것으로 나타났다(Geetha and Varalakshmi, 2001; Pereira Beserra et al., 2020). Lupeol은 핵 인자 카파B(NF-κB)의 활성화를 억제하고, 대식세포를 염증 촉진형인 M1에서 항염증형인 M2로 전환시켜 특히 염증성 장질환과 같은 만성 염증성 질환에서 효과를 나타낸다(Saleem, 2009; Zhu et al., 2016). 그리고 lupeol은 TLR4-PI3K- Akt-NF-κB 신호전달 경로를 억제함으로써 심장 비대와 섬유증을 감소시키며, 이를 통해서 심혈관 보호 효과를 나타낸다(Li et al., 2022). 또한, lupeol을 국소적으로 염증성 사이토카인의 감소와 조직 재생 촉진을 통해 상처 치유를 촉진한다(Pereira Beserra et al., 2020).
Trilinolein
Trilinolein은 트리아실글리세롤이며, LPS로 자극된 대식세포에서 산화질소, TNF-α, IL-1β, IL-6의 생성을 억제하고, iNOS, COX-2, NF-κB, MAPKs와 같은 염증 관련 단백질의 발현을 감소시켜 마우스 족부종 모델에서 항염증효과를 나타낸다(Huang et al., 2014). Trilinolein은 내피세포에서 산화 LDL로 유도한 산화 스트레스와 염증을 감소시키며, 세포 사멸 및 접착 분자 발현을 줄여주며, 혈관 염증에 대한 보호역할을 한다(Luo et al., 2014).
최근 연구에서는 trilinolein이 각질형성세포의 미토콘드리아 기능 부전을 회복시키고 산화 스트레스를 감소시킴으로써 아토피 피부염과 유사한 피부 병변 완화 효과를 보고 하였고, 이 효과는 주로 AhR-Nrf2 경로를 통한 피부 장벽 기능 회복과 항염증 효과와 관련된다(Wang et al., 2024). 그리고, trilinolein은 염증 조절의 핵심 기전인 AMPK-mTOR 신호 전달 경로를 통해 자가포식을 촉진함으로써 UVB에 의한 피부 손상으로부터 피부 세포를 보호한다(Lin et al., 2024). 지금까지 연구 결과를 통해서 trilinolein은 염증신호 전달 경로 억제, 산화 스트레스 감소, 세포 재생 과정 촉진 등의 기전을 통해 항염증 효과를 나타낸다(Huang et al., 2014; Lin et al., 2024; Luo et al., 2014; Wang et al., 2024).
Robinin
Robinin은 플라보놀 배당체로서 관절염 동물 모델에서 단독 투여 시 염증 감소가 유의미하지 않았으나 엽산 대사 길항작용을 가진 면역억제제인 metothrexate와 병용 투여한 경우 인터루킨-17A 및 관절 효소 활성 등 염증 표지자의 감소 효과가 증진되는 결과를 나타내었는데 이는 표준 항염증 약물과 약한 시너지 효과가 있음을 나타낸다(Tsiklauri et al., 2021). 췌장암 관련 세포 실험에서는 robinin이 세포 증식과 이동을 억제하고, 염증성 사이토카인인 IL-6와 TNF-α의 발현을 유의미하게 감소시켰으며, 이러한 효과는 TLR2–PI3K–AKT 신호 전달 경로의 억제와 관련이 있다(Zhang et al., 2023c). 이러한 연구 결과는 robinin이 주요 염증 경로와 사이토카인의 조절을 통해 항염증 효과를 나타내며, 염증성 질환 및 일부 암에 대한 보조 치료제로서의 잠재력을 지니고 있음을 시사한다(Tsiklauri et al., 2021; Zhang et al., 2023c).
Gallic acid
Gallic acid는 식물계에서 흔히 발견되는 phenolic compound로 방향족산으로 구분할 수 있다. Gallic acid는 TNF-α와 IL-6와 같은 염증을 촉진하는 사이토카인의 생성을 억제하고, 리놀레산 및 아라키돈산 대사를 포함한 급성 염증 관련 대사 경로를 조절함으로써 염증을 감소시킨다(Bai et al., 2021; Wu et al., 2022).
Gallic acid는 염증 반응의 중심 역할을 하는 NF-κB 및 MAPK 신호 전달 경로의 활성화를 억제하여 염증 매개 물질의 분비를 줄이고 조직의 무결성을 보호한다(Bai et al., 2021; Cai et al., 2022; Zhu et al., 2019). 통풍성 관절염 모델에서는 gallic acid가 NLRP3 인플라마좀과 세포용해(pyroptosis)를 Nrf2 신호 경로의 강화로 억제함에 따라 관절의 부종이 감소하고 염증 세포의 침윤이 줄어드는 효과를 보였다(Lin et al., 2020).
제왕절개 수술을 받은 산모의 자궁 근육층과 태아막, 그리고 동물 모델 실험에서 gallic acid가 염증 유발 사이토카인, 케모카인, 그리고 조직 재형성 효소의 발현을 억제하여 조산 예방 및 궤양성 대장염 치료에 효과적일 수 있음이 입증되었다(Nguyen- Ngo et al., 2020; Zhu et al., 2019). 또한, gallic acid는 독성 없이 산화 스트레스와 염증 표지자를 감소시켜 안염 및 안구건조증을 개선하며(Li et al., 2023), in vitro에서도 농도 의존적으로 단백질 분해효소 활성과 알부민 변성을 억제하는 항염증 특성을 보였다(Agrawal et al., 2021).
β-adenosine
β-adenosine은 주로 A2A 및 A2B 수용체를 통해 면역세포의 활성과 염증 반응을 억제하는 것으로 알려져 있으며, 특히 중성구와 대식세포의 활성, 산화 스트레스, 그리고 세포 부착을 감소시킨다(Cronstein, 1985; Cronstein and Sitkovsky, 2017; Haskó and Cronstein, 2013). adenosine은 류마티스 관절염, 건선, 피부염 등 다양한 염증성 질환에서 IL-6, TNF-α와 같은 염증 매개물질의 생성을 억제하고, IL-10과 같은 항염증성 사이토카인의 생성을 촉진한다(Chen et al., 2024; Cronstein and Sitkovsky, 2017; Sohn et al., 2021). 더불어, adenosine의 항염증 효과는 CD39와 CD73 효소에 의해 조절되는데, 이 효소들이 활성화되면 세포 외부에서 adenosine이 생성되어 염증을 억제하는 기전을 보인다(Caiazzo et al., 2016; Regateiro et al., 2011; Sohn et al., 2021). 최근에는 adenosine 수용체를 직접 표적으로 하는 치료제 개발 연구가 활발히 진행되고 있으며, 피부 질환을 포함한 여러 염증성 질환에서 긍정적인 결과들이 보고되고 있다(Chen et al., 2024; Cronstein and Sitkovsky, 2017). 이와 같이, adenosine은 다양한 경로를 통해 강력한 항염증 효과를 나타내며, 이를 활용한 치료 전략이 여러 염증성 질환에서 유망하게 평가되고 있다(Caiazzo et al., 2016; Chen et al., 2024; Cronstein, 1985; Cronstein and Sitkovsky, 2017; Haskó and Cronstein, 2013; Sohn et al., 2021).
고 찰
작두콩으로부터 용매추출, 컬럼크로마토그래피법을 이용한 분리 및 정제, 구조결정을 통해 화학적으로 동정된 성분을 기반으로, 염증 관련 활성 성분을 고찰하였다. 작두콩에서는 flavonoids, terpenoids, steroids, 유기산, 아민계 화합물 등 다양한 생리활성 화합물이 분리되었으며, 이들 중 일부는 항염증 활성을 확인 할 수 있었다.
항염증 작용을 갖는 성분으로는 β-sitosterol, formononetin, medicarpin, rutin, methyl gallate, kaempferol-3-O- rutinoside, lupeol, trilinolein, robinin, gallic acid 등이 있으며, 이들 성분은 NF-κB, MAPK, TLR4, NLRP3 inflammasome 등의 염증 관련 신호 전달 경로를 억제하거나 조절하여 염증 매개물질의 생성을 감소시키는 기전을 갖는다. 일부 화합물은 면역세포의 분극, 장벽 기능 유지, 산화스트레스 억제 등 다양한 다중 기전으로 항염증 효과를 나타낸다.
결론적으로, 작두콩은 전통적으로 활용되어 온 한약으로서 과학적 근거에 기반한 항염증 효과를 갖는 다양한 화합물을 함유하고 있으며, 앞으로 식의약 소재로의 개발 가능성이 높다. 또한 본 연구는 추정 화합물이 아닌 구조적으로 확인된 성분을 중심으로 항염증 작용을 평가함으로써 작두콩의 기능성 및 의약적 활용에 대한 기초자료를 제공하였다.
적 요
작두콩(Canavalia gladiata)은 아시아 각 지역에서 전통의약으로 사용되어 온 콩과 식물로, 최근 그 다양한 생리활성 화합물과 항염증 효능으로 과학적 관심을 받고 있다. 최근 식물화학연구에서 씨앗, 열매, 뿌리 등에서 플라보노이드, 테르페노이드, 스테로이드, 유기산, 질소 함유 화합물, 페놀 유도체 등 다양한 생리활성 화합물이 확인되었다. 본 리뷰는 크로마토그래피를 이용한 분리·정제 및 NMR 분석을 기반으로 화학적 구조가 규명된 화합물들을 중심으로 작두콩의 항염증 효능 화합물에 대한 연구 동향을 정리하고 기능성 식품 또는 의약품 개발을 위한 기초 자료를 제공하고자 한다.