서 언
재료 및 방법
시약
실험 재료 및 건조 조건
추출 및 농축
항산화 물질 함량 및 활성 분석
세포 배양
세포 독성
산화질소 생성 억제 활성
통계분석
결과 및 고찰
가용성 고형분 수율
항산화 물질 함량 분석
DPPH 및 ABTS 라디칼 소거능
항염증 활성
적 요
서 언
최근 천연물 기반 기능성 소재에 대한 수요가 증가함에 따라 식물 유래 생리활성 물질의 활용 가능성이 크게 주목받고 있다(Lourenço et al., 2019; Mudondo et al., 2025; Parveen et al., 2025). 항산화, 항염증, 항노화, 항비만 등 다양한 생리활성으로 인해 식품, 의약품, 화장품 산업 등에서 핵심 소재로 활용되고 있다(Benbaibeche et al., 2025; Patra et al., 2015). 특히 나고야의정서 시행 이후 해외 생물자원의 이용이 제한되면서 국내 자생식물 자원의 탐색과 산업적 활용가치가 더욱 중요해지고 있다.
국내에는 다양한 고유종을 포함한 자생식물이 풍부하며, 이들은 기능성 성분의 원천으로 높은 잠재가치를 가진다. 그러나 대부분 식물 자원은 계절적으로 수확 시기가 제한되고 저장성이 낮아 안정적인 공급이 어렵다. 대부분의 식물은 수분 함량이 80% 이상으로 높아 미생물 증식, 효소반응 및 산화적 변화가 쉽게 일어나 품질이 빠르게 저하될 수 있다(Belwal et al., 2022). 따라서 수분을 제거하거나 감소시키는 건조 과정은 식물 소재의 안정화를 위한 중요한 보존 기술 중 하나로 널리 활용된다(Rocha et al., 2011). 건조는 단순히 수분을 제거하는 과정이 아니라 식물 소재의 농축, 안정화, 장기 저장성 확보 및 가공 적합성 향상을 가능하게 하는 핵심 공정이다(Eapen et al., 2025). 또한 다양한 건조 기술은 열 분해, 산화적 변화 또는 효소 반응을 유도하여 식물 화학적 프로필 및 생리 활성에 영향을 미친다(Saikia et al., 2016). 따라서 특성에 따라 적합한 건조 방법을 선택하는 것이 중요하다.
쑥부쟁이속(Aster spp.)은 국화과(Asteraceae)에 속하는 다년생 초본으로 국내에는 약 26종의 쑥부쟁이속 식물이 자생하고 있으며(KPNIC, 2025), 관상용, 약용 및 식용으로 활용되고 있다. 특히 쑥부쟁이(Aster indicus), 개쑥부쟁이(Aster meyendorffii), 섬쑥부쟁이(Aster pseudoglehnii) 등을 포함한 10여 종이 식품공전에 등재된 원료로 안전성이 확보되어 있으며(MFDS, 2025), 항산화, 항염증, 항종양, DNA 손상 억제 등 다양한 생리활성이 보고되어 기능성 소재로서 잠재력이 높다(Lee et al., 2022; Ngabire et al., 2018). 그러나 쑥부쟁이속 식물의 종 간 생리활성 비교 연구는 제한적이며, 특히 건조방법과 같은 가공 공정이 쑥부쟁이속 기능성 변화에 대한 연구는 거의 이루어지지 않았다. 따라서 본 연구에서는 생물자원으로서 잠재적 가치가 높은 자생 쑥부쟁이속 5종을 대상으로 건조방법에 따른 생리활성을 비교하여 품질 향상 및 생리 활성 유지에 효율적인 건조 조건을 구명하고자 한다.
재료 및 방법
시약
본 연구에 사용된 시약 중1,1-diphenyl-2-picrylhydrazyl (DPPH), 2,2’-azino-bis (3-ethylbenzothiazoline-6-sulphonic acid) (ABTS), 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT), diethylene glycol (DEG), dimethyl sulfoxide (DMSO), Folin-Ciocalteu’s reagent, Griess reagent, lipopolysaccharide (LPS), naringin, potassium peroxydisulfate, sodium carbonate, sodium nitrite, tanninc acid는 Sigma-Aldrich Co. (St. Louis, MO, USA)에서 구입하였다. 1N sodium hydroxide solution및 Ethyl alcohol은 각 Samchun Chemical Co. (Pyungtack, Korea) 및 Dukans (Ansan, Korea)에서 구입하여 사용하였다. Dulbecco’s modified Eagle’s medium (DMEM), fetal bovine serum (FBS), penicillin/streptomycin는 Cytiva (Logan, UT, USA)에서 구입하였다.
실험 재료 및 건조 조건
추산쑥부쟁이(Aster × chusanensis), 단양쑥부쟁이(A. danyangensis), 눈갯쑥부쟁이(A. hayatae), 개쑥부쟁이(A. meyendorffii), 섬쑥부쟁이(A. pseudoglehnii)를 2022년 8월 5일에 안동대학교 유전자원포에서 수확하였다. 건조처리는 동결건조(FD) 및 풍건(AD) 두 가지 방법으로 수행하였다. 동결건조는 시료를 액체질소로 동결한 후 동결건조기(FD8508, lishinbiobase Co. Ltd., Korea)를 사용하여 콜드 트랩온도 -80℃, 작동 압력 5 mTorr 이하의 조건에서 건조하였다. 풍건은 25℃의 실험실에서 선풍기를 이용하여 건조하였으며, 두 건조 방법 모두 시료의 무게가 일정하게 유지되는 시점까지 진행되었다. 이후 건조된 시료는 분쇄 후 실험에 사용하기 전까지 -80℃에서 보관하였다.
추출 및 농축
쑥부쟁이속 5종의 유효성분을 추출하기 위해 분쇄된 건조 시료(1 g)를 50% 에탄올 50 mL에 침지한 후 45분 동안 초음파 추출하였다. 추출액은 여과지로 여과한 후 회전감압농축기를 이용하여 농축하였다.
항산화 물질 함량 및 활성 분석
항산화 물질 함량은 총 폴리페놀 및 플라보노이드 함량 분석을 수행하였으며, 항산화 활성은 ABTS 및 DPPH 라디칼 소거 활성능을 평가하였다. 이전 연구(Lee et al., 2023)와 동일한 방법으로 수행하였으며, 총 폴리페놀은 tannic acid, 플라보노이드는 naringin을 표준물질로 사용하여 각 함량을 계산하였다. 항산화 활성 분석은 라디칼 소거능을 전자공여능(EDA %)로 계산하였으며, EDA가 50%가 되는 시료의 농도 [Reduction concentration of 50% (RC50), ㎎·mL-1]를 비교하였다.
전자공여능(EDA, %): [(공시험 흡광도 – 시료의 흡광도) / 공시험 흡광도] × 100
세포 배양
항염증 활성 분석을 위해 RAW264.7 세포주를 한국세포주은행(KCLB, Korea Cell Line Bank, Seoul, Korea)으로부터 분양받아 사용하였다. DMEM 배지에 10% FBS 및 1% penicillin/streptomycin (100U/mL)을 첨가하였으며, 배양조건은 5% CO₂ 및 37℃ 환경에서 2일 간격으로 계대배양하였다.
세포 독성
각 시료 추출물의 세포 독성은 MTT assay를 이용하여 측정하였다. 96-well plate에 7.5 × 10⁵ cells/mL 농도의 세포를 well 당 200 μL를 분주하여 6시간 동안 처리한 후, 각 LPS (1 ㎍·mL-1), quercetin (50 μM) 및 시료(100 ㎍·mL-1)을 처리하여 18시간을 추가적으로 배양하였다. 이후 1 ㎎·mL-1의 MTT 시약을 well 당 10 μL씩 90분간 처리한 후 DMSO로 용해하여 550 ㎚에서 ELISA reader를 이용하여 흡광도를 측정하였다.
산화질소 생성 억제 활성
산화질소 생성량은 상기 언급된 방법과 같이 처리된 세포의 배양액 100 μL와 Griess 시약 100 μL를 혼합하여 10분간 반응시켰다. 이후 ELISA reader를 이용하여 550 ㎚에서 흡광도를 측정하였으며, sodium nitrate로 표준곡선을 작성하여 산화질소의 함량을 산출하였다. 항염증 활성 분석 실험은 세포독성을 띄지 않는 처리구를 대상으로 진행하였다.
통계분석
추출 수율, 항산화 물질 함량 및 활성 분석 실험은 3회 반복하였으며, 항염증 활성 분석은 6 회 반복하여 수행하였다. 모든 데이터는 평균 ± 표준오차로 제시하였다. 전체 처리구 간 평균 비교는 일원 분산분석(one-way ANOVA) 후 Tukey’s range test를 통해 p <0.05 수준에서 유의성을 검정하였으며, 동일 종 내에서 건조방법에 따른 차이를 확인하기 위해 독립표본 t-test를 병행하여 분석하였다. 또한 건조방법(요인A)과 종(요인 B)의 상호작용을 확인하기 위해 이원 분산분석(two-way ANOVA)을 수행하였다. 모든 통계분석은 SAS 프로그램(version 9.4, SAS Institute Inc., Cary, NC, USA)을 사용하였다.
결과 및 고찰
가용성 고형분 수율
쑥부쟁이속 5종의 가용성 고형분 추출 수율은 3.0-15.5%로 건조방법과 종에 따라 상이한 결과를 나타냈다(Table 1). 눈갯쑥부쟁이 AD는 15.5%로 모든 처리구 중 가장 높은 수율을 보였으며, FD 대비 AD에서 약 1.8배 증가하여 건조 방법의 영향이 뚜렷하게 나타났다. 반면, 단양쑥부쟁이는 AD (6.0%)에 비해 FD (10.5%)에서 약 1.6배 높은 수율을 보였다. 한편, 개쑥부쟁이 FD 및 AD에서 각 3.8 및 3.0%로, 다른 종에 비해 유의적으로 낮은 수율을 보였으며, 건조방법에 따른 차이도 상대적으로 크지 않았다. 이러한 결과는 수율이 추출물 내 총 용해성 고형분의 지표로, 종별 조직 구조 및 수분함량에 따른 추출 효율의 차이를 반영하는 것으로 판단된다.
Table 1.
Soluble solid of extract yield of five Aster species as influenced by drying methods.
| Plant species | Dry method | Yield (%) |
| Aster × chusanensis | FDz | 10.7 ± 0.17 bcx |
| ADy | 9.8 ± 1.09 b | |
| Aster danyangensis | FD | 10.5 ± 0.50 b |
| AD | 6.0 ± 0.29 cd | |
| Aster hayatae | FD | 8.5 ± 1.26 bc |
| AD | 15.5 ± 0.29 a | |
| Aster meyendorffii | FD | 3.8 ± 0.43 d |
| AD | 3.0 ± 0.58 d | |
| Aster pseudoglehnii | FD | 9.2 ± 1.17 bc |
| AD | 9.0 ± 0.29 bc |
항산화 물질 함량 분석
쑥부쟁이속 5종의 항산화 물질 함량은 건조 방법 및 종에 따른 뚜렷한 차이를 보였으며, 이원 분산분석 결과, 건조방법(A), 종(B) 및 상호작용 (A × B) 모두에서 유의한 효과가 확인되었다(Table 2; p <0.05). 이러한 결과는 동일 속(genus)이라도 종(species)별로 조직 구조, 수분함량에 따라 대사성분 조성에 차이가 존재하며, 이로 인해 건조 과정에서 페놀성 화합물의 분해 정도와 보존 효율이 상이하게 나타날 수 있다는 선행 연구들과도 일치한다(Hajimehdipoor et al., 2012; Nguyen et al., 2022; Özcan et al., 2021; Saifullah et al., 2019; Skendi et al., 2023).
Table 2.
Two-way ANOVA results for antioxidant parameters of five Aster species as influenced by drying methods.
| Significancez | TPC | TFC | DPPH | ABTS |
| A | *** | *** | *** | NS |
| B | *** | *** | *** | *** |
| A × B | *** | *** | *** | *** |
먼저 추산쑥부쟁이 및 단양쑥부쟁이는 FD의 총 폴리페놀 함량은 각 73.0 및 61.7 ㎎ TAE·g-1으로 AD에 비해 유의적으로 높은 함량을 보였다(Fig. 1). 두 종의 플라보노이드 또한 AD와 비교하여 FD에서 각 1.3 및 1.2배 함량이 증가하였다(Fig. 2). FD는 낮은 온도에서 빠르게 수분이 제거되어 열에 민감한 물질의 손실이 최소화되었기 때문으로 판단된다(Zhang, 2019). 따라서 저온 기반 건조가 추산쑥부쟁이 및 단양쑥부쟁이의 페놀성 화합물의 보존에 효과적임을 보여준다. 반면 눈갯쑥부쟁이 및 섬쑥부쟁이의 폴리페놀 함량은 FD 처리(54.3 및 45.2 ㎎ TAE·g-1)보다 AD 처리(55.9 및 81.2 ㎎ TAE·g-1)에서 높은 함량을 보였으며, 특히 섬쑥부쟁이 AD의 총 페놀 함량은 5종 중 유의적으로 가장 높은 값을 보였다. 플라보노이드 함량 또한 눈갯쑥부쟁이, 개쑥부쟁이 및 섬쑥부쟁이 모두 AD처리에서 각 14.8, 5.63 및 89.58% 증가하였다.
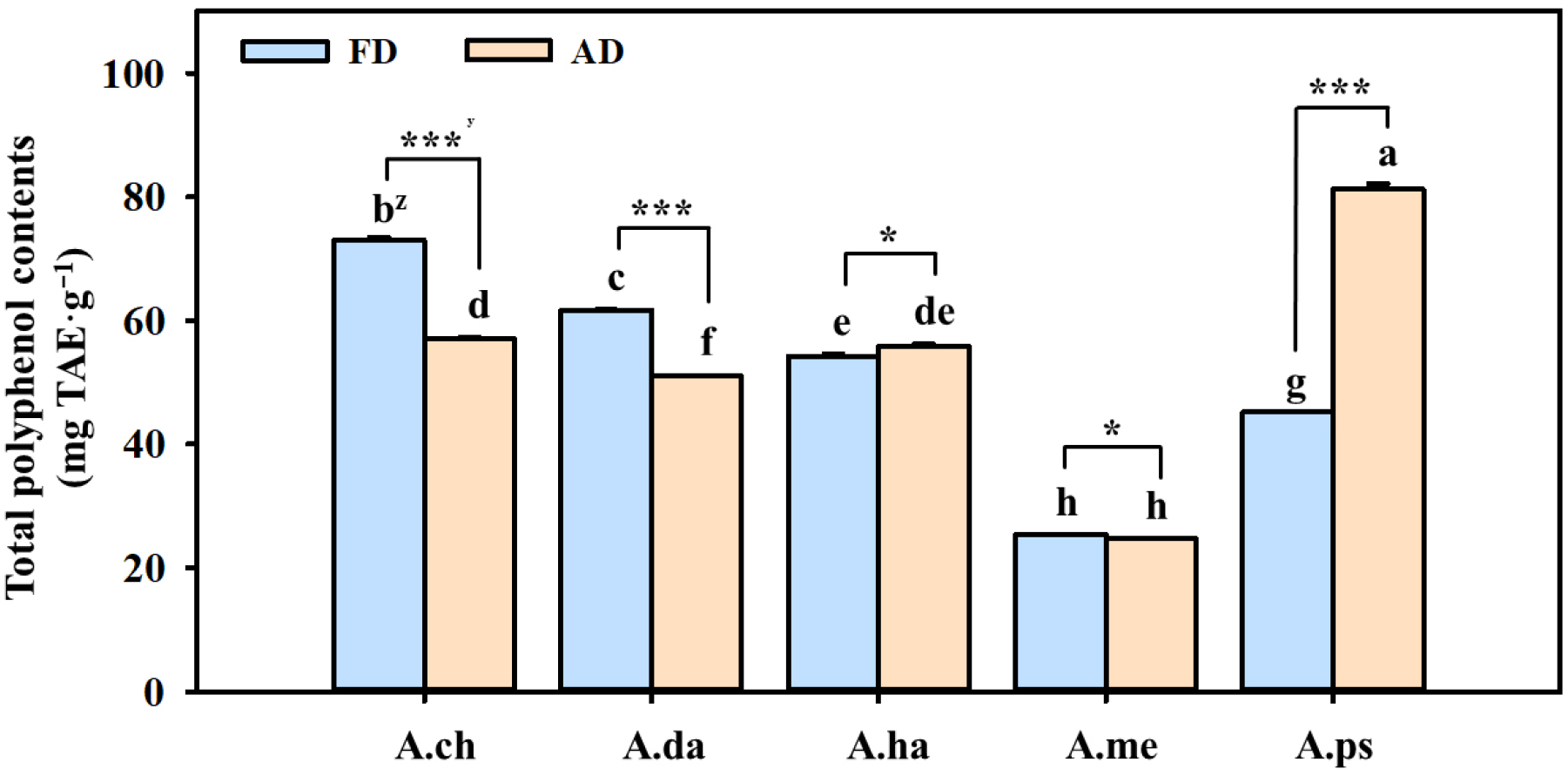
Fig. 1.
Total polyphenol contents of five Aster species as influenced by drying methods. FD; Freeze drying, AD; Air drying. A.ch; Aster × chusanensis, A.da; A. danyangensis, A.ha; A. hayatae, A.me; A. meyendorffii, A.ps; A. pseudoglehnii. zDifferent lowercases letters indicate significant difference based on Tukey’s HSD test at p < 0.05 (n = 3). yAsterisks indicate significant differences within the same species between different drying methods by t-test (*, p <0.05; ***, p <0.001).
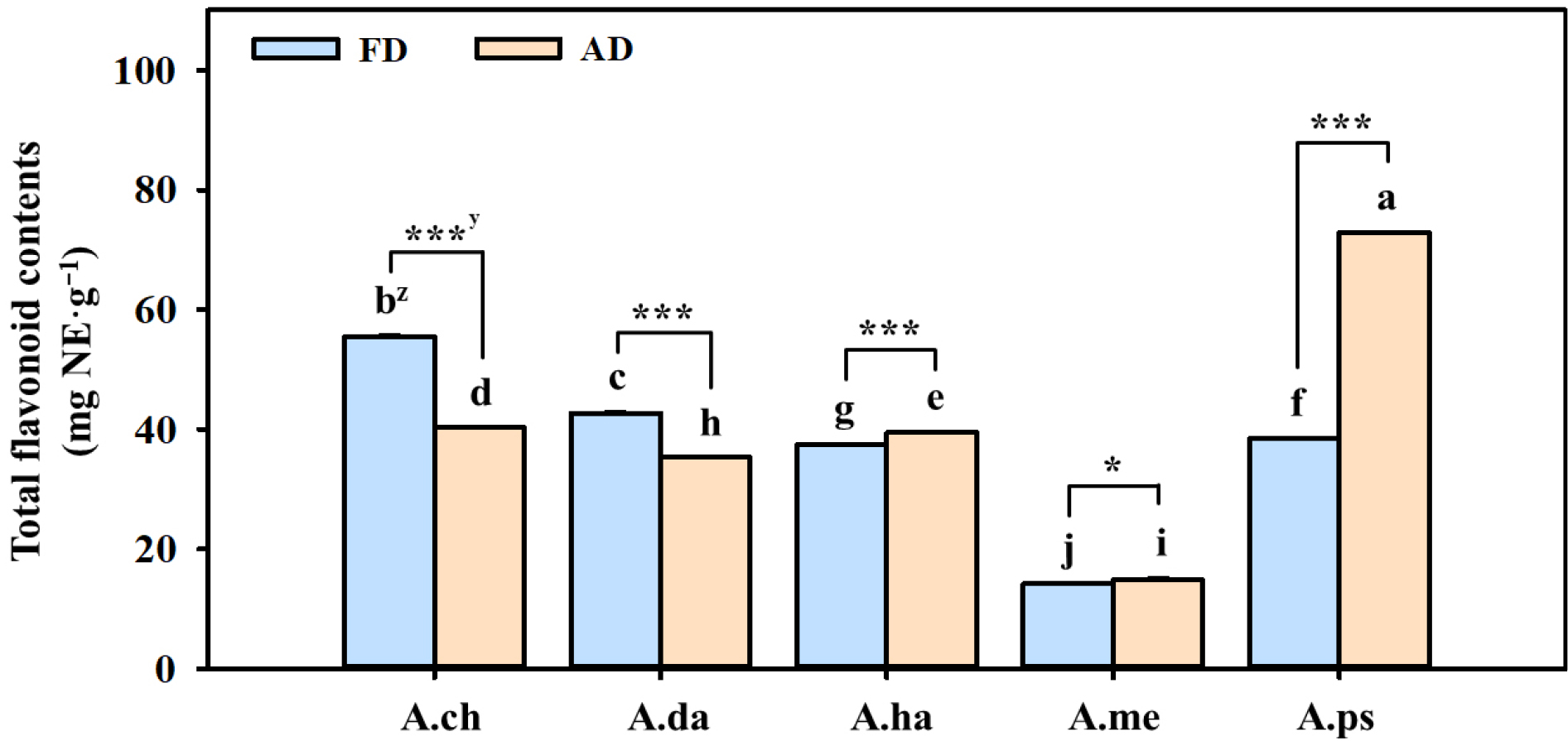
Fig. 2.
Total flavonoid contents of five Aster species as influenced by drying methods. FD; Freeze drying, AD; Air drying. A.ch; Aster × chusanensis, A.da; A. danyangensis, A.ha; A. hayatae, A.me; A. meyendorffii, A.ps; A. pseudoglehnii. zDifferent lowercases letters indicate significant difference based on Tukey’s HSD test at p < 0.05 (n = 3). yAsterisks indicate significant differences within the same species between different drying methods by t-test (*, p <0.05; ***, p <0.001).
선행연구에 따르면 건조 온도 및 시간이 증가함에 따라 총 페놀 함량이 증가하는 경향이 보고되었다(Chang et al., 2006). 이는 열처리 과정에서 고분자 페놀성 화합물이 저분자로 전환되거나(Kim et al., 2018a), 세포벽을 비롯한 조직의 파괴로 인해 phenol계 유도체의 가용화 및 추출이 용이해진 것으로 보고되었다(Kim et al., 2013). 본 연구의 일부 종에서 AD 처리시 총 폴리페놀 및 플라보노이드 함량이 증가한 결과 또한 상대적으로 높은 건조 온도에 의한 열 스트레스가 항산화 물질의 유리 및 추출을 유도한 결과로 해석할 수 있다.
DPPH 및 ABTS 라디칼 소거능
건조방법 및 종별 항산화 활성을 평가하기 위해 DPPH 및 ABTS 라디칼 소거능을 측정하였다. 두 분석 방법 모두 free radical의 소거에 따라 흡광도가 감소하며, 낮은 RC50 값은 높은 항산화 활성을 의미한다. DPPH 라디칼 소거활성 분석 결과, 추산쑥부쟁이를 제외한 4 종에서 AD가 FD에 비하여 유의적으로 높은 항산화 활성을 나타내었다(Fig. 3). 특히 섬쑥부쟁이 AD의 RC50은 1.1 ㎎·mL-1로, FD (5.23 ㎎·mL-1)에 비해 약 4.75배 감소하여 건조방법 간의 가장 큰 차이가 확인되었다(p <0.001). 반면 추산쑥부쟁이는 AD 및 FD 간의 유의적인 차이를 보이지 않았다. ABTS 라디칼 소거능에서는 DPPH 결과와 상이한 경향이 관찰되었다(Fig. 4). 섬쑥부쟁이를 제외한 모든 처리구에서 FD가 AD보다 높은 활성을 보였으며, 섬쑥부쟁이만이 AD에서 유의적으로 높은 활성이 조사되었다(AD, 0.7 ㎎·mL-1; FD, 1.65 ㎎·mL-1).
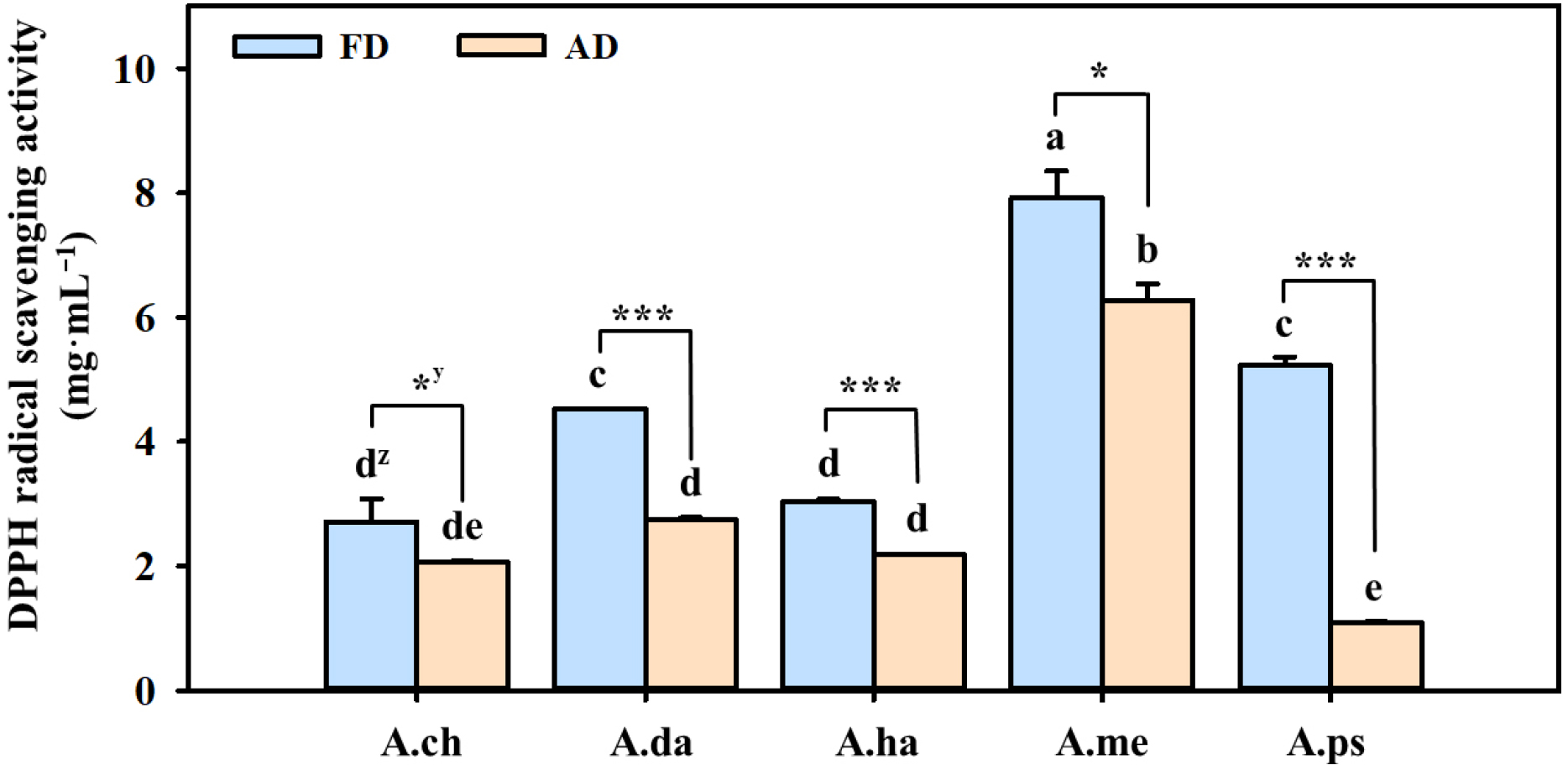
Fig. 3.
DPPH radical scavenging activity of five Aster species as influenced by drying methods. FD; Freeze drying, AD; Air drying. A.ch; Aster × chusanensis, A.da; A. danyangensis, A.ha; A. hayatae, A.me; A. meyendorffii, A.ps; A. pseudoglehnii. zDifferent lowercases letters indicate significant difference based on Tukey’s HSD test at p < 0.05 (n = 3). yAsterisks indicate significant differences within the same species between different drying methods by t-test (*, p <0.05; ***, p <0.001).
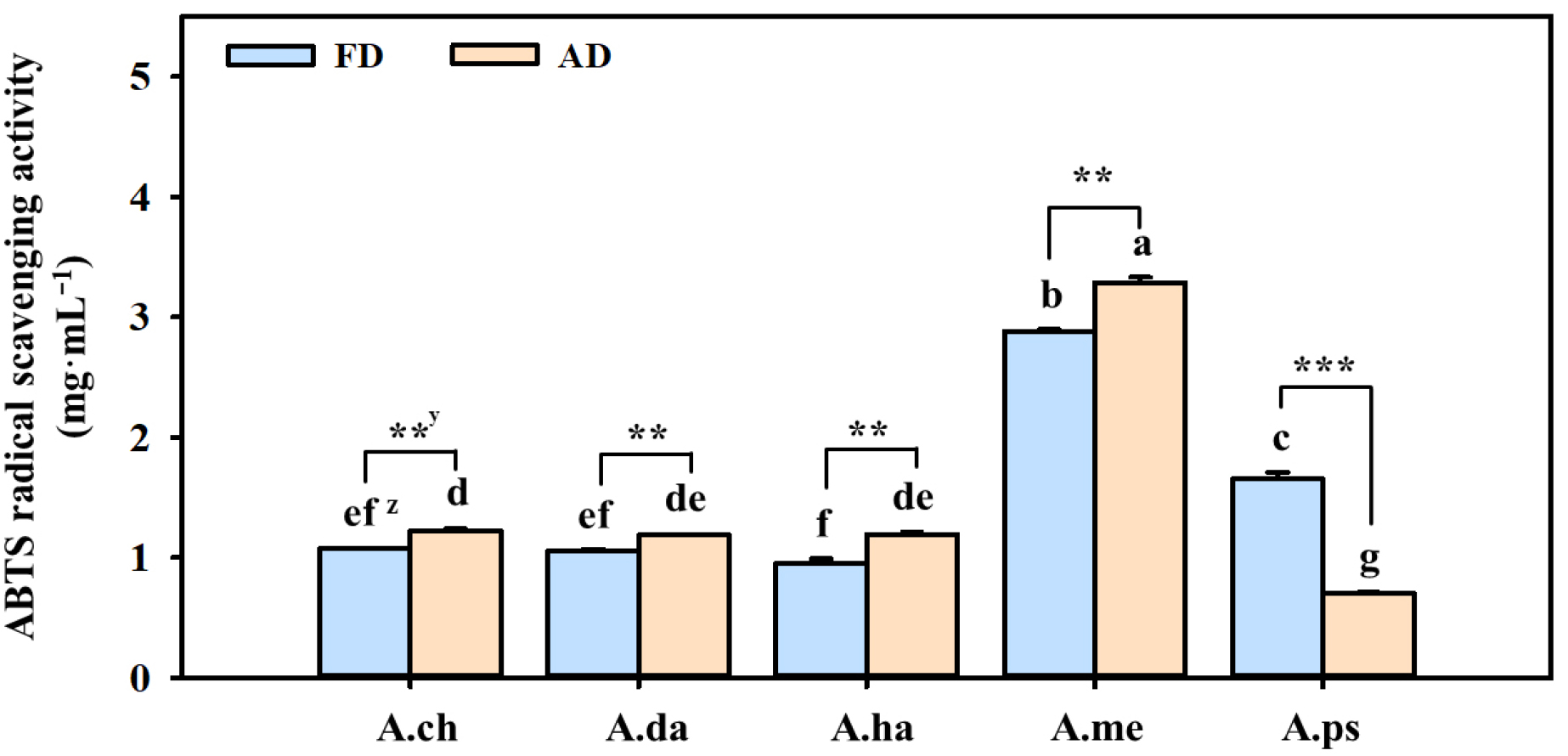
Fig. 4.
ABTS radical scavenging activity of five Aster species as influenced by drying methods. FD; Freeze drying, AD; Air drying. A.ch; Aster × chusanensis, A.da; A. danyangensis, A.ha; A. hayatae, A.me; A. meyendorffii, A.ps; A. pseudoglehnii. zDifferent lowercases letters indicate significant difference based on Tukey’s HSD test at p < 0.05 (n = 3). yAsterisks indicate significant differences within the same species between different drying methods by t-test (**, p <0.01; ***, p <0.001).
한편, 개쑥부쟁이 AD 및 FD 모두에서 RC50값이 각 3.29 및 2.88 ㎎·mL-1으로 다른 종에 비해 유의적으로 낮은 활성을 보였다. DPPH 및 ABTS 간 서로 다른 경향은 두 라디칼의 반응 특성에 기인하는 것으로 보인다. ABTS 라디칼은 폴리페놀뿐 아니라 다양한 친수성 및 지용성 항산화 물질과 반응하는 반면 DPPH 라디칼은 주로 페놀과 반응하며, 특정 페놀산류나 당류와는 반응하지 않는다(Mareček et al., 2017). 따라서 건조 방법에 따라 페놀성 화합물의 조성 변화가 다르게 나타나면서 분석법별 반응의 경향이 달라진 것으로 판단된다(Kim, 2012). 특히 섬쑥부쟁이에서 AD 처리시 두 분석에서 모두 높은 활성이 관찰된 것은 섬쑥부쟁이에 함유된 caffeic acid, quercetin, rutin 등의 주요 페놀성 성분이 열에 의해 부분적으로 분해되거나 전환되어 항산화 활성이 증가했을 가능성이 있다. Chaaban et al. (2017)은 quercetin 및 rutin이 열에 민감하여 가열 중 분해산물이 새롭게 형성되고, 이들 분해산물 또한 라디칼 소거능을 가진다고 보고한 바 있다. Buchner et al. (2006)은 두 화합물을 60분간 열처리했을 때 약 20% 수준의 새로운 라디칼 소거 활성 물질이 생성됨을 확인하였다. 따라서 본 연구에서 확인된 섬쑥부쟁이 AD 처리구의 높은 DPPH 및 ABTS 활성은 열 노출에 따른 페놀성 화합물의 구조 변화 및 항산화 활성 증가에 영향일 수 있으며, 이는 건조 과정이 항산화 물질의 활성 유지 또는 증진에 중요한 영향을 준다는 것을 시사한다.
항염증 활성
쑥부쟁이속 5종이 RAW264.7 대식세포에 미치는 독성을 MTT assay를 이용하여 세포 생존율을 측정하였다(Fig. 5A). FD 처리구는 추산쑥부쟁이를 제외한 모든 종에서 80% 이상으로 나타났으며, AD 처리구에서도 눈갯쑥부쟁이, 개쑥부쟁이 및 섬쑥부쟁이가 80% 이상의 생존율을 유지하여 항염증 활성 평가에 적합함을 확인하였다. 이러한 결과를 통해 두 건조방법 모두 대부분의 종(100 ㎍·mL-1)에서 세포 독성을 유발하지 않으며, NO 생성 억제능 비교가 가능한 농도 범위에서 시료의 안전성을 확인하였다. RAW264.7 대식세포는 LPS 자극에 의해 NO를 생성하며, 이는 염증 반응의 주요 지표로 활용된다(Jo et al., 2014; Nam, 2024). 이에 따라 건조방법별 쑥부쟁이속의 NO 생성 억제능을 평가하였다(Fig. 5B). FD 처리 시 섬쑥부쟁이를 제외한 4종에서 NO 생성 억제 효과를 보였으며, 특히 개쑥부쟁이는 quercetin보다 더 낮은 NO 생성량을 나타냈다. 한편, AD 처리에서는 모든 시료가 quercetin과 비교하여 유의적인 차이 없이 우수한 NO 생성 억제 효과를 나타내었다. 그 중 눈갯쑥부쟁이는 quercetin에 비해 NO 생성량이 상대적으로 낮은 것으로 확인되었다.
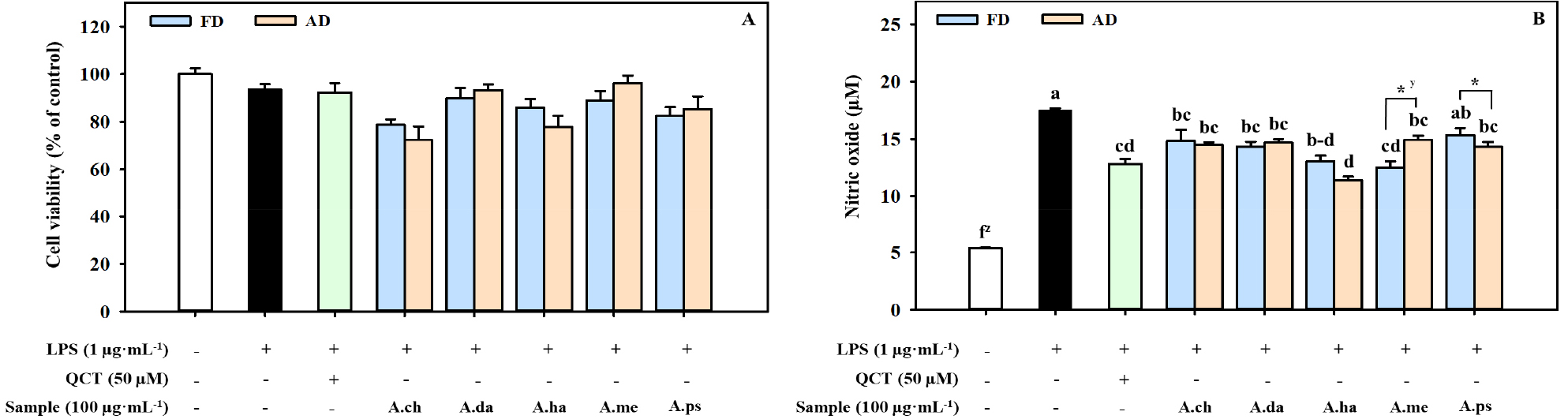
Fig. 5.
Inhibitory effects of five Aster species as influenced by drying methods on cell viability (A) and nitric oxide production (B) in RAW 264.7 macrophages. Cells were co-treated with plant extracts (100 ㎍·mL-1) and LPS for 18 h. FD; Freeze drying, AD; Air drying. LPS; lipopolysaccharide, Qct; quercetin, A.ch; Aster × chusanensis, A.da; A. danyangensis, A.ha; A. hayatae, A.me; A. meyendorffii, A.ps; A. pseudoglehnii. zDifferent lowercases letters indicate significant difference based on Tukey’s HSD test at p < 0.05 (n = 6). yAsterisks indicate significant differences within the same species between different drying methods by t-test (*, p <0.05).
이러한 결과는 항산화 활성과 마찬가지로 건조 조건에 따라 항염증 활성에 기여하는 페놀성 물질 또는 기타 생리활성 성분의 안정성 및 구성 변화가 달라질 수 있음을 시사한다. 또한 Kim et al. (2018b)에 따르면 섬쑥부쟁이 추출물이 NF-kB 신호 억제를 통해 iNOS, COX-2 및 염증성 사이토카인의 발현을 감소시킨다고 보고한 바 있다. 본 연구에서 근본적인 메커니즘을 직접적으로 조사하진 않았으나, 관찰된 NO 억제 활성이 이러한 기전적 배경과 일치하는 경향을 보였다. 전반적으로 쑥부쟁이속 5종은 건조 방법에 따라 LPS 유도 NO 생성 억제 수준에서 유의한 차이를 보였으며, 특정 종에서는 건조 방법이 항염 활성 성분의 보존 및 전환에 긍정적 영향을 미치는 것으로 확인되었다.
본 연구에서는 쑥부쟁이속 5종을 대상으로 동결건조(FD) 및 풍건(AD) 처리에 따른 항산화 및 항염증 활성을 비교하였다. 그 결과, 동일한 속에 속한 식물이라 하더라도 종별로 가장 효과적인 건조방법이 서로 다르며, 또한 동일한 종에서도 건조방법에 따라 생리활성의 정도가 크게 달라질 수 있음을 확인하였다. 이는 건조 방법이 식물 소재의 기능성 평가 및 활용에 있어 핵심적인 요인임을 보여준다. 따라서 종의 특성과 주요 유효성분의 안정성을 고려하여 적절한 건조방법을 선택하는 것이 생리활성 보존 및 증진에 필수적이며, 이는 기능성 식품 및 천연물 기반 소재 개발에서도 중요한 전략적 요인으로 작용할 것으로 판단된다. 본 연구는 국내 자생식물의 활용 가치를 높이기 위한 기초자료를 제시하며, 향후 건조 과정에서의 대사 및 유효성분 변화를 분자·대사체 수준에서 구명하는 후속 연구가 필요하다.
적 요
본 연구에서는 쑥부쟁이속(Aster spp.) 5종을 대상으로 동결건조(FD) 및 풍건(AD) 두 가지 건조방법에 따른 항산화 및 항염증 활성을 비교하였다. 각 시료는 예비실험을 통해 최적 조건으로 선정된 50% 에탄올을 용매로 하여 45분 초음파 추출하였다. 추출 수율은 종과 건조방법에 따라 유의적인 차이를 보였다. 총 폴리페놀 및 플라보노이드 함량은 추산쑥부쟁이(FD: 73.0 ㎎ TAE·g-1; 55.5 ㎎ NE·g-1)와 단양쑥부쟁이(FD: 61.7 ㎎ TAE·g-1; 42.6 ㎎ NE·g-1)에서 FD가 AD보다 높았던 반면, 섬쑥부쟁이(AD: 81.2 ㎎ TAE·g-1; 72.8 ㎎ NE·g-1)와 눈갯쑥부쟁이(AD: 55.9 ㎎ TAE·g-1; 39.4 ㎎ NE·g-1)는 AD 처리에서 더 높은 함량을 보였다. DPPH 및 ABTS 라디칼 소거능 또한 종별로 건조방법에 따라 상이한 경향을 나타냈다. 항염증 활성 평가에서 NO 생성 억제능은 종 및 건조 조건에 따라 유의적 차이를 보였다. 본 연구 결과는 동일 속 식물이라도 종별 특성과 건조 방법에 따라 생리활성의 보존 및 증진 효과가 달라질 수 있음을 제시하며, 기능성 식품 및 바이오헬스 소재 개발에서 건조 공정의 중요성을 뒷받침하는 기초자료로 활용될 수 있다.




