서 언
재료 및 방법
재료수집
시약 및 기기
분석시료 추출
UPLC condition
Method validation
토양 특성 분석
통계분석
결과 및 고찰
분석조건 설정
Method validaiton
Albiflorin, Paeoniflorin 함량
재배지별 작약의 중량
토양특성
작약 토양특성과 중량, 지표성분 간의 상관관계
적 요
서 언
작약(Paeonia lactiflora Pall.)은 작약과(Paeoniaceae)에 속하는 다년생 초본으로 전국적으로 재배되고 있는 식물이다. 생약(한약)에서 사용되는 작약(芍藥, Paeoniae Radix)은 작약(P. lactiflora) 또는 기타동속 근연식물의 뿌리를 사용한다. 한방에서는 유간지통(柔肝止痛), 양혈염음(養血斂陰), 평억간양(平抑肝陽) 등의 효능이 있으며, 주요한 방제로 사군자탕(四君子湯)의 숙지황(熟地黃, Rehmanniae Radix Preparata), 천궁(川芎, Cnidii Rhizoma), 당귀(當歸, Angelicae Giantis Radix)와 같이 배합하여 월경불순, 불임증, 갱년기 장애, 임신중독, 산후증 등에 사용되고 있다(KFDA, 2012; Won et al., 2009).
작약의 성분은 monoterpene glucoside와 monoterpene 두 종류로 구분할 수 있다. 대표적인 주요성분으로는 paeoniflorin, albiflorin, oxypaeoniflorin, benzoylpaeoniflorin, oxybenzoylpaeoniflorin, lactiflorin, galloylpaeoniflorin, paeonin, paeonolide, paeonol, paeoniflorigenone 등으로 대부분의 성분이 monoterpene 배당체이다(He and Dai, 2011; Kim and Han, 2012). 대한민국약전(KH)에서는 paeoniflorin과 albiflorin의 합이 2.3%이상으로 지표성분 함량 기준이 설정되어 있다(KFDA, 2012). 작약의 생리활성에 대한 연구로는 항염증, 면역조절작용, 항관절염 효과 등이 보고된 바 있다(Kim and Han, 2012; Koo et al., 2010; Zhu et al., 2005).
최근 국민소득 향상 및 청정임산물에 대한 관심이 높아지면서 약용임산물에 대한 소비자의 관심 및 수요가 증가하고 있다. 따라서 고품질 약용자원 생산 측면에서 재배적지 구명 및 효율적인 생산관리 기반 구축이 필요하며, 지역의 토양과 기상 등 입지환경에 따른 기능성 성분의 차이가 나타날 수 있으므로 이와 관련된 연구가 요구된다(Eo et al., 2020; Jeong et al., 2021; Kim et al., 2020). 작약 생산·유통 실태조사에 따르면 생산량은 2016년도 797톤에서 2019년도 6,655톤으로 8.3배 증가하였고, 생산액은 2016년도 381억원에서 2019년 1,231억원으로 3.2배 증가하였다(KFS, 2020). 작약의 재배연구로는 식재시기에 따른 생육 및 수량, 수확시기에 따른 albiflorin, paeoniflorin 함량구명 등의 연구가 이루어진 바 있다(Kim et al., 2000; Kim et al., 2006). 그러나 재배지 토양특성이 생육 및 지표성분 함량에 미치는 영향에 대한 연구는 미비한 실정이다.
따라서 본 연구는 전국 다양한 작약 재배지의 토양특성, 식물체 뿌리 생육(중량) 및 albiflorin, paeoniflorin 함량특성을 비교 분석하여 재배지 토양특성이 작약의 albiflorin, paeoniflorin 함량에 미치는 영향을 구명하기 위해 수행하였다.
재료 및 방법
재료수집
본 연구에서 사용한 시료 수집은 2019년도 10월부터 11월까지 전국 26지역 39재배지에서 분주묘를 이식하여 재배한 4년생 작약을 대상으로 분석시료(뿌리) 및 토양을 채취하였다. 수집한 분석시료는 증류수로 세척 후 열풍건조 하였다. 건조가 완료된 시료에 대하여 건중량을 측정 후, 분쇄기로 분쇄한 다음 80 mesh standard sieve를 통과한 분말을 –70 ℃에서 보관하며 분석시료로 사용하였다. 실험에 사용한 시료는 본 연구진의 식물분류학적 동정을 거쳤으며, 시료의 확증표본(FMRRC-2019-KHJ-1~117)을 산림약용자원연구소 소재은행 표본실(FMRRC)에 보관 중이다.
시약 및 기기
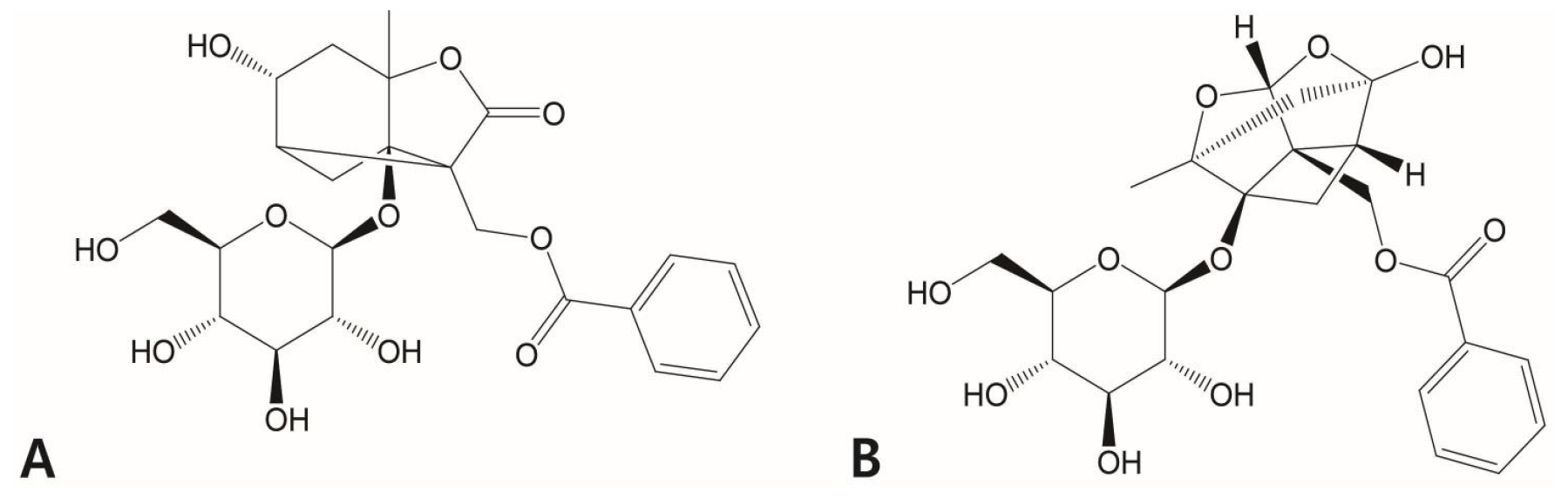
분석에 사용된 albiflorin, paeoniflorin 표준품은 Sigma에서 구입하여 사용하였고, 구조식은 Fig. 1에 나타냈다. 추출 및 UPLC 분석에서 사용한 MeOH, acetonitrile, distilled water는 특급 및 HPLC 등급으로 J.T.Baker (USA) 제품을 사용하였다. 추출은 초음파추출기(JAC-5020, KODO, Korea), 교반추출기(ISF-R, Jeio Tech, Korea), 원심분리기(Labogene, BMS, Korea)를 사용하였다. 정량분석에 사용한 UPLC는 Waters (MA, USA)를 사용하였다.
분석시료 추출
본 실험에서는 작약의 albiflorin, paeoniflorin 함량분석을 위한 추출조건을 최적화하였다. 분쇄한 시료 0.1 g에 추출용매는 MeOH로 고정하고, 20, 40, 60, 80, 99% 비율로 10 mL를 가한 후 1시간 초음파추출을 하였다. 추출방법은 이전단계에서 선택된 80% MeOH 조건으로 상온침지, 초음파추출, 교반추출하여 선정하였다. 추출시간은 30분, 1시간, 2시간 동안 추출하여 추출조건을 확립하였다.
재배지별 작약 117점의 추출은 시료 0.1 g에 80% MeOH 10 mL를 가한 후 1시간 초음파추출, 1시간 상온교반추출을 실시하였다. 추출액은 원심분리기에 10분간 원심분리하였으며, 상층액을 0.2 ㎛ membrane filter (Whatma Syringe Filter, UK)로 여과하여 분석시료로 사용하였다.
UPLC condition
Albiflorin, paeoniflorin 분석은 UPLC를 이용하여 Column은 Acquity UPLC HSS T3 (2.1 × 100 ㎜, 1.7 ㎛, Waters, Korea)를 사용하였으며, 오븐 온도는 50℃를 유지하였다. 이동상으로 solvent A는 formic acid 0.1%가 첨가된 water, solvent B는 formic acid 0.1%가 첨가된 acetonitrile을 사용하였고, 시간에 따른 용매의 조건은 다음과 같이 기울기 용리법으로 분석하였다. 0-1 min, 5% B; 1-5 min, 20% B; 5-10 min, 20% B; 10-10.5 min, 95% B; 10.5-11 min, 95% B로 설정하여 전개하였고, 모든 시료에 대한 분석은 11분간 실시하였다. 유속은 0.2 mL/min, 주입량은 2 μL였으며, 검출파장은 UV 230 ㎚에서 측정하였다.
Method validation
Albiflorin, paeoniflorin의 농도에 대한 직선적인 측정값을 확인하기 위해 직선성(Linearity)를 조사하였다. 각 표준용액을 6가지 농도로 순차적으로 희석한 후 UPLC 분석을 실시하였다. 분석한 결과에 따라 검량선을 작성하여 선형식을 계산하고 상관관계수 값을 통해 직선성을 확인하였다. 또한 분석물의 각 성분에 대한 검출 및 정량이 가능한 최저 농도를 확인하기 위한 검출한계(Limit of detection, LOD), 정량한계(Limit of quantification, LOQ)를 측정하였다. LOD와 LOQ는 각각 S/N ratio=3인 값과 S/N ratio=10인 값으로 결정하였다. 정밀성(Precision)과 정확성(Accuracy)은 표준용액을 3가지 농도로 일내, 일간 시험을 통해 평가하였다. 정밀성은 일내, 일간 시험에서 얻어진 측정값들의 상대표준편차(RSD)로 평가하였고, 정확성은 검량선에 의하여 정량한 농도의 평균값을 기지의 농도로 나눈 값의 백분율(%)로 구하였다. 회수율(Recovery)은 표준물 첨가법에 의하여 수행하였으며, 작약 추출물에 표준물질을 첨가하여 각 3회 반복 분석 후 상대표준편차를 측정하였다.
토양 특성 분석
재배지에서 채취한 시료의 토양 특성 분석은 농촌진흥청의 [종합검정실 분석 매뉴얼]을 참고하여 분석하였다(RDA, 2013). 공시토양의 토성(Soil texture)는 피펫법을 이용하여 측정된 모래, 미사, 점토의 비율로 미국농무성법 토성구분 삼각도표를 이용하여 확인하였다. 토양 pH와 전기전도도(Electrical conductivity, EC)는 풍건한 토양 10 g을 증류수 50 mL에 첨가하여 1:5로 희석하고 1시간 동안 진탕한 후 pH meter와 EC meter로 각각 측정하였다. 토양 유기물(Organic matter, OM) 함량은 Tyurin 법을 이용하여 측정하였고, 전질소(Total nitrogen, TN) 함량은 Kjeldahl 황산분해증류법으로 측정하였다. 유효인산(Available phosphate, P2O5) 함량은 Lancaster 침출법을 이용하여 1-amino-2-naphtol-4-sulfonic acid 용액에 의한 몰리브덴청법을 통해 측정하였다. 풍건한 토양 시료를 1 N NH4OAc (pH 7.0)에 침출한 후, 유도결합 플라즈마 분광광도계(Inductively coupled plasma-optical emission spectrometry, ICP-OES)를 이용하여 치환성 양이온(Exchangeable cation)을 측정하였고, 치환된 암모늄(NH4+)을 Kjeldahl 증류법으로 양이온치환용량(Cation exchange capacity, CEC)를 측정하였다.
통계분석
분석된 데이터 값은 평균 ± 표준오차(means ± standard error, S.E.) 값으로 나타냈고, 실험값의 통계분석은 SAS (Statistical Analysis System ver. 7.1) software를 이용하여 일원배치분산분석(one-way ANOVA)과 t-test 검정을 통해 유의수준 5% (p < 0.05)로 검증하였다. 작약의 albiflorin, paeoniflorin, 중량, 토양특성 데이터 간의 상관관계분석(Correlation analysis)은 IBM SPSS Statistics (version 25)를 사용하여 Pearson’s 상관관계(r)와 유의성(P < 0.05)을 확인하였다.
결과 및 고찰
분석조건 설정
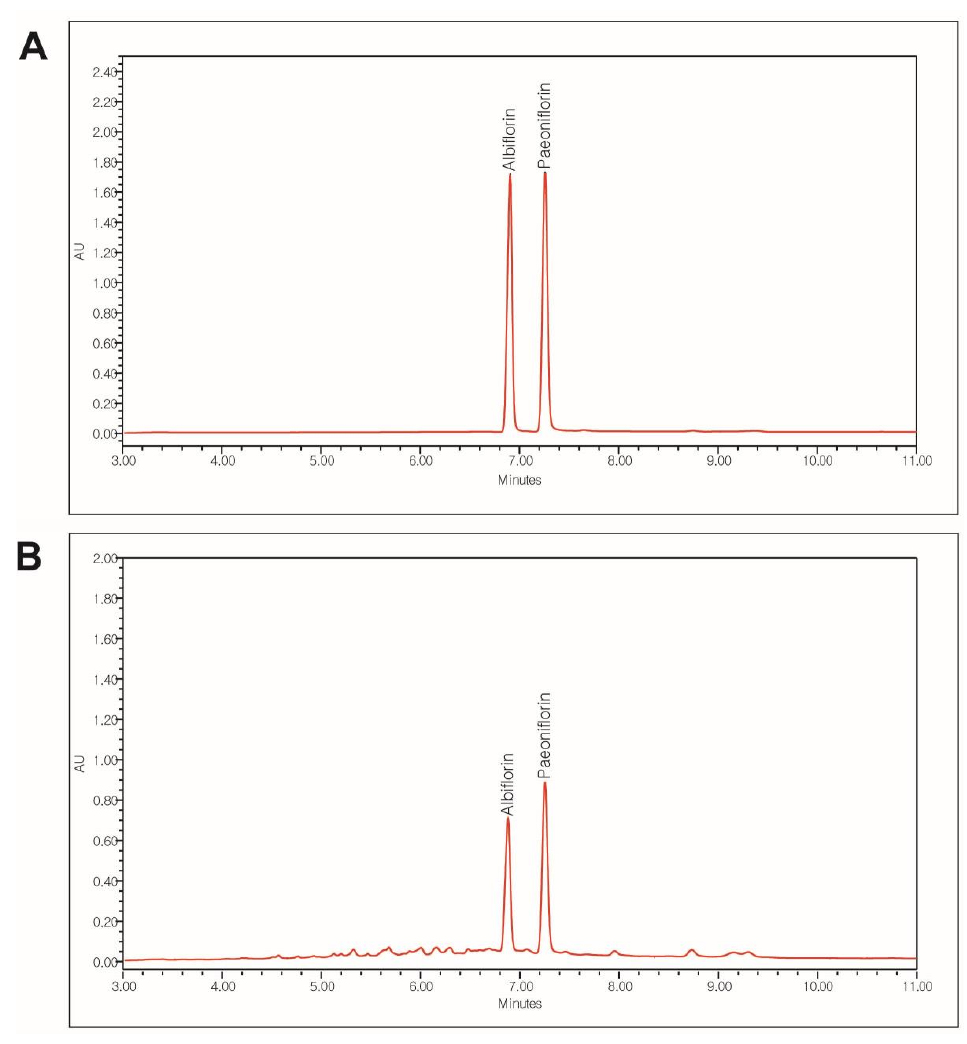
작약의 albiflorin, paeoniflorin의 UPLC를 이용한 동시분석법을 확립하였다. 총 분석시간은 11분이며, 표준품을 분석하였을 때 피크의 머무름 시간은 albiflorin 6.90분, paeoniflorin 7.25분이었다. 본 연구의 분석조건에서 표준물질의 분리능은 양호하였으며, 전처리한 작약 추출물의 크로마토그램을 비교하여 albiflorin, paeoniflorin의 피크가 분리되는지를 확인한 결과, 각 성분들이 다른 피크와 간섭 없이 분리되었으며, 표준용액의 피크유지시간과 작약 추출물의 피크유지시간 일치하는 것을 확인하였다(Fig. 2).
Method validaiton
선정된 분석법의 검증을 위하여 albiflorin, paeoniflorin의 직선성, LOD, LOQ, 정밀성, 정확성, 회수율을 조사하였다. 직선성의 농도 범위는 albiflorin, paeoniflorin 각각 5 ~ 250 ㎍ / mL로 6단계 농도의 표준용액을 분석하였고, 농도별 피크면적과 농도 간의 상관관계를 회귀분석을 통하여 결정하였다. 그 결과, 상관관계지수 r2은 0.9999 이상의 양호한 직선성을 확인하였다. 분석대상물질 albiflorin, paeoniflorin의 검출 가능한 최저 농도인 LOD는 각각 0.04, 0.01 ㎍ / mL이고, 분석대상물의 정량이 가능한 최저농도인 LOQ는 각각 0.15, 0.05 ㎍ / mL로 나타났다(Table 1). LOD와 LOQ를 계산하는데 이용되는 신호잡음비는 baseline에 대한 noise와 peak의 상대비로 그 값이 낮을수록 해당 표준물질이 주어진 조건에서 잘 검출된다(He et al., 2015). 분석법의 정밀성 평가에서는 albiflorin, paeoniflorin의 intra-day가 각각 0.66 ~ 1.37, 0.51 ~ 1.74 %, inter-day는 1.13 ~ 1.98, 0.33 ~ 4.30%의 상대표준편차(RSD)를 보였다. 정확성 평가에서는 albiflorin, paeoniflorin의 intra-day가 각각 96.01 ~ 100.97%, 97.40 ~ 100.66%, inter-day는 100.14 ~ 101.83%, 102.57 ~ 105.12%를 보였다(Table 2). 회수율은 표준품을 첨가한 검액과 대조검체로 표준물을 첨가하지 않은 검액을 분석하여 평가하였다. 그 결과, albiflorin, paeoniflorin의 회수율은 95.25 ~ 101.93%로 나타났고, 상대표준표차(RSD) 값은 1.94%이하의 값으로 나타났다(Table 3). 따라서 직선성, 검출한계, 정량한계, 정밀성, 정확성, 회수율의 method validation을 통하여 분석법에 대한 재현성과 신뢰성을 확보하였다.
Table 1.
Linear regression, LOD, LOQ of albiflorin, paeoniflorin compounds
Table 2.
Intra-, Inter-day precision and accuracy of albiflorin, paeoniflorin compounds
Table 3.
Recoveries of albiflorin, paeoniflorin compounds
| Compound |
Spiked concentration (㎍/mL) |
Recoveryz (%) (n=3) |
RSD (%) |
| Albiflorin | 12.5 | 95.25 | 1.94 |
| 50 | 101.93 | 0.30 | |
| 200 | 101.87 | 1.40 | |
| Paeoniflorin | 12.5 | 99.02 | 0.59 |
| 50 | 98.87 | 0.26 | |
| 200 | 101.34 | 0.43 |
Albiflorin, Paeoniflorin 함량
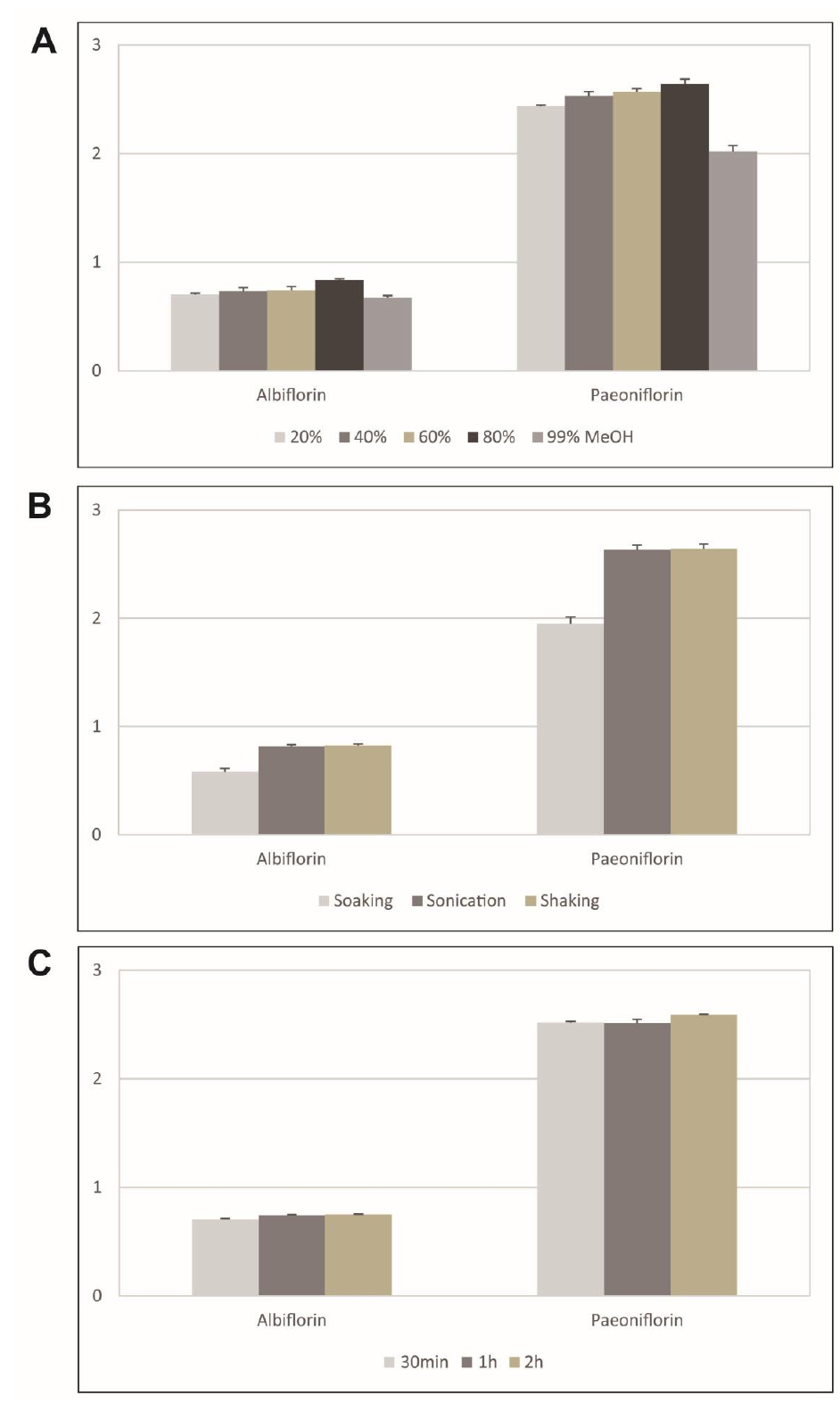
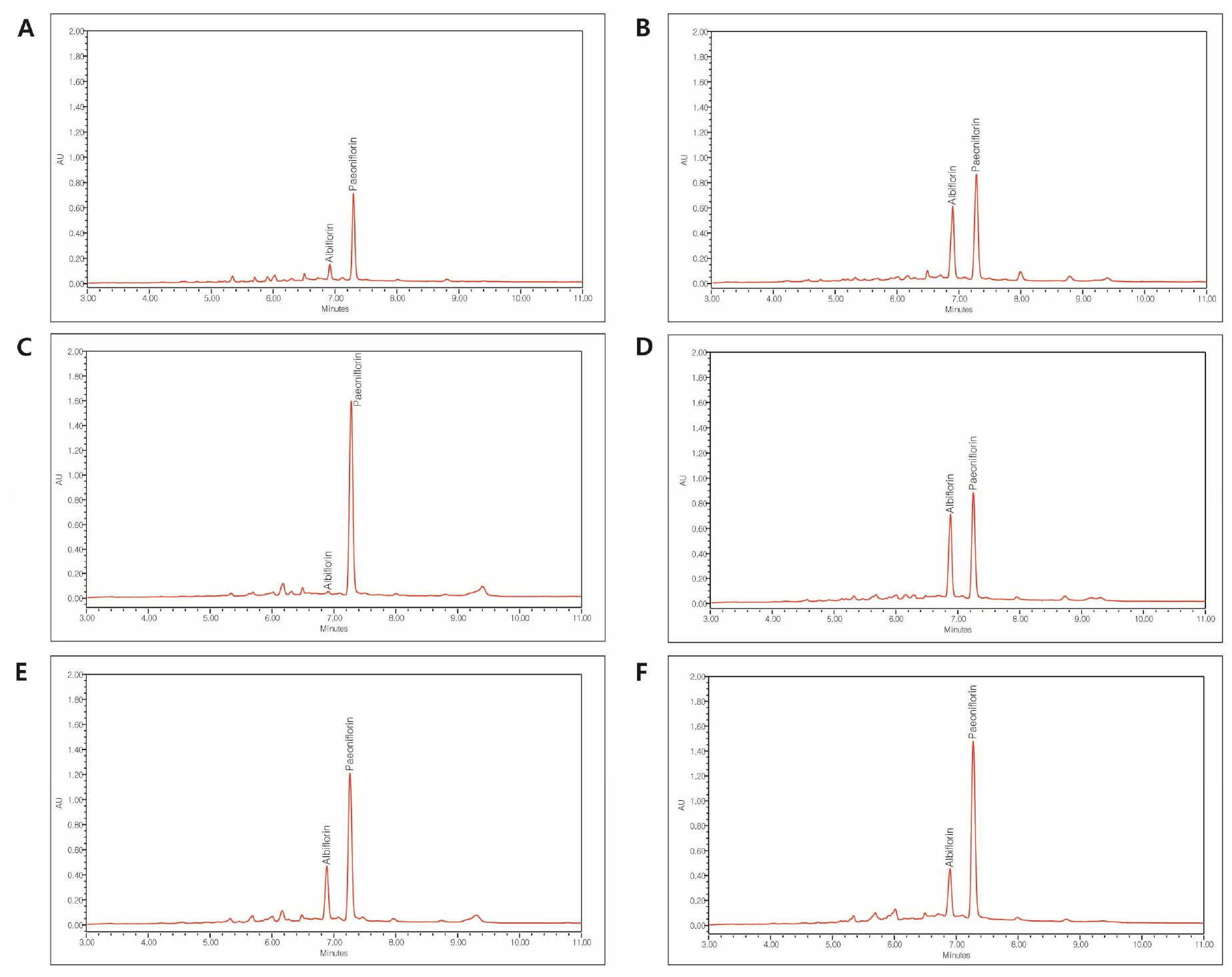
작약의 albiflorin, paeoniflorin을 추출조건을 확립하기 위해 MeOH 용매 비율별로 추출한 결과, 80%에서 두 화합물의 조성이 높게 확인되었다. 또한 추출방법은 초음파추출과 교반추출에서 두 화합물의 합이 각각 3.45 ± 0.06%, 3.46 ± 0.09%로 침지추출 2.53 ± 0.06% 보다 높게 확인되었으며, 추출시간은 2시간 조건에서 30분, 1시간 보다 두 화합물의 양이 높게 확인되었다(Fig. 3). 따라서 재배지별 함량분석을 위한 추출조건은 추출용매 80% MeOH로 1시간 초음파추출, 1시간 교반추출 조건을 선정하여 albiflorin, paeoniflorin 함량분석을 수행하였다.
재배지별 작약의 albiflorin, paeoniflorin의 함량을 분석하여 Table 4에 제시하였다. 분석 결과는 각 성분의 peak 면적을 calibration curve의 식을 이용하여 농도로 환산하였으며, 최종적으로 %단위로 나타내었다. 분석한 모든 시료에서 albiflorin, paeoniflorin이 확인되었으며, albiflorin는 0.04 ± 0.00 ~ 2.79 ± 0.21%로 범위로, JN12, CN12, JN11, GB2, CN2 순으로 함량이 높았으며, paeoniflorin는 1.98 ± 0.14 ~ 6.67 ± 0.84%로 확인되었으며, CB3, GB3, GB4, CN1 순으로 확인되었다(Fig. 4). 작약의 주산지인 의성, 거창 및 영천지역에서 수집한 paeoniflorin 함량 차이 연구에서 2.15% ~ 4.08%로 지역별 함량 차이를 보고한 바 있다(Kim et al., 1996). 이러한 차이는 재배지 기상환경 및 토양특성에 따라 재배지별 차이를 보이는 것으로 판단된다. 또한, 두 성분의 총 함량은 2.35 ± 0.06 ~ 8.41 ± 0.71%로 CB3, CN1, GB3, JN12, GB5 순으로 확인되어 지역별 정량적인 함량 차이를 확인하였다. 대한약전에서 작약의 함량 기준을 albiflorin, paeoniflorin의 총 합이 2.3% 이상을 기준으로 제시하였으며, 본 연구에서 분석한 39개 재배지역의 작약은 대한약전의 품질규격에 적합한 시료로 확인되었다. 본 연구에서 전국 재배지 작약에 대한 albiflorin, paeoniflorin 함량 자료는 품질관리를 위한 객관적이고 과학적인 근거자료 될 것으로 판단되며, 산업화 원료소재를 위한 유통에 기초자료로 활용될 것으로 사료된다.
Table 4.
Comparison of albiflorin, paeoniflorin contents and root dry weight of Paeonia lactiflora in 39 different cultivation regions
재배지별 작약의 중량
전국 39개소 재배지에서 수집한 작약의 개체별 중량을 조사한 결과, 0.06 ± 0.02 ~ 1.27 ± 0.28 ㎏으로 확인되었으며, CB1, JN1, GN1, JB3, JB4 순으로 확인되었다(Table 4). 최근 기후변화로 인하여 심한 가뭄 및 홍수 등이 빈번히 발생하고 있어 약용식물 재배에 있어 생산량 변화가 있으며, 특히 작약의 경우 강우량에 따른 토양 수분장력 변화가 생육에 영향을 미치는 것으로 보고된 바 있다(Kim et al., 2001). 또한, 관수가 작약의 생육과 수량에 미치는 영향에 관한 연구에 따르면 생육초기에 관수가 2,045 ㎏/10a로 자연 강우의 1,708 ㎏/10a, 대조구 1,776 ㎏/10a에 비교하여 각각 20, 15% 이상 생산량 향상되는 것으로 알려진 바 있다(Kim and Kim, 2001). 따라서 본 연구에서 수집된 작약의 개체별 중량 차이는 재배의 기상환경과 관수로 인한 토양 수분장력 변화에 따른 것으로 판단된다.
토양특성
재배지별 작약의 토양특성을 분석한 결과, 재배지 모두 토성은 사양토이고, pH는 4.01 ~ 6.76으로 확인되었다(Table 5). 전기전도도는 0.05 ~ 0.31 dS/m, 유기물 함량은 1.21 ~ 6.30%, 질소전량은 0.09 ~ 0.51%, 유효인산은 58.51 ~ 2414.45 mg/㎏, 치환성 칼륨 0.11 ~ 0.94 cmol+/㎏, 치환성 칼슘 1.67 ~ 12.20 cmol+/㎏, 치환성 마그네슘 0.41 ~ 3.58 cmol+/㎏, 치환성 나트륨 0.02 ~ 0.17 cmol+/㎏으로 나타났고, 양이온치환용량은 7.83 ~ 19.26 cmol+/㎏으로 나타났다. 기존의 작약 재배지의 토양이화학성 연구에 따르면, pH 5.5 ~ 7.6, 전기전도도는 0.35 ~ 0.42 dS/m, 유기물 함량은 28.9 ~ 45.1 g/㎏, 유효인산은 258 ~ 368 ㎎/㎏, 치환성 칼륨 0.87 ~ 1.17 cmol+/㎏, 치환성 칼슘 4.15 ~ 10.97 cmol+/㎏, 치환성 마그네슘 1.17 ~ 3.51 cmol+/㎏으로 보고된 바 있다(Park et al., 2011). 이와 같은 자료를 바탕으로 본 연구에서 수집한 작약 재배지의 토양특성은 기존의 연구결과와 유사한 것으로 확인되었다.
Table 5.
Soil properties of P. lactiflora in 39 different cultivation regions
작약 토양특성과 중량, 지표성분 간의 상관관계
Pearson’s 상관관계 분석을 통해 재배지 토양특성과 작약 뿌리 중량 간의 상관관계를 분석한 결과(Table 6), 작약 뿌리 중량은 유효인산, 전기전도도, 치환성 나트륨이 유의적인 정의 상관관계를 보이는 것을 확인하였다. 우리나라 전국 밭토양의 평균 전기전도도는 0.75 dS/m이고, 산림토양의 전기전도도는 0.22 ~ 0.50 dS/m으로 보고되고 있다(Kim et al., 2019b; Sung et al., 2013). 본 연구에서 사용된 작약 재배지 토양의 전기전도도는 가장 높은 재배지가 0.31 dS/m로 우리나라 밭토양과 산림토양의 평균보다 낮은 것으로 확인되었으며, Kim et al. (2019a)는 미국 농무부(United States Department of Agriculture, USDA)가 제시한 염분 토양의 기준에서 비염류토양(Non-saline soil)의 전기전도도가 2.0 dS/m 이하로 보고 한 바 있다. 따라서 본 연구에서 유의적인 상관관계를 보인 전기전도도와 치환성 나트륨은 작약의 생육에는 큰 영향을 주지 않는 것으로 판단된다. 유효인산은 식물의 세포구성 물질로 뿌리, 잎, 꽃과 과실의 발달에 관여하고, 식물이 성장하는데 중간 대사물질과 에너지 대사에 중요한 역할을 한다(Lim, 2005). Lee et al. (2010)은 약용식물인 도라지의 품질은 토양의 무기태질소와 인산 함량의 차이가 뿌리의 무게와 약효성분 등에 영향을 줄 것이라고 보고하였다. 이와 같은 선행연구는 본 연구에서 작약 뿌리의 중량과 토양 유효인산 간의 유의적인 정의 상관관계 연구결과를 뒷받침한다.
Table 6.
Pearson’s correlation coefficient between soil chemical properties and root dry weight of P. lactiflora
작약의 중량과 지표성분 함량 간의 상관관계를 분석한 결과(Table 7), 작약의 albiflorin, paeoniflorin은 중량과 유의적인 부의 상관관계를 가지는 것으로 확인되었다. 대표적인 약용식물인 산양삼 및 인삼의 경우 생육특성과 진세노사이드 함량 간의 상관관계 연구에서 뿌리의 직경과 진세노사이드 함량 간의 부의 상관관계를 보인다고 보고한 바 있다(Han et al., 2013; Kim et al., 2020; Li et al., 2009). 또한 Park et al. (2020)은 참당귀의 생육특성과 지표성분 간의 상관관계 분석결과, 식물체 뿌리 중량이 nodakenin, decursin, decursinol angelate 부의 상관관계가 있다고 보고한 바 있어, 본 연구와 유사한 결과를 확인하였다. 약용식물의 식물체 중량과 지표성분 함량은 한약재 유통에 있어 중요한 인자로 이들에 대한 상호연관성을 구명하는 연구가 추가적으로 필요하다고 판단된다.
Table 7.
Pearson’s correlation coefficient between marker compounds and root dry weight of P. lactiflora
| Correlation coefficient (r)z | ||
| Albiflorin | Paeoniflorin | |
|
Root dry weight |
-0.218* (0.018) |
-0.190* (0.040) |
상기 결과를 종합하면 작약의 재배지 토양의 유효인산은 작약의 중량과 유의적인 정의 상관관계를 보였으며, 이러한 중량은 이차대사산물인 albiflorin, paeoniflorin 함량과 유의적인 음의 상관관계를 확인하였다. 따라서 작약 재배에 있어 지표성분인 albiflorin, paeoniflorin 함량과 생산량을 동시에 증가시키는 적정 시비법 등의 재배법 개발이 필요하다고 판단된다.
적 요
본 연구는 작약의 재배지별 토양특성과 albiflorin, paeoniflorin 함량 간의 상관관계를 구명하기 위하여 수행되었다. UPLC를 사용하여 직선성, LOD, LOQ, 정밀성, 정확성, 회수율을 평가하여 분석법을 검증하였다. 작약의 albiflorin 함량은 0.04 ± 0.00 ~ 2.79 ± 0.21%, paeoniflorin은 1.98 ± 0.14 ~ 6.67 ± 0.84%로 확인되었다. 또한 작약의 개체별 뿌리 중량을 조사한 결과, 0.06 ± 0.02 ~ 1.27 ± 0.28 ㎏로 지역별 차이를 확인하였다. 작약 재배지의 토양특성은 pH, 전기전도도, 유기물 함량, 질소전량, 유효인산, 치환성 칼륨, 치환성 칼슘, 치환성 마그네슘, 치환성 나트륨, 양이온치환용량 등을 분석하였다. 재배지 토양특성과 작약 뿌리 중량 간의 상관관계를 분석한 결과, 토양의 유효인산과 작약 뿌리 중량 간의 유의적인 정의 상관관계를 확인하였다. 또한 작약 뿌리 중량과 지표성분 함량 간의 상관관계를 분석한 결과, 작약 뿌리 중량은 지표성분인 albiflorin, paeoniflorin의 함량과 유의적인 부의 상관관계를 보이는 것을 확인하였다. 따라서 작약 재배에 있어 지표성분과 생산량을 동시에 증가시키는 재배법 개발에 유용한 정보를 제공할 것으로 판단된다.