서언
재료 및 방법
시료 추출 및 제조
시약 및 기기
추출 및 분획
n-BuOH 분획으로부터 화합물의 분리
MeOH 추출물 LC-MS분석
세포배양
세포독성
H2O2에 의한 세포의 손상으로부터 심장세포보호 효과 측정
유세포분석기(Flow cytometry)를 이용한 H2O2에 유도된 심장 세포내 활성산소종 감소 효과 측정
결과 및 고찰
화합물 분리 및 구조 분석
제주모시풀 MeOH LC-MS 분석
화합물 1과 2의 H9c2세포에서의 세포생존율에 미치는 영향
화합물 1과 2의 H9c2 cells에서 H2O2로 유도된 독성 보호효과
화합물 1과 2의 H9c2세포에서 H2O2로 유도된 세포내 활성산소종(ROS)에 대한 영향
적요
서언
우리나라에는 모시풀속(Boehmeria) 식물 9종이 자생하고 있으며, 주로 잎의 형태와 크기, 지역에 따라 왕모시풀, 섬모시풀, 긴잎모시풀 등으로 분류하고 있다(An, 2011; Lee, 2006). 예로부터 모시풀은 섬유자원으로 이용되어 왔으며, 고려시대부터 재배하기 시작하여 1960년대 말까지 재배량이 증가하였다. 한방에서는 모시풀의 뿌리를 저마근(苧麻根)이라 하여 양혈지혈(凉血止血), 혈열안태(血熱安胎), 청열이뇨(淸熱利尿), 해독(解毒)작용으로 사용하고 있다(Kim et al., 2006). 최근 모시풀속의 모시풀로부터 분리된 fatty acid는 항진균 활성 효과(Xu et al., 2011)를, 왕모시풀에서 분리된 alkaloid는 위암 활성효과(Cai et al., 2006)를 나타내었다. 이와 같이 모시풀속에 식물에 대한 활성성분 연구가 진행되었으나, 제주모시풀(Boehmeria quelpaertense)에 대한 활성 성분 연구가 이루어지지 않는 실정이다. 제주모시풀은 쐐기풀과의 다년초로서 우리나라 제주도에 분포하고 있다. 높이는 1 m 자라며 왕모시풀에 비해 잎 뒷면이 짧고 털이 있고 엽병 또한 털이 있는 것이 특징이다(An, 2011).
고혈압, 동맥경화, 심근경색 등과 같은 심혈관계 질환은 심장의 지속적인 손상을 일으키게 되며 현대사회의 스트레스나 식생활에 의해 발병률이 증가되고 있다(You et al., 2004). 이러한 심혈관계 질환은 지속적인 조직 손상을 야기하여 활성산소종(reactive oxygen species, ROS)을 급격하게 증가시키게 된다(Devasagayam et al., 2004). 또한, 증가된 활성산소종은 또한 세포손상을 유도하게 되어 악순환이 반복되게 된다. 최근에는 천연물이나 천연성분을 이용하여 활성산소의 발생을 예방 하려는 연구가 시도되고 있다(Cho et al., 2005; Kim et al., 2014; Sun et al., 2011).
이에 본 논문에서는 제주모시풀 전초를 methanol로 추출하여 극성 별 용매 분획 후 얻은 BuOH 분획에서 각종 column chromatography법을 이용하여 2종의 flavonoid를 분리하였고, 1H-, 13C-NMR, LC ESI IT-TOF MS를 통해 화학 구조를 동정하였다. 분리한 2종의 화합물은 이 식물로부터 처음 분리되었고, 분리된 화합물에 대한 심근세포에서 항산화 및 세포보호효과 활성을 측정하여 심혈관계 질환 예방 기능성 소재로써 가능성을 확인하고자 하였다.
재료 및 방법
시료 추출 및 제조
본 연구에 사용한 제주모시풀은 쐐기풀과(Urticaceae)에 속하는 Boehmeria quelpaertense로서 목포대학교 한약자원학과 김휘 교수님의 식물학적 동정을 거쳤으며, 실험에 시용한 시료의 확증표본(TKM-2049)은 한약진흥재단 한약재연구팀에 보관하고 있다.
시약 및 기기
Column chromatography의 고정상으로 RP-C18 silica gel (50 ㎛, YMC)을 사용하였다. RP TLC로는 Merck RP-C18 F254s plates를 사용하였다. 성분 분리를 위해 Prep-HPLC는 Agilent A1200 series (Agilent, U.S.A) 장비를 이용하였고, 사용된 컬럼은 Luna 5 μ C18(2) 100A column (250 × 30.00 ㎜, Phenomenex)이다. 구조 동정에 사용된 NMR (Nuclear magnetic resonance) spectrum은 Varian 500 spectrometer (1H: 500 MHz, 13C: 125 MHz)으로 측정하였고, NMR 용매는 DMSO-d6, CD3OD (Sigma, USA)를 사용하였다. 세포 배양액인 Dulbacco’s modified Egles medium (DMEM)과 Fetal bovine serum (FBS), Streptomycin의 세포 배양 시약들은 Gibco (USA)에서 구입하여 사용하였고, 3-(4,5- dimethylthiazol-2-yl)-5-(3-carboxymethoxyphenyl)-2-(4-sulfophenyl)-2H-tetrazolium (MTS, CellTiter 96A Queous One Solution Cell Proliferation Assay)는 Promega (USA)에서, H2O2, 2'7'-Dichlorofluorescindiacetate (DCFH-DA)는 Sigma (USA)에서 구입하여 사용하였다.
추출 및 분획
신선한 제주모시풀(2.5 kg)를 100% MeOH로 3시간, 3회 추출, 농축하여 MeOH extract 273 g을 얻었다. MeOH extract (273 g)을 증류수에 하고 n-hexane, methylene chloride, ethyl acetate, n-butanol 로 극성순으로 용매 분획하여 각각 47, 5, 7, 40 g을 얻었다.
n-BuOH 분획으로부터 화합물의 분리
BuOH 분획물 40 g을 ODS gel (50 ㎛, 350 g, YMC, Japan)이 충진 된 column (8 ㎝ × 100 ㎝)에 Acetonitrile-Water (1:9 → 4:1 in 0.02% formic acid)을 용매 조건으로 하여 column chromatography를 실시하였고, 9개의 소분획(BQB1~7)을 얻었다. 그 중 BQB 4 분획물 25 g을 silica gel (70-230 mesh, Merck, Germany) 200 g이 충진 된 glass column (3 ㎝ × 70 ㎝)에 로딩시키고 EtOAc-MeOH-Water (8:2:1.5) 조건으로 진행하였고, 소분획물은 TLC를 이용하여 유사한 분획을 합친 다음 농축하여 9개의 소분획물로 나누었다(BQB4-1 ~ BQB4-9). 이중 BQB4-3을 ODS column (3 ㎝ × 25 ㎝, 5 ㎛, phenomenex, USA)이 장착된 prep-LC (Agilent, infinity 1260, USA)를 사용하여 화합물 1 (90 ㎎)과 2 (50 ㎎)를 순수하게 분리하였다.
화합물 1 (Isoquercitrin): Yellow powder; LC ESI IT-TOF MS: m/z 465 [M+H]+; 1H-NMR (500 MHz, CD3OD, δH) 7.71 (1H, brs, H-2'), 7.58 (1H, dd, J = 8.5, 2.0 Hz, H-6'), 6.86 (1H, d, J = 8.5 Hz, H-5'), 6.38 (1H, s, H-8), 6.19 (1H, s, H-6), 5.26 (1H, d, J = 8.5 Hz, H-1''), 3.72 (1H, dd, J = 12.0, 2.0 Hz, H-6''a), 3.58 (1H, dd, J = 12.0, 5.5 Hz, H-6''b); 13C-NMR (125 MHz, DMSO-d6, δC) 178.1 (C-4), 164.6 (C-7), 161.6 (C-5), 157.6 (C-2), 157.0 (C-9), 148.4 (C-4'), 144.5 (C-3'), 134.2 (C-3), 121.8 (C-1'), 121.6 (C-6'), 116.1 (C-2'), 114.6 (C-5'), 104.3 (C-10), 102.8 (C-1''), 98.5 (C-6), 93.3 (C-8), 77.0 (C-3''), 76.7 (C-5''), 74.3 (C-2''), 69.8 (C-4''), 61.1 (C-6'').
화합물 2 (Hyperoside): Yellow powder; LC ESI IT-TOF MS: m/z 465 [M+H]+; 1H-NMR (500 MHz, DMSO-d6, δH) 7.66 (1H, dd, J = 8.5, 2.0 Hz, H-6'), 7.53 (1H, d, J = 2.0 Hz, H-2'), 6.81 (1H, d, J = 8.5 Hz, H-5'), 6.39 (1H, s, H-8), 6.19 (1H, s, H-6), 5.37 (1H, d, J = 8.5 Hz, H-1''); 13C-NMR (125 MHz, DMSO-d6, δC) 177.8 (C-4), 164.9 (C-7), 161.6 (C-5), 156.7 (C-9), 156.5 (C-2), 148.8 (C-4'), 145.3 (C-3'), 133.8 (C-3), 122.3 (C-6'), 121.3 (C-1'), 116.4 (C-5'), 115.5 (C-2'), 104.1 (C-10), 102.3 (C-1''), 99.3 (C-6), 93.8 (C-8), 76.1 (C-5''), 73.4 (C-3''), 71.6 (C-2''), 68.3 (C-4''), 60.4 (C-6'').
MeOH 추출물 LC-MS분석
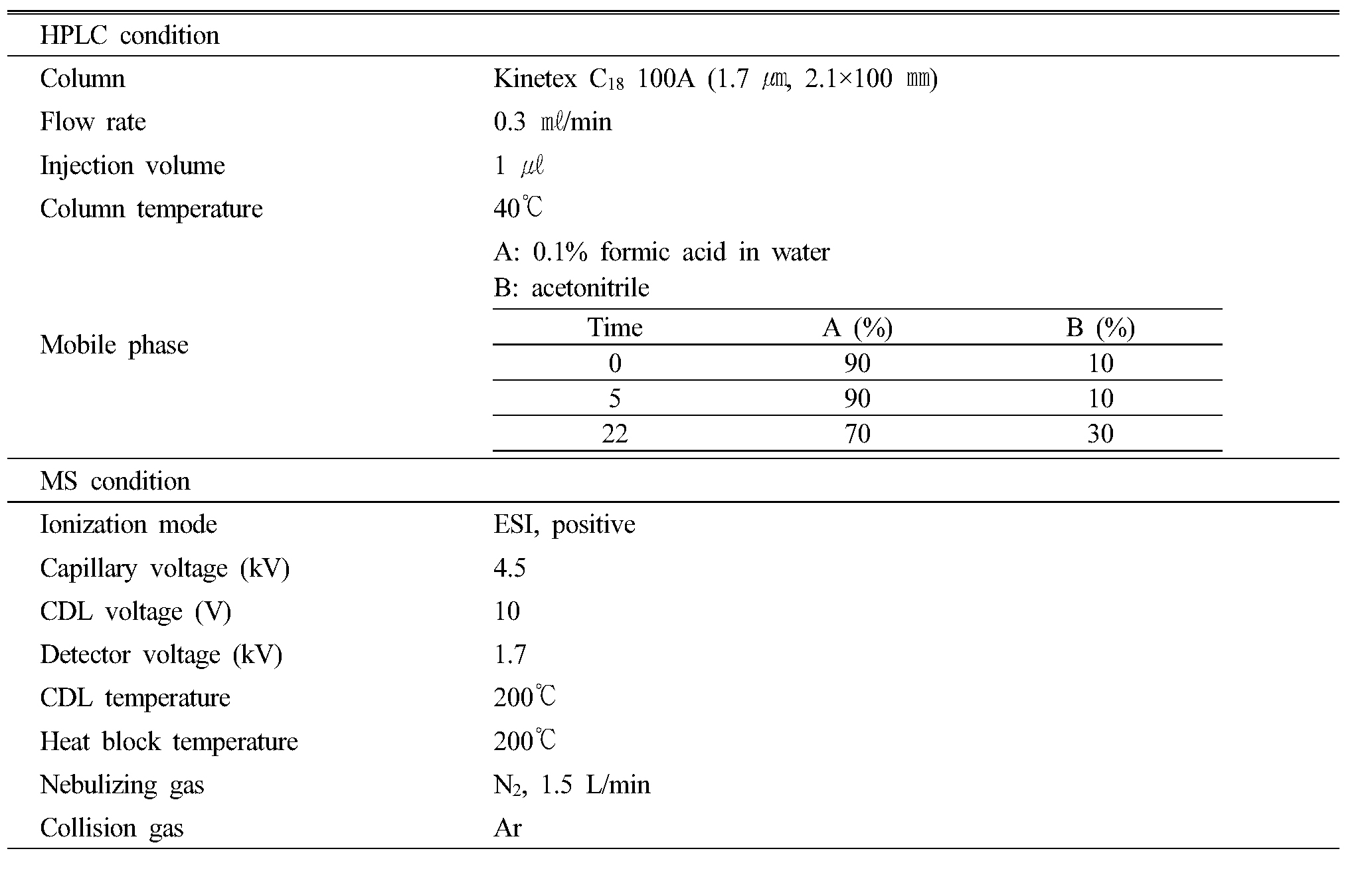
제주모시풀 MeOH 추출물을 prominence UFLC system (LC- 20AD pump, CTO-20A column oven, DGU-20A3 degasser, SPD-20A UV detector, SIL-20A XR autosampler, Shimadzu, Japan)을 사용하여 Table 1의 조건으로 측정하였고, 분리된 peak들은 ESI (electrospray ionization) interface를 통해 hybrid IT TOF mass spectrometer (Shimadzu LCMS-IT-TOF, Kyoto, Japan)로 분석하였다.
세포배양
Rat cardiomyoblast cell line인 H9c2는 한국세포주은행에서 구입하여 사용하였으며, DMEM에 10% FBS, 100 U/㎖ P/S를 혼합한 배지를 사용하여 37℃, 5% CO2 Incubator에 배양하여 사용하였다.
세포독성
96 well plate에 50,000 cells/well의 H9c2 세포를 분주하고 세포를 안정화 시켰다. 시료를 첨가하고 24시간 동안 배양한 다음 10 ㎕의 MTS (3-(4,5-dimethylthiazol-2-yl)-5-(3- carboxymethoxyphenyl)-2-(4-sulfophenyl)-2H-tetrazolium) solution을 분주한 후 CO2배양기(37℃, 5% CO2)에서 3시간 동안 배양시킨 뒤, 570 nm에서 흡광도의 변화를 측정하였다.
H2O2에 의한 세포의 손상으로부터 심장세포보호 효과 측정
세포를 96-well plates에 50,000 cells/well 분주한 뒤 세포를 안정화 시킨 다음 시료를 처리하고 30분 뒤 H2O2를 첨가하고 하루 더 배양한 후 MTS assay로 세포의 생존율을 측정하였다.
유세포분석기(Flow cytometry)를 이용한 H2O2에 유도된 심장 세포내 활성산소종 감소 효과 측정
세포를 96-well plates에 5×105 cells/well 농도로 100 ㎕씩 분주한 뒤 DCFH-DA를 세포 내에 형광 염색될 수 있게 30분 전처리한 후, H2O2와 시료를 동시에 처리하고 37℃에 3시간동안 배양하였다. 그 후 flow cytometry를 이용하여 관찰하고 histogram을 이용하여 정리하였다.
결과 및 고찰
화합물 분리 및 구조 분석
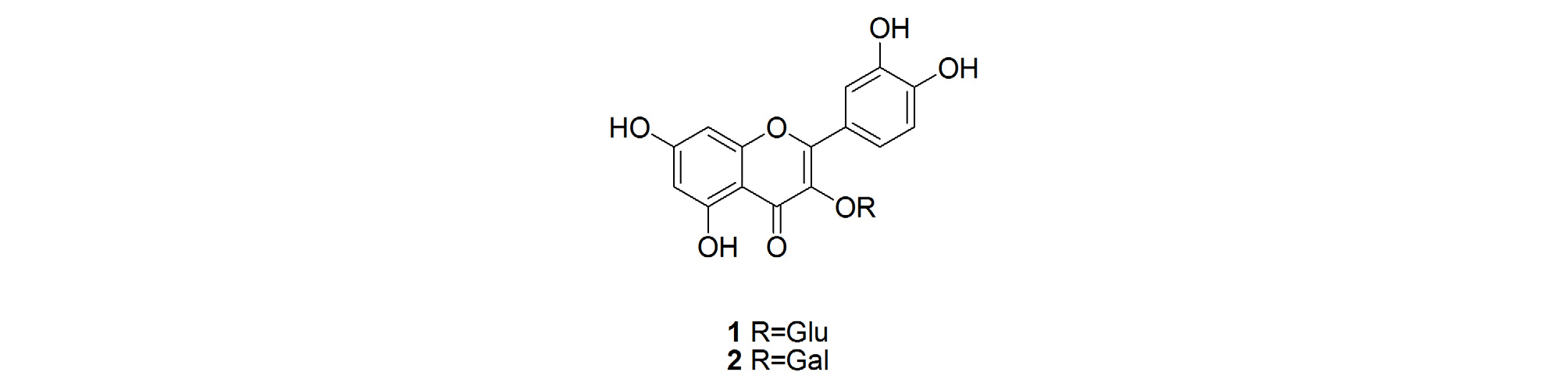
제주모시풀 전초(2.5 kg)를 100% MeOH로 추출하여 얻어진 추출물을 용매의 극성에 따라 n-hexane, methylene chloride, ethyl acetate, n-butanol, H2O로 분획하고 감압 농축하여 5개의 분획을 얻었다. 그 중 butanol 분획을 각종 column chromatography를 이용하여 2종의 화합물을 분리하였다(Fig. 1).
화합물 1 (yellow powder)은 LC ESI IT-TOF MS에서 m/z 465 [M+H]+의 분자이온 피크가 관측되어 분자량을 464로 결정하였다. 1H-NMR spectrum에서 1,3,4-trisubstitued proton δH 7.71 (1H, brs, H-2'), 7.58 (1H, dd, J = 8.5, 2.0 Hz, H-6'), 6.86 (1H, d, J = 8.5 Hz, H-5')로부터 flavonoid의 B환을, δH 6.38 (1H, s, H-8)와 6.19 (1H, s, H-6)의 signal로부터 flavonoid A환의 meta 위치에 존재하는 것을 관찰하여 quercetin 모핵을 갖는 것을 확인하였다. 13C-NMR spectrum에서 quercetin 모핵에 당 1개를 포함한 22개의 carbon peak를 확인하였다. 당의 chemical shift [δH 5.26 (1H, d, J = 8.5 Hz, H-1''); δC 102.8 (C-1''), 77.0 (C-3''), 76.7 (C-5''), 74.3 (C-2''), 69.8 (C-4''), 61.1 (C-6'')]이 관찰되었고, glycopyranose로 판명하였다. 당의 anomeric proton의 J value (8.5 Hz)를 통해 β-결합하는 것을 확인하였다. 위의 모든 결과를 종합하여 기존 문헌(Lee et al., 2014)과 비교한 결과 화합물 1을 isoquercitrin으로 동정하였다.
화합물 2 (yellow powder)은 LC ESI IT-TOF MS에서 m/z 465 [M+H]+의 분자이온 피크가 관측되어 분자량을 464로 결정하였다. 1H, 13C-NMR spectra에서 화합물 1과 유사한 양상을 나타내지만, 당의 carbon chemical shift의 차이를 나타내었다. 1H-NMR spectrum에서 당의 anomeric proton은 δH 5.37 (1H, d, J = 8.5 Hz, H-1'')에 관찰되었고, 13C-NMR spectrum에서는 δC 102.2 (C-1''), 76.2 (C-5''), 73.6 (C-3''), 71.6 (C-2''), 68.3 (C-4''), 60.5 (C-6'')가 확인되어 galactose로 결정하였다. δH 5.37에 확인되는 anomeric proton의 coupling constant 값이 8.5 Hz 로 galactose는 β-결합하는 것을 확인하였다. 위의 모든 결과를 종합하여 기존 문헌(Park et al., 2010)과 비교한 결과 화합물 2을 hyperoside로 동정하였다. 2개의 화합물은 이 식물로부터 처음으로 분리 보고되는 화합물이다.
제주모시풀 MeOH LC-MS 분석
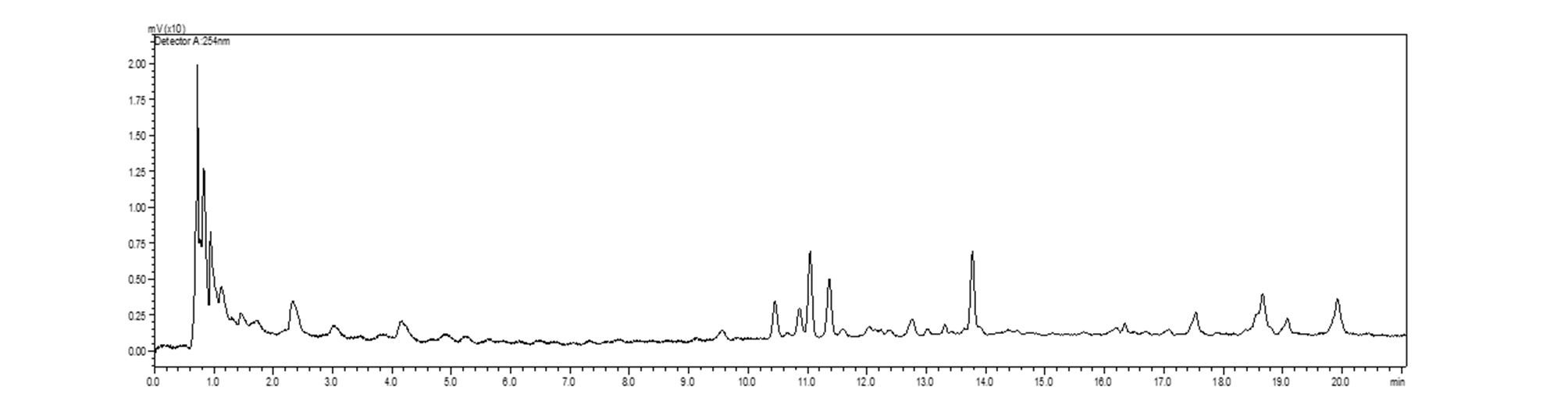
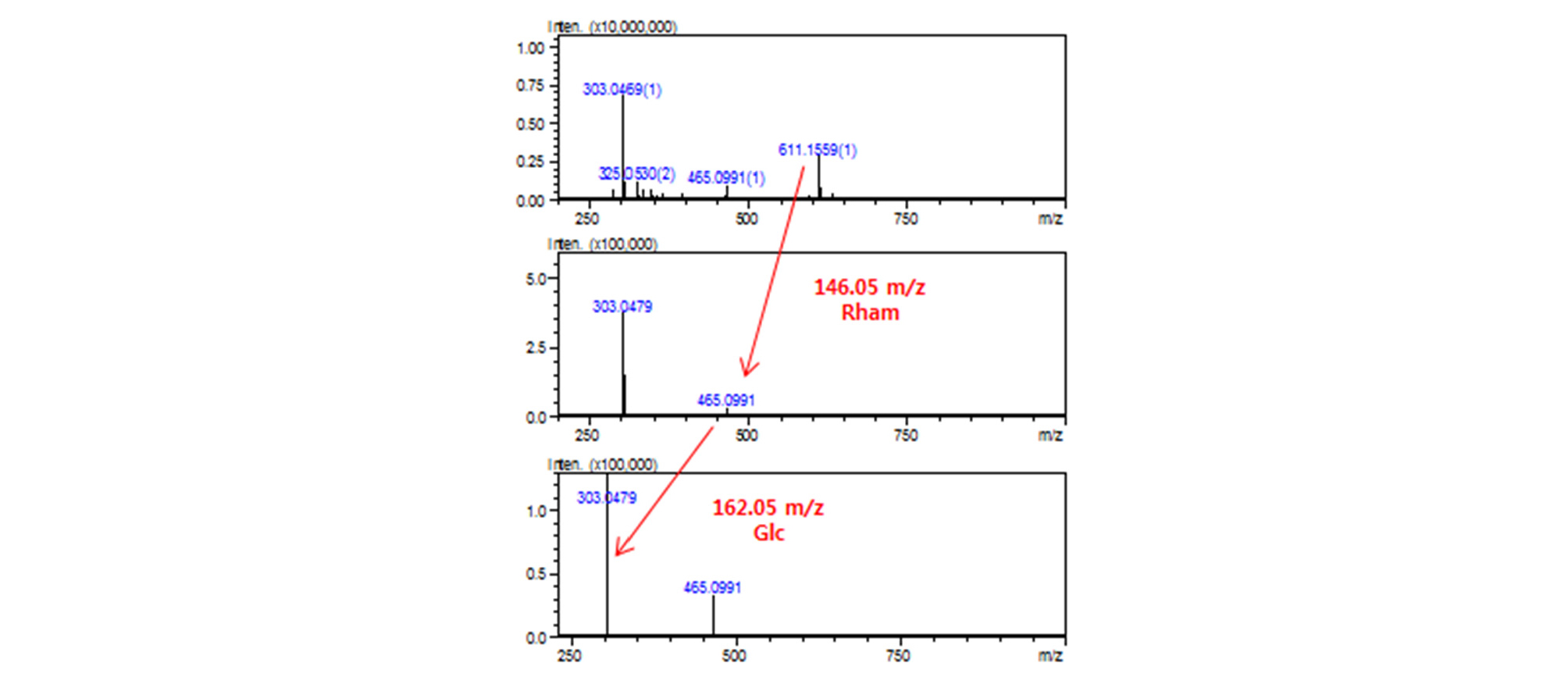
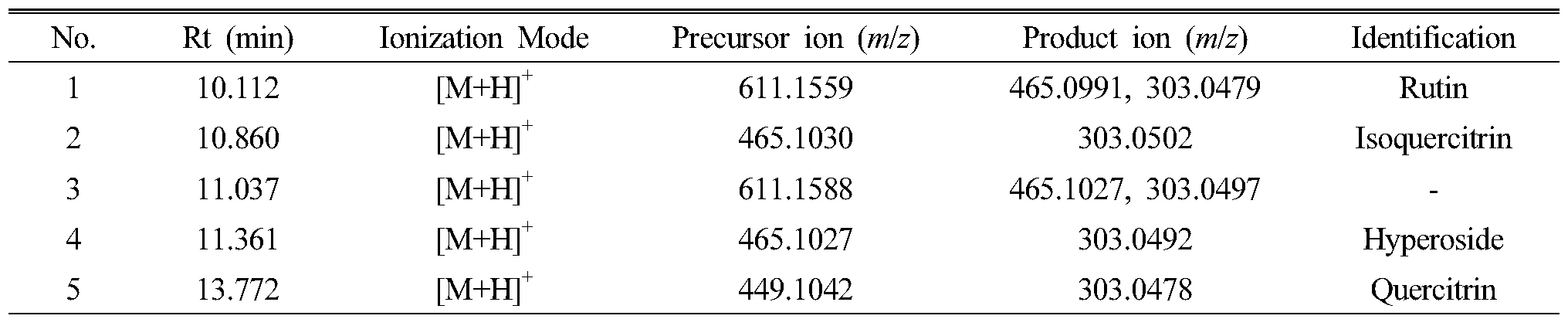
제주모시풀 MeOH 추출물 LC-MS 분석 결과 10~14분 사이에 총 5개의 major peak가 나타났고(Fig. 2), n-butanol 층에서 분리된 화합물은 각각 10.860분, 11.361분의 peak로 확인되었다. 10.112분과 11.037에 확인되는 두 peak는 m/z 611 [M+H]+의 분자량이 검출되었으며, 146 dalton, 162 dalton 차이의 fragment ion signal m/z 465, 303 [M+H]+이 관찰되었다. 이 결과로 quercetin에 glucose, rhamnose가 결합한 화합물로 예측하였고, 표준품과 비교한 결과 11.037분 peak는 rutin으로 확인되었다(Fig. 3). 또한 10.112분 peak는 rutin과 동일한 분자량 및 fragment signal이 관찰되었으나, retention time이 다른 것으로 보아 당의 결합 위치가 다를 것으로 예상하였다. 13.772분의 peak는 m/z 449 [M+H]+의 분자량이 검출되었으며, 162 dalton 차이의 fragment ion signal m/z 303 [M+H]+을 확인하였고, 표준품과 비교하여 quercitrin으로 확인하였다(Table 2).
화합물 1과 2의 H9c2세포에서의 세포생존율에 미치는 영향
화합물 1과 2의 세포독성을 나타내는 농도를 알아보기 위해 MTS 분석법을 이용하여 세포생존율을 측정하였다. MTS는 살아 있는 세포에 있는 mitochondrial NADH-dehydrogenase와 반응하여 tetrazolium salt를 환원시켜 색상을 갖은 formazan을 형성하여 살아있는 세포를 정량화 할 수 있다(Desai et al., 2006). 화합물 1 과 2를 6.25, 12.5, 25, 50, 100 μM의 농도로 처리하였을 때 심장세포(H9c2)가 농도별로 세포생존률이 감소하였으나 통계적 유의성은 없는 것으로 나타났다(Fig. 4).
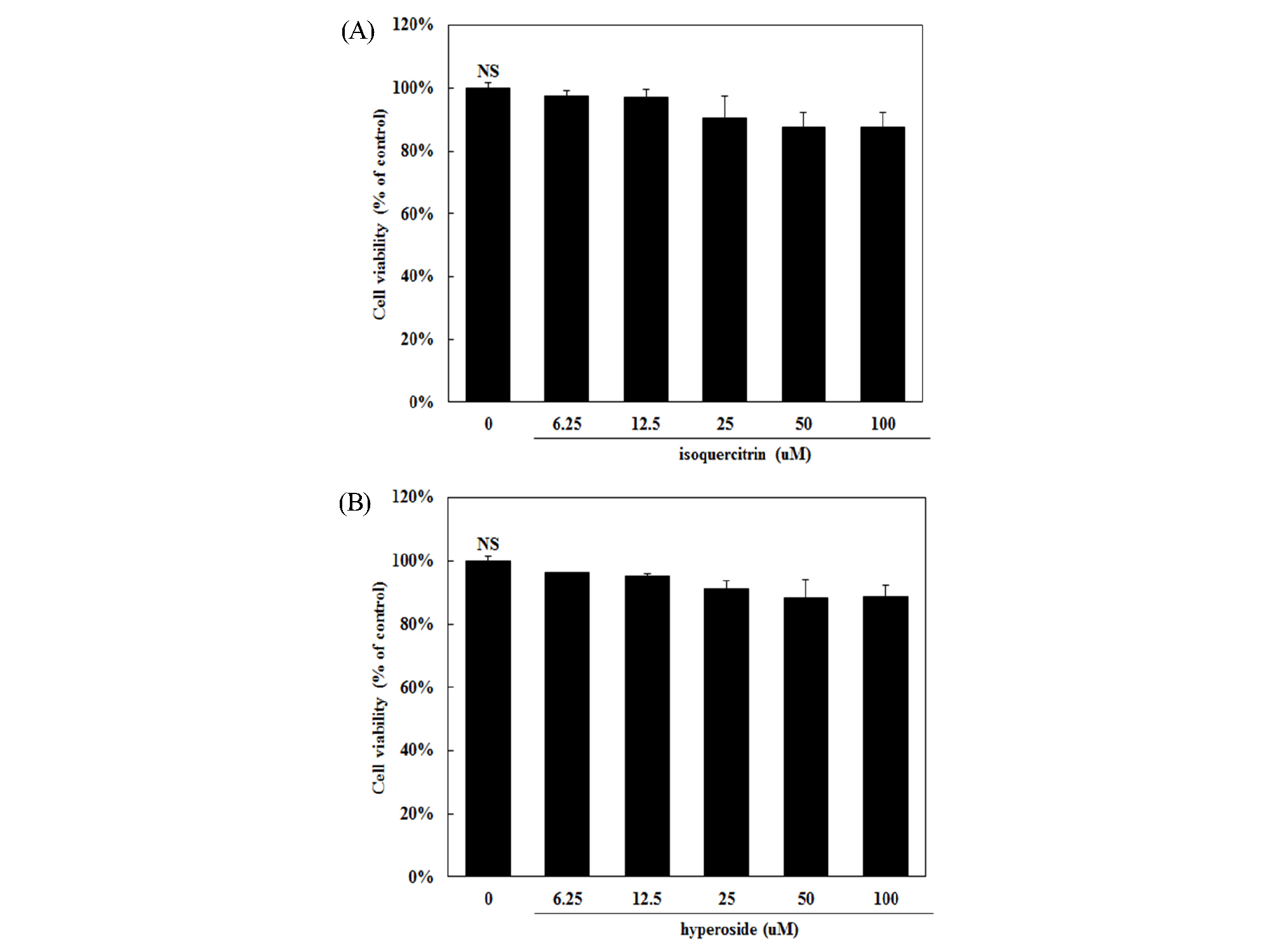
Fig. 4.
Effect of flavonoids on cell viability in H9c2 cells. Cells were incubated for 24 hrs in the presence or absence of (A) isoquercitrin (B) hyperoside indicated dose. Cell viability was evaluated by MTS assay as described in materials and methods. NS: non-significant. Significant differences between treated groups were determined using the Student’s t-test. Data represent the mean ± S.D. of triplicate determinations from three separate experiments.
화합물 1과 2의 H9c2 cells에서 H2O2로 유도된 독성 보호효과
H2O2는 산화적 스트레스를 유발시키는 대표적인 물질로서 세포에 처리하게 되면 독성이 유도된다고 알려져 있다(Desai et al., 2007). 독성보호 효과를 측정하기 위해 H9c2 cells에 화합물 1과 2를 독성이 없는 농도인 6.25, 12.5, 25 μM의 농도로 세포를 처리하고, H2O2에 의해 세포독성을 유발시켰다. H2O2에 의해 독성이 유도된 H9c2 세포는 정상군에 비하여 유의하게 세포생존율이 감소하였다. H2O2 단독처리군보다 화합물 1과 2를 처리하였을 때, 모두 농도의존적으로 유의성 있게 세포독성을 완화시키는 것을 확인할 수 있었다(Fig. 5).
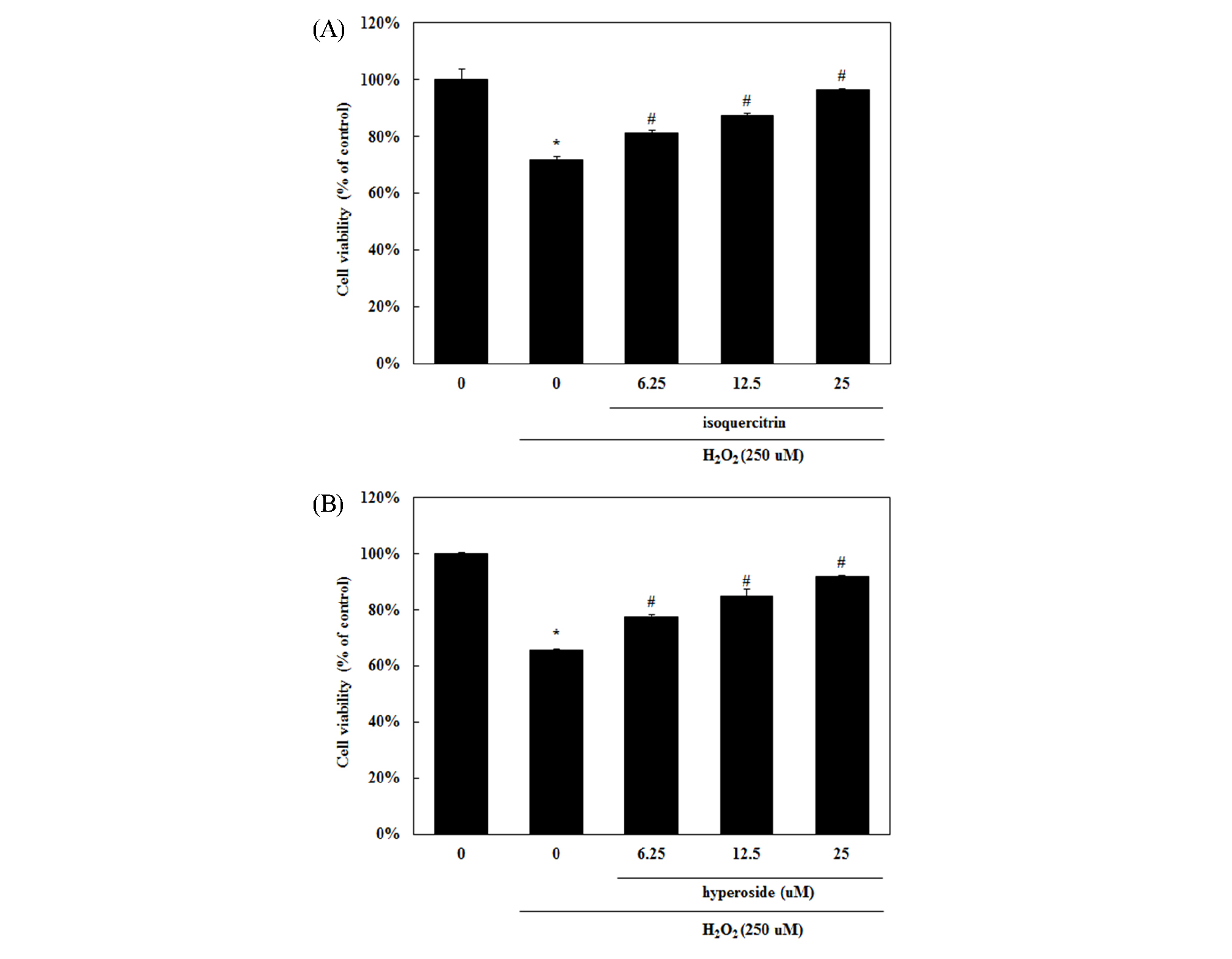
Fig. 5.
Effect of flavonoids on hydrogen dioxide (H2O2)-mediated cytotoxicity in H9c2 cells. Cells were pre-treated with the indicated concentration of (A) isoquercitrin (B) hyperoside for 1 hr before being incubated with H2O2 (250 μM) for 24 hrs. Cell viability was evaluated by MTS assay as described in materials and methods. Statistical significance: *p<0.05 **p<0.01, when compared to the normal group; #p<0.05 ##p<0.01, when compared to the H2O2 alone treated group. Significant differences between treated groups were determined using the Student’s t-test. Values shown are the mean ± S.D. of triplicate determinations from three separate experiments.
화합물 1과 2의 H9c2세포에서 H2O2로 유도된 세포내 활성산소종(ROS)에 대한 영향
H9c2에 대한 H2O2에 의해 유도된 활성산소종(ROS)을 DCFH- DA라는 활성산소가 발생된 세포를 염색하는 형광시약을 이용해 측정하였다. H2O2에 의해 유도된 H9c2는 정상군에 비하여 유의하게 ROS-positive cell이 증가하였다. 화합물 1과 2를 6.25, 12.5, 25.0 μM의 농도로 세포를 처리하였을 때, H2O2 단독처리군보다 H9c2세포에서 농도의존적으로 유의성 있게 세포내 활성산소종을 완화시키는 것을 확인할 수 있었다(Fig. 6, 7). 이는 기존에 hyperoside (2)가 인간상피세포(ECV304)의 세포내 활성산소종의 감소와 같은 비슷한 결과를 얻을 수 있었다(Li et al., 2008). 하지만 isoquercitrin (1)은 인간 소장세포에서 세포내 활성산소종의 감소하지 않았지만(Yokomizo et al., 2006), 여러 연구들을 통해 isoquercitrin이 ABTS와 DPPH 라디칼 소거능이 등 항산화 능력이 뛰어난 것으로 알려져 있다(Shibano et al., 2008; Regasini et al., 2008; Masuoka et al., 2006). 본 실험에서도 심장세포에서 세포내 활성 산소종을 감소시켜 항산화 효과가 뛰어난 것을 확인하였다.
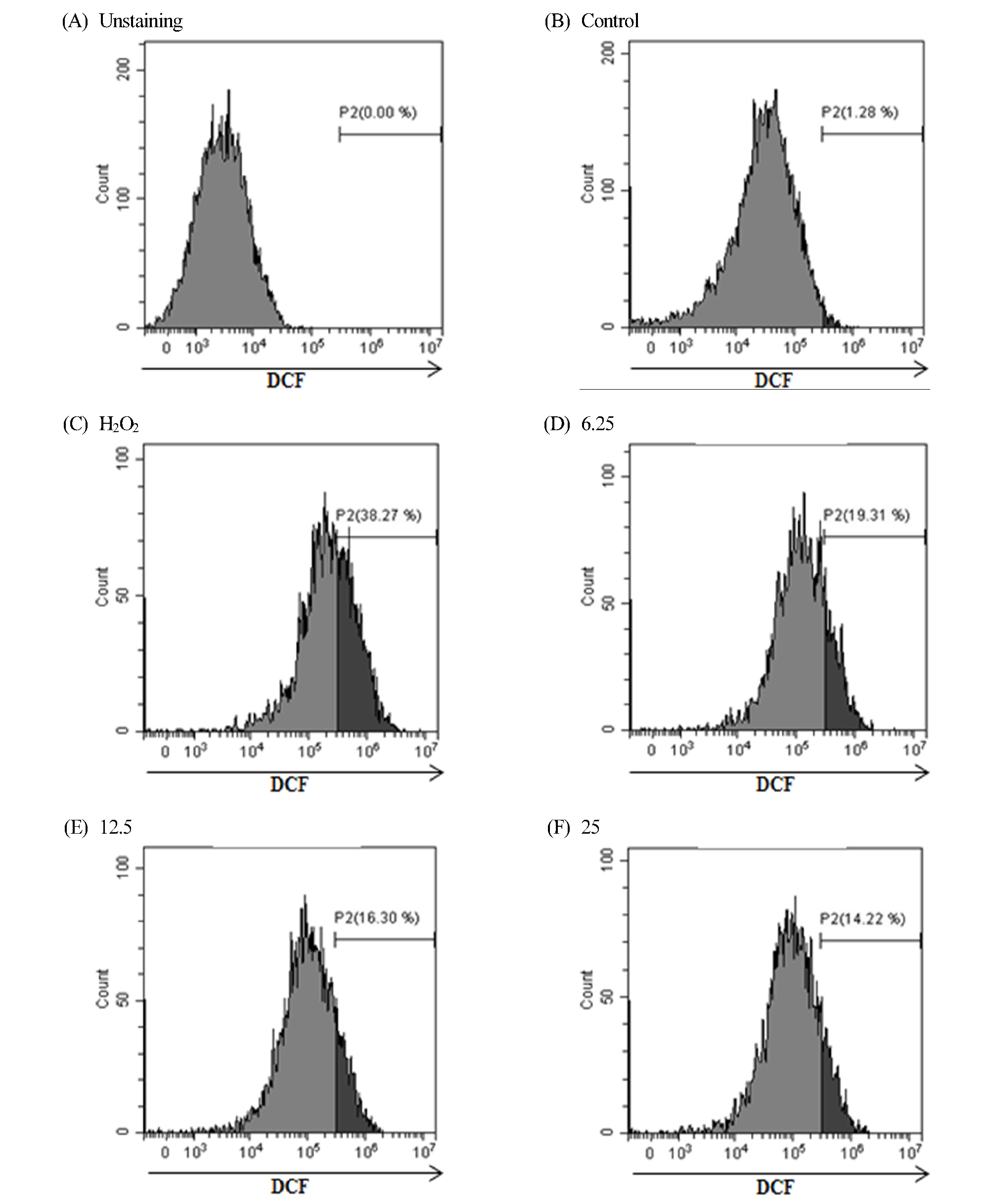
Fig. 6.
Effect of isoquercitrin on hydrogen dioxide (H2O2)-mediated ROS induction in H9c2 cells. H9c2 were pre-treated with DCFH-DA for 30 min, followed by the indicated concentration of isoquercitrin and 1 mM of H2O2 treatment for 3 hrs incubation. Levels of intracellular ROS were measured by flow cytometry. (A) Unstaining, (B) Control, (C) H2O2-treated cells, isoquercitrin (D) 6.25 μM and H2O2-treated cells (E) 12.5 μM and H2O2-treated cells (F) 25 μM and H2O2-treated cells.
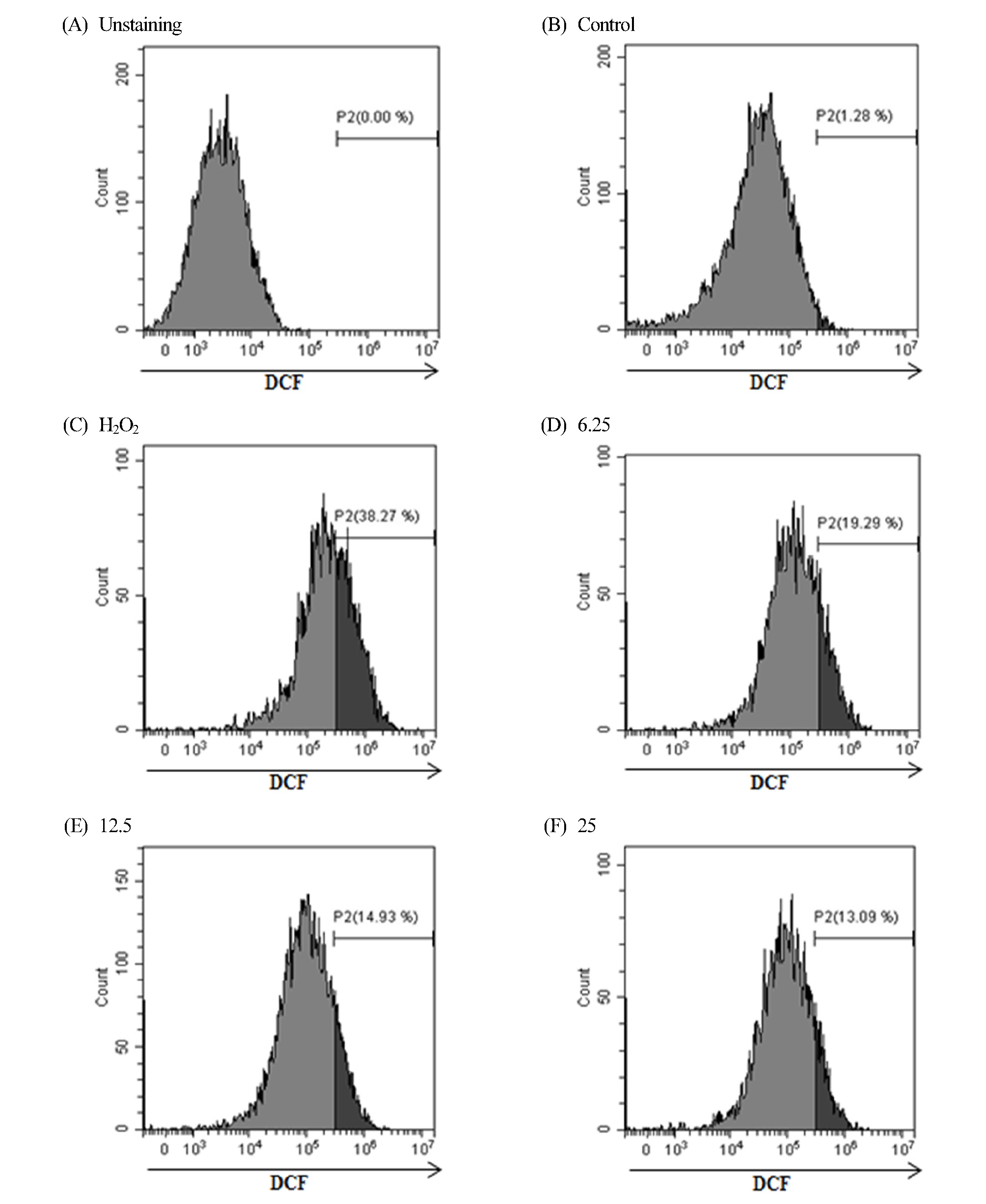
Fig. 7.
Effect of hyperoside on hydrogen dioxide (H2O2)-mediated ROS induction in H9c2 cells. H9c2 were pre-treated with DCFH-DA for 30 min, followed by the indicated concentration of hyperoside and 1 mM of H2O2 treatment for 3 hrs incubation. Levels of intracellular ROS were measured by flow cytometry. (A) Unstaining, (B) Control, (C) H2O2-treated cells, hyperoside (D) 6.25 μM and H2O2-treated cells (E) 12.5 μM and H2O2-treated cells (F) 25 μM and H2O2-treated cell.