서 언
재료 및 방법
식물재료
기내 배양 및 식물체 재분화
DNA 추출 및 ISSR 분석
Data 분석
결과 및 고찰
기내배양에 의한 식물체 재생
재분화 녹색 식물체의 DNA 밴드 양상
유전적 유사도 지수
군집분석
적 요
서 언
지구온난화에 따라 농업부문 신재생에너지의 중요성이 증대되고 있다. 홍띠(Imperata cylindrica ‘Rubra’)는 벼과 띠속의 다년생 식물로서 원산지는 북아메리카, 아시아, 아프리카의 온대 및 열대 지방이며(Lee, 2003; http://www.missouribotanicalgarden.org/PlantFinder), 띠(Imperata cylindrica L.)의 한 부류로서 잎의 상단부가 붉은색을 띤 관상 가치가 있는 조경용 자원식물이다. 홍띠가 속하는 화본과 식물은 바이오에너지 식물자원으로 중요한 소재이며(Goh et al., 2011; Moon et al., 2016; Yoo et al., 2012; Yu et al., 2015), 지구온난화 시대에 있어 조경소재, 피복작물 등 다양한 식물자원 소재로 그 이용 가치가 높다(Hwang et al., 2018; Kim et al., 2005; Moon et al., 2016; 2019).
기내 재분화를 통한 바이오에너지 식물자원의 효율적인 대량번식체계 구축을 위한 화본과 식물의 기내재생에 관한 연구로 다양한 식물종 및 식물체 부위, 생장조절제의 영향 등에 관한 연구(Cho and Byeon, 2011; Kim et al., 2005; Kusano et al., 2003; Umami et al., 2012; Yu et al., 2015)가 수행되었다. 치상 부위로는 종자 부위(Cho and Byeon, 2011; Goh et al., 2011; Kim et al., 2005; Kusano et al., 2003), 미성숙 화기(Yu et al., 2015), 미숙 화서 부위(Akashi and Ikeda, 1989), 생장점(Umami et al., 2012) 등이 이용되고 있다. 또한, 띠(cogongrass)에서는 기내배양에 대한 연구(Akashi and Ikeda, 1989; Umami et al., 2012; Shigeki et al., 2009)가 보고되고 있으나 홍띠에서는 거의 찾아보기 힘든 실정이다. 안정적인 기내 식물체 대량증식을 위해서는 치상할 식물체의 적정 부위, 생장조절물질 종류 및 농도 등 다경 줄기(multiple shoot) 유도 조건 구명과 재분화 식물체의 순화체계 구축 외에도 재분화 식물체의 유전적 변이성에 대한 검토가 중요한 요소이다.
기내 재생 재분화 식물체의 유전적 변이(somaclonal variation)에 대한 분석에는 RAPD, SSR, AFLP, ISSR 등 다양한 분자 마커들이 이용되고 있다(Amin et al., 2018; Coronel et al., 2018; Fatiha et al., 2019; Jin et al., 2008; Mo et al., 2009; Ramakrishnan et al., 2014; Ryu et al., 2011; Ryu et al., 2013). ISSR 마커는 4~10회 반복된 염기서열을 바탕으로 특정 프라이머에 의해 식물체 genome 상의 반복된 염기서열로, 이러한 반복서열은 genome 내에 풍부하게 존재하기 때문에 5’이나 3’ 끝에 2~4개의 임의의 염기를 가지는 16~18 bp의 반복서열로 구성된 단일 프라이머를 이용하여 genome 상의 여러 지역에서 증폭 가능하여 서로 다른 개체들 사이에서 증폭산물들이 다형성을 나타낸다(Godwin et al., 1997; Zietkiewicz et al., 1994). 화본과 식물의 기내배양에 의한 재분화 식물체의 유전적 변이와 다양성 연구는 ISSR 분석 등 다양한 방법(Carlos et al., 2018; Goh et al., 2011; Ramakrishnan et al., 2014)으로 진행되었다. 지금까지 화본과 식물에서 ISSR 분석 연구(Ramakrishnan et al., 2014)가 보고되고 있으나 띠(I. cylindrica var. koenigii (Ritz) Benth. ex Pilg.)와 홍띠에서는 본 연구팀의 연구(Kang et al., 2019; Kang et al., 2020) 외에 찾기 힘든 실정이다.
따라서 본 연구는 홍띠(Imperata cylindrica ‘Rubra’) 식물의 기내 식물체 재생과 재생 식물체의 유전적 안정성에 대한 자료를 제공할 목적으로 생장점 부위를 포함한 식물조직을 기내배양하여 식물체를 재생시키고, ISSR 표지를 사용하여 기내에서 재생된 녹색 식물체의 유전적 안정성을 조사하였다.
재료 및 방법
식물재료
공시재료는 재배식물로 개발된 홍띠(Imperata cylindrica ‘Rubra’)로 ‘하늘정원 야생화(대표 이동국)’에서 분양받았으며, 영양체 번식된 대조구 식물체(mother plant) 8개체, 실내의 포트에서 재배시킨 재분화 녹색 식물체 10개체, 1년간 노지에서 재배시킨 재분화 녹색 식물체 10개체로 총 28개체를 공시하였다(Fig. 1-G, H, I).

Fig. 1
In vitro regeneration process (A to F), and 28 individual accessions (G, H and I) used in ISSR analysis of Imperata cylindrica ‘Rubra’. A: Callus induction from in vitro cultured tissues including growing point, B: Shoot induction from calli, C: Multiple shooting, D: Regenerated plantlet growth with rooting, E: Hardening on sterilized vermiculite, F: Hardening under cap-open condition, G: Mother plants (Control), H: Green-regenerants cultivated at culture room, I: Green-regenerants cultivated at field condition.
기내 배양 및 식물체 재분화
홍띠의 기부생장점 부위를 포함한 식물체를 70% 에탄올에서 30초간, 2% sodium hypochlorite에서 15분, 멸균증류수에서 1분간 침지한 다음 3회 수세 후 멸균된 여과지로 수분을 제거하여 표면 살균하였다. 기본배지로 MS 배지(Murashige and Skoog, 1962)를 사용하였고, pH는 멸균 전 5.80±0.05로 적정하여 121℃, 1.2기압 하에서 15분간 멸균하였다. 재분화 녹색 식물체 재생은 Umami et al. (2012)의 띠(congongrass)의 기내 배양사례를 일부 수정하여 MS 배지 + 0.1 ㎎/L 2,4-D + 2.0 ㎎/L BA 첨가 배지에 생장점을 포함한 부위를 치상하여 캘러스를 유도하고, 캘러스 증식, 신초 재분화를 유도하였다. 재분화된 신초는 MS에 이식하여 뿌리를 유도하고 재생된 유식물체를 순화, 활착시켰다. 배양은 26±2℃, 25 μ㏖/s/㎡, 14h/10h (day/night)의 조건에서 실시하였다.
DNA 추출 및 ISSR 분석
DNA는 식물체의 잎 부위를 CTAB 방법(Fang and Roose, 1997)에 따라 추출하여 0.8%의 agarose gel에서 전기영동하여 밴드를 확인하고, Nanodrop Spectrophotometer (Thermo Fisher Scientific, Netherlands)로 농도를 측정하여 최종농도는 50 ng/μL로 희석하였다.
ISSR 분석은 총 26개의 ISSR 프라이머(UBC primer Set No. 9, University of British Columbia, Canada)로 예비 실험 후 밴드가 명확한 22개의 프라이머를 선발하여 ISSR 분석에 이용하였다(Table 1). PCR 반응액은 주형 DNA 50 ng/μL, 2X PCR Premix (LugenTM), 10 pmol 프라이머로 총 20 μL로 혼합하여 사용하였다. PCR 반응은 Gene Amp 2700 (Applied Biosystem)을 사용하여 94℃에서 5분간 초기 변성시킨 후 94℃에서 45초간 denaturation, 52℃에서 45초간 annealing, 72℃에서 90초간 extension 과정을 40회 수행한 후 최종적으로 72℃에서 7분간 반응시킨 후 종료하였다. PCR이 완료된 후의 증폭산물 15 μL를 RedSafe Nucleic Acid Staining Solution 20,000X (Intron Biotechnology, Inc.)를 첨가한 1.2% agarose gel에 loading하여 전기영동(50V, 60분)한 다음 GelDoc (GDS200D, Korea)을 사용하여 주요 밴드를 확인하였다.
Table 1.
Sequence of the 23 ISSR primers, numbers of total bands and polymorphic bands amplified by each primers across all 28 individuals of Imperata cylindrica ‘Rubra’
Data 분석
ISSR로 분석된 DNA 밴드 양상은 이진수를 이용하여 밴드 유·무에 따라 1과 0으로 data를 표시하여 Jaccard 계수 (Jaccard coefficient)로 유전적 유사도지수를 산출하고 평균연결법(Average linkage method)으로 군집분석을 하였다. 모든 통계처리는 SPSS V.12 (SPSS Inc., USA)를 이용하여 실시하였다.
결과 및 고찰
기내배양에 의한 식물체 재생
기내 식물체의 재분화를 위하여 홍띠의 기부에서 적출한 생장점 부위를 0.1 ㎎/L 2,4-D와 2 ㎎/L BA를 첨가한 MS (Murashige and Skoog, 1962) 배지에 치상하여 4주 동안 캘러스를 유도하고(Fig. 1-A), 0.1 ㎎/L 2,4-D와 0.05 ㎎/L BA 첨가 배지에서 3~4주 동안 캘러스를 증식하였다(Fig. 1-B). 캘러스로부터 신초를 유도하기 위하여 0.01 ㎎/L NAA와 2 ㎎/L BA를 첨가한 배지에서 증식된 캘러스를 이식하여 4~5주 동안 신초를 재분화시켰다(Fig. 1-C). 4~6주 동안 MS 배지에서 발근을 유도하여 재분화 식물체를 양성하고(Fig. 1-D), 멸균한 버미큘라이트 상토를 포함한 배양병에서 3주간 배양병의 뚜껑을 점진적으로 개방하여 직경 6 ㎝의 포트에 이식하여 100% 활착시켰다(Fig. 1-E, F, H). 재분화 식물체는 모체가 가지고 있는 붉은 색과 달리 녹색을 나타내었고, 이 재분화 식물체를 분석용 시료로 사용하였다.
Akashi and Ikeda (1989), Umami et al. (2012)은 띠의 생장점 부위를 이용하여 캘러스 유도시 주로 2,4-D를 단독처리하거나 옥신 대비 낮은 농도의 사이토키닌을 병행처리에서 효과적이고, 캘러스 증식에는 캘러스 유도 보다 낮은 농도의 2,4-D를 처리하였는데, 이는 본 연구의 홍띠에서도 비슷한 경향이었다. 또한, 신초의 재분화는 BA와 상대적으로 낮은 농도의 NAA 처리에서 양호했는데(Akashi and Ikeda, 1989; Goh et al., 2011; Kusano et al., 2003; Shigeki et al., 2009; Yu et al., 2015), 본 실험에서도 유사한 재분화 양상을 나타내었다.
재분화 녹색 식물체의 DNA 밴드 양상
녹색을 띠는 재분화 식물체를 실내에서 포트 재배한 10개체와 이 녹색 재분화 식물체를 노지 포장에서 재배한 10개체, 그리고 대조구로 모식물체 8개체, 총 28개체를 시료로 하여 재현성이 높은 22개의 ISSR 프라이머를 선발하여 분석하였다(Table 1). ISSR 분석결과, 대조구 8개체에서 밴드 수는 최저 1개(UBC 852, UBC 880)에서 최고 7개(UBC 810, UBC 827)로 한 프라이머 조합당 평균 밴드 수는 4.4개였다. 공시한 22개 프라이머 모두 동일한 밴드패턴을 나타내어 다형성 밴드는 검출되지 않았다.
실내재배 재분화 식물체에서 밴드 수는 최저 1개(UBC 852, UBC 880)에서 최고 7개(UBC 810, UBC 827)로 평균 밴드 수는 4.4개였으며, 다형성 밴드의 수는 최저 0개(UBC 804, UBC 815, UBC 820, UBC 824, UBC 826, UBC 827, UBC 836, UBC 845, UBC 847, UBC 848, UBC 852, UBC853, UBC 856, UBC 857, UBC 861, UBC 862, UBC 866, UBC 880, UBC 889, UBC 893)에서 최고 3개(UBC 810)였다. 20개 프라이머(UBC 804, UBC 815, UBC 820, UBC 824, UBC 826, UBC 827, UBC 836, UBC 845, UBC 847, UBC 848, UBC 852, UBC 853, UBC 856, UBC 857, UBC 861, UBC 862, UBC 866, UBC 880, UBC 889, UBC 893)에서 모두 동일한 밴드패턴을 나타내었고, 나머지 2개 프라이머(UBC 810, UBC 834)에서 4개의 다형성 밴드로 프라이머 당 0.18개가 검출되었다(Table 1, Fig. 2).
노지재배 재분화체에서 밴드 수는 최저 1개(UBC 852, UBC 880)에서 최고 7개(UBC 810, UBC 827)로 평균 밴드 수는 4.4개였으며, 다형성 밴드의 수는 최저 0개(UBC 804, UBC 820, UBC 824, UBC 826, UBC 827, UBC 834, UBC 836, UBC 845, UBC 847, UBC 848, UBC 852, UBC 853, UBC 856, UBC 857, UBC 861, UBC 862, UBC 866, UBC 880, UBC 889)에서 최고 1개(UBC 810, UBC 815, UBC 893)였다. 19개 프라이머(UBC 804, UBC 820, UBC 824, UBC 826, UBC 827, UBC 834, UBC 836, UBC 845, UBC 847, UBC 848, UBC 852, UBC 853, UBC 856, UBC 857, UBC 861, UBC 862, UBC 866, UBC 880, UBC 889)에서 모두 동일한 밴드패턴을 나타내었고, 나머지 3개 프라이머(UBC 810, UBC 815, UBC 893)에서 3개의 다형성 밴드로 프라이머 당 0.14개가 검출되었다(Table 1, Fig. 2).

Fig. 2
Examples of ISSR electrophoresis profiles for 28 individual accessions of Imperata cylindrica ‘Rubra’. Amplification products were separated on 1.2% agarose gels in 1×TAE buffer and photographed using gel documentation system (Bio-rad, USA). Lane M: 1kb ladder marker. Lanes 1~8: mother plants, 9~18: Regenerants cultivated at culture room (ReR), 19~28: Regenerants cultivated at field condition (ReF). All the primer names were included in Table 1.
이상과 같이 유전적 다형성 비율은 재분화체(실내포트 재배식물체 4.1%, 노지 재배식물체 3.1%)에서 대조구인 모식물체(0%) 보다 높게 나타났다. 이는 2,4-D 및 kinetin을 비롯한 기내배양에 사용한 생장조절제가 형태적, 유전학적 각종 변이(somaclonal variation)를 유발하는 것에 기인한 것으로 보인다(Bednarek and Renata, 2020; Coronel et al., 2018; Dewir et al., 2018; Garcia et al., 2019; Jin et al., 2008). 그러나 옥수수 재분화체(Ramakrishnan et al., 2014), 바나나 재분화체(Ray et al., 2006) 보다 낮거나 비슷한 수준(Liu et al., 2011)으로 재분화체들은 유전적으로 안정된 편이었다. 또한, 종자유래 갈대의 재분화 기내재생 식물체에서 프라이머 당 1.3개의 다형성 밴드 검출로 17%의 다형성 비율을 보인 보고(Ryu et al., 2013)와 가지과 다양한 품종의 잎절편 유래 재생식물체의 18.5% (Aversano et al., 2009) 보다 본 연구에서 다형성 비율은 낮게 나타났다.
유전적 유사도 지수
ISSR 마커를 이용하여 상기 총 28개체 재분화 식물체들의 유전적 유사도를 평가하였다(Table 2). 총 28개체 간의 유전적 유사도 지수는 최저 0.919(19, 21, 26, 27번과 17번)에서 최고에서 최고 1.00(13, 14번과 9, 10, 11, 12, 13번 외) 사이로 28개 개체간 전체 유전적 유사도 지수 평균은 0.972였다.
Table 2.
Genetic similarity matrix of Imperata cylindrica ‘Rubra’ 28 accessions revealed by ISSR analysisz
대조구 8개체의 유전적 유사도 지수 평균은 1.0이었으며, 실내재배 재분화 식물체 간의 유전적 유사도 지수 평균은 0.993, 노지재배 재분화체간의 유전적 유사도 지수 평균은 0.993로 기내 재생 식물체간의 유사도는 동일한 값을 나타냈다. 처리구 두 그룹이 대조구 보다 낮지만 매우 높은 유전적 유사도를 나타내어 재분화 식물체들의 유전적 구조가 매우 안정한 것으로 나타났다. 이 결과는 홍띠의 경우 국내외에서 ISSR 연구 보고의 사례를 거의 유래를 찾기 힘들며(Kang et al., 2020), 초본 식물의 ISSR 분석 시 재분화 식물체간 평균 유사도 0.982 (Liu et al., 2011), 목본식물의 재분화체를 ISSR 분석한 결과인 0.96~0.99 (Vijayan et al., 2015)에 비해 다소 낮거나 비슷하였고, 가지과 여러 품종 유래의 재분화체의 유전적 유사도 0.72~0.99보다는 높았다(Aversano et al., 2009).
군집분석
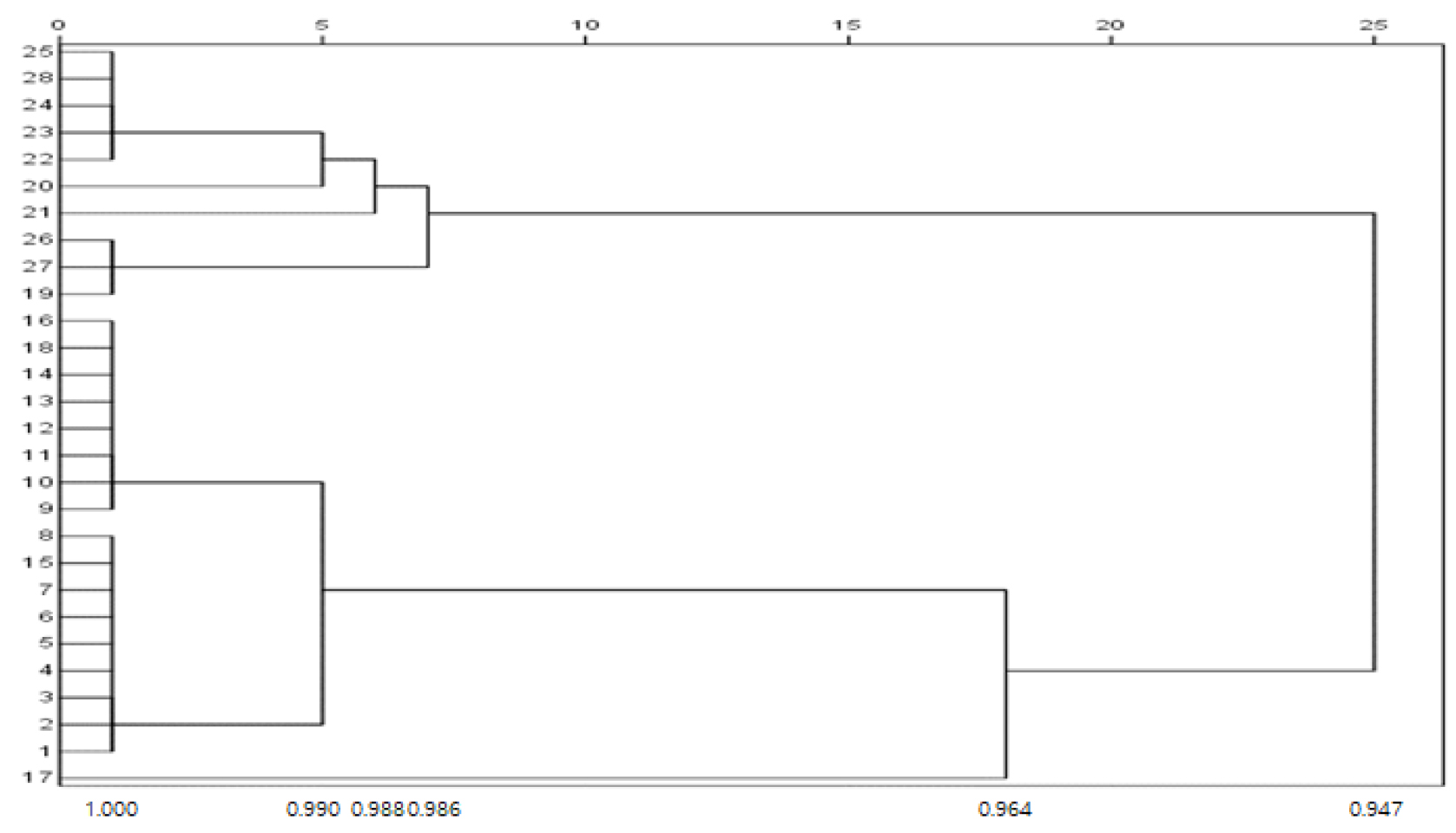
ISSR 분석결과를 토대로 ISSR 마커의 밴드 양상을 평균연결법(Average linkage method)으로 군집 분석한 결과는 Fig. 3과 같다. 모든 개체는 유사도지수 0.947~1.00 내에 분포하였다. 유전적 유사도지수 0.950에서 2개 그룹으로 유집되었으며, 대조구(1~8번)와 노지재배 재분화 식물체(19~28번)는 모두 분리되어 독립적인 그룹으로 유집되었다. 또한, 17번을 제외한 실내재배 재분화 식물체(9~18번)는 대조구와 같은 중그룹으로 유집되었다. 유전적 유사도지수 0.988에서 유집되는 2개의 하부 그룹에서 실내환경에서 재배한 재분화 식물체중 15번과 17번을 제외한 8개체(9~14번, 16, 18번)는 동일그룹으로 유집되었고, 대조구도 또다른 동일 그룹으로 밀접하게 유집되었다. 이러한 결과는 생장조절제 처리 등 배양시 유전적 변이를 유발하는 배지 내 여러 가지 환경(Garcia et al., 2019)에 기인한 것이 주요 원인이지만 Bednarek and Renata (2020)은 외부환경에 의한 변이의 가능성을 언급하고 있어 향후 장기적 관점에서 이에 대한 검토가 필요할 것으로 보인다. 한편 다년생 약용식물인 Inula 잎절편(Amin et al., 2018), 가지과 잎절편 유래 재분화체(Aversano et al., 2009) 및 옥수수 shoot apex 유래 재분화체를 대상으로 ISSR primer 분석(Ramakrishnan et al., 2014)한 결과 모식물체와 동일한 그룹으로 유집된 반면, 다른 품종별에서 유래한 재분화체는 다른 그룹으로 유집되어(Ray et al., 2006) 품종 또는 재분화식물체의 단일 개체 유래 여부에 따라 다른 결과를 보였다.
적 요
바이오에너지작물의 중요한 소재를 제공하는 화본과 식물인 홍띠(Imperata cylindrica ‘Rubra’)의 기내재생 식물체의 유전적 안정성을 조사하고자 생장점 부위를 기내배양하여 재분화시킨 녹색 재생식물체의 변이성을 ISSR 마커로 조사하였다. MS (Murashige and Skoog, 1962) 배지에 식물체 기부의 생장점 부위를 적출하여 캘러스를 유도하고(0.1 ㎎/L 2,4-D와 2 ㎎/L BA), 캘러스 증식(0.1 ㎎/L 2,4-D와 0.05 ㎎/L BA), 신초 재분화(0.01 ㎎/L NAA와 2 ㎎/L BA) 후 MS 배지에서 발근시켜 재분화 식물체를 유도하고 100% 활착시켰다. 대조구인 모식물체 홍띠 8개체, 1년간 노지 포장에서 재배중인 재분화 녹색 식물체 10개체와 실험실 내 화분에서 재배중인 재분화 녹색 식물체 10개체, 총 28개체에 대하여 ISSR 분석한 결과 유전적 다형성은 재분화 식물체가 실내포트 재배식물체 4.1% 및 노지 재배식물체 3.1%로 0%인 대조구보다 높게 나타났다. 또한, 총 28개체들 간의 유전적 유사도를 평가한 결과, 유전적 유사도 지수는 0.919~1.0 사이에 분포하며, 평균 0.972로 유전적 충실도가 높게 나타났다. 군집분석 결과 노지에서 재배한 재분화 식물체와 모식물체(대조군)가 독립적으로 유집되었다.