서언
재료 및 방법
분석용 연구재료
DNA 추출 및 정제
DNA 바코드 부위 증폭 및 염기서열 결정
분자계통학적 유연관계 분석
결과
염기서열 특징 및 변이
분자계통학적 유연관계 분석
고찰
적요
서언
천남성속(Arisaema L.) 식물은 천남성과(Araceae)에 속하는 다년생 초본식물이며, 최근 보고에 의하면 전 세계적으로 117속 4,095종이 분포하는 것으로 알려져 있다(Angiosperm phylogeny website ver. 13, 2016, http://www.mobot.org/ MOBOT/research/APweb/). 이들 중 천남성속은 약 150여 종으로 생태적으로 주로 숲의 하층에 서식하고 있다(Gusman and Gusman, 2002). 그 중 대부분인 140여 종이 히말라야, 스리랑카, 남인도, 중국, 한국, 일본과 동남아시아 등에 분포하고 1종이 네팔에서부터 사우디아라비아와 오멘을 거쳐 동아프리카까지 분포는 것으로 알려져 있으며, 5-6종은 동아프리카 고유종으로, 그리고 3종은 북아메리카에 분포하는 고유종으로 알려져 있다(Renner et al., 2004). 천남성속 식물은 독성식물로 알려져 있지만 한국, 중국, 일본 등의 아시아 지역에서는 둥근잎천남성(A. amurense Maxim. f. amurense), 두루미천남성(A. heterophyllum Blume), 및 일파산남성(=중국천남성, A. erubescens Schott)의 괴경을 예로부터 가래를 삭이고 경련을 멈추며 어혈을 없애는 효능이 있다고 하여 중풍, 얼굴신경마비, 반신불수, 파상풍, 관절통, 급성 및 만성기관지염 등의 치료하는 천남성(天南星, Arisaematis Rhizoma)이라는 약재로 사용해 왔다(Korea Institute of Oriental Medicine, 2017).
국내에 분포하는 천남성속 식물에 대해서는 Ko (2000)과 Ko et al. (2006)에서 섬천남성(A. negishii)이 2엽성 무늬천남성의 오동정으로 국내에 분포하지 않는다는 견해와 함께 둥근잎천남성(A. amurense f. amurense), 천남성(A. amurense f. serratum Nakai), 두루미천남성(A. heterophyllum), 무늬천남성(A. thunbergii Blume subsp. thunbergii), 점박이천남성(A. serratum (Thunb.) Schott), 눌맥이천남성(A. peninsulae f. convolutum (Nakai) Y. Kim et S. Ko), 섬남성(A. takesimense Nakai), 큰천남성(A. ringens (Thunb.) Schott)의 6종 2품종이 분포하는 것으로 보고되었으며, 2000년대 중반 거문천남성(A. thunbergii subsp. geomundoense S. C. Ko)이 무늬천남성의 아종으로 추가 보고되었다. 그러나 최근 분류학적 견해에 의하면 눌맥이천남성, 점박이천남성 및 섬남성의 분류학적 처리, 무늬천남성과 거문천남성의 분류학적 처리, 그리고 둥근잎천남성과 천남성의 분류학적 처리를 재정리하여 국내에는 눌맥이천남성을 제외한 6종 1아종 1품종에 해당하는 8분류군이 분포하는 것으로 보는 것이 지배적이다(2015 Proceeding of Asian Plant Distribution Research Society, unpublished data).
천남성속 식물은 잎의 개수와 형태, 불염포와 화수부속체의 모양 등을 기준으로 Tortuosa절(무늬천남성, 거문천남성, 두루미천남성), Arisaema절(둥근잎천남성, 천남성, 점박이천남성, 섬남성), Pistillata절(큰천남성)로 분류된다(Ko and Kim, 1985; Ko et al., 1987; Ko et al., 1990; Oh et al., 1990). 하지만 최근 화수 부속체가 S자 모양인지 채찍처럼 길게 늘어지는 것인지를 기준으로 Tortuosa절의 일부 또는 다수가 Flagellarisaema절로 옮겨지거나, 화수 부속체와 약의 형태 등을 기준으로 Pistillata절과 Arisaema절을 구분하지 않고 Pistillata절로 통합하는 방식으로 절의 분류체계가 변화하였다(Gusman and Gusman, 2002; Li et al., 2010). 이에 따르면 국내에 분포하는 두루미천남성과 무늬천남성은 Flagellariaema절로, 둥근잎천남성과 점박이천남성, 그리고 큰천남성은 Pistillata절로 분류된다(Murata et al., 2014).
최근 중합효소연쇄반응(PCR)을 이용한 염기서열 분석법뿐만 아니라 Next Generation Sequencing (NGS)을 이용한 유전체 분석법 등이 빠른 속도로 발달하면서 생물들의 DNA에 저장되어 있는 정보에 보다 쉽게 접근할 수 있게 되었고, 이 정보로 생물들의 과거 진화 경로를 유추하는 연구가 활발하게 진행되고 있다(Park et al., 2012; Hong et al., 2014). 특히 대량 sequencing 기술의 발달에 따른 다양한 식물 DNA 바코드 구간의 발굴은 분자유전학적 분석을 통한 계통유연관계를 밝히는데 이용되고 있다. 엽록체 게놈에 존재하는 matK와 rbcL 유전자는 식물의 종 동정과 계통분류학적 연구에 적합하다고 보고되고 있으며(Bremer et al., 2002; Bell, 2003; Purushothaman et al., 2014; Techen et al., 2014), 핵에 존재하는 rDNA-ITS 부위는 종간 염기서열 변이가 빈번하게 발생하는 특징으로 인하여 다양한 분류군의 계통분석 및 DNA 바코드 연구에 이용되고 있다(Álvarez and Wendel, 2003; China Plant BOL Group et al., 2011, Chen et al., 2010). 국내에서는 핵의 rDNA-ITS 부위와 엽록체 게놈의 다양한 DNA 바코드 염기서열을 이용하여 한국산 괭이눈속의 계통연구(Han et al., 2011), 한국산 담배풀속의 계통분류(Yoo and Park, 2012), 한국산 수국속의 계통연구(Kim et al., 2016), 한국산 피나무속의 계통연구(Boo and Park, 2016) 등 다양한 분류군에 대한 분자계통학적 유연관계를 분석하여 보고하였다.
국내에 분포하는 천남성속 식물의 분자계통분석 연구로는 Renner et al. (2004)이 아시아, 북아메리카, 동아프리카에 이르는 범위에 서식하고 있는 천남성속 식물 11개 절에 대한 분자계통학적 유연관계를 보고하면서 국내에 분포하는 일부 천남성이 포함되어 분석된 바 있으며, Jung et al. (2004)과 Lee and Kim (2005)은 각각 trnL-F 유전자 부위 염기서열 비교 분석, RAPD를 이용한 게놈 지문분석을 통해 종간 유연관계를 제안하였으나, 이 보고에서 절을 나누는 형태적 분류기준이 현재와 다르고 분류군의 처리도 현재와 달라 최근에 정리된 국내분포 천남성 6종 1아종 1품종 전체에 대한 DNA 바코드 기반 분자계통학적 유연관계 분석 연구는 진행된 바가 없다.
따라서 본 연구에서는 Consortium for the Barcode of Life (CBOL)에서 식물의 DNA 바코드로서 사용하는 것을 추천한 엽록체 유전자인 matK와 rbcL 부위와 함께(CBOL Plant Working Group, 2009), 약용 식물들과 그 근연종들의 판별에 적합하다고 보고된 rDNA-ITS 부위의 염기서열 정보를 바탕으로(Chen et al., 2010), 약용으로 사용되는 중국 분포 천남성 1종과 국내에 분포하는 천남성속 식물 6종 1아종 1품종을 포함하는 9개 분류군에 대한 분자계통학적 유연관계를 분석하여, 첫째로 한국산 천남성속 식물에 대한 분자계통학적 분석을 기반으로 이들의 절과 종간의 분류학적 유연관계와 형태학적 분류 체계와의 상관성을 확인하고자 하였으며, 둘째로 국내 천남성과 다른 절(Sinarisaema절)에 속하고 중국에 주로 분포하며 정품 한약재로 사용 가능한 일파산남성을 포함하여 한약재 천남성으로 약용할 수 있는 천남성 3종과 사용할 수 없는 천남성 종 간의 분류학적 근연관계를 확인하고자 하였다.
재료 및 방법
분석용 연구재료
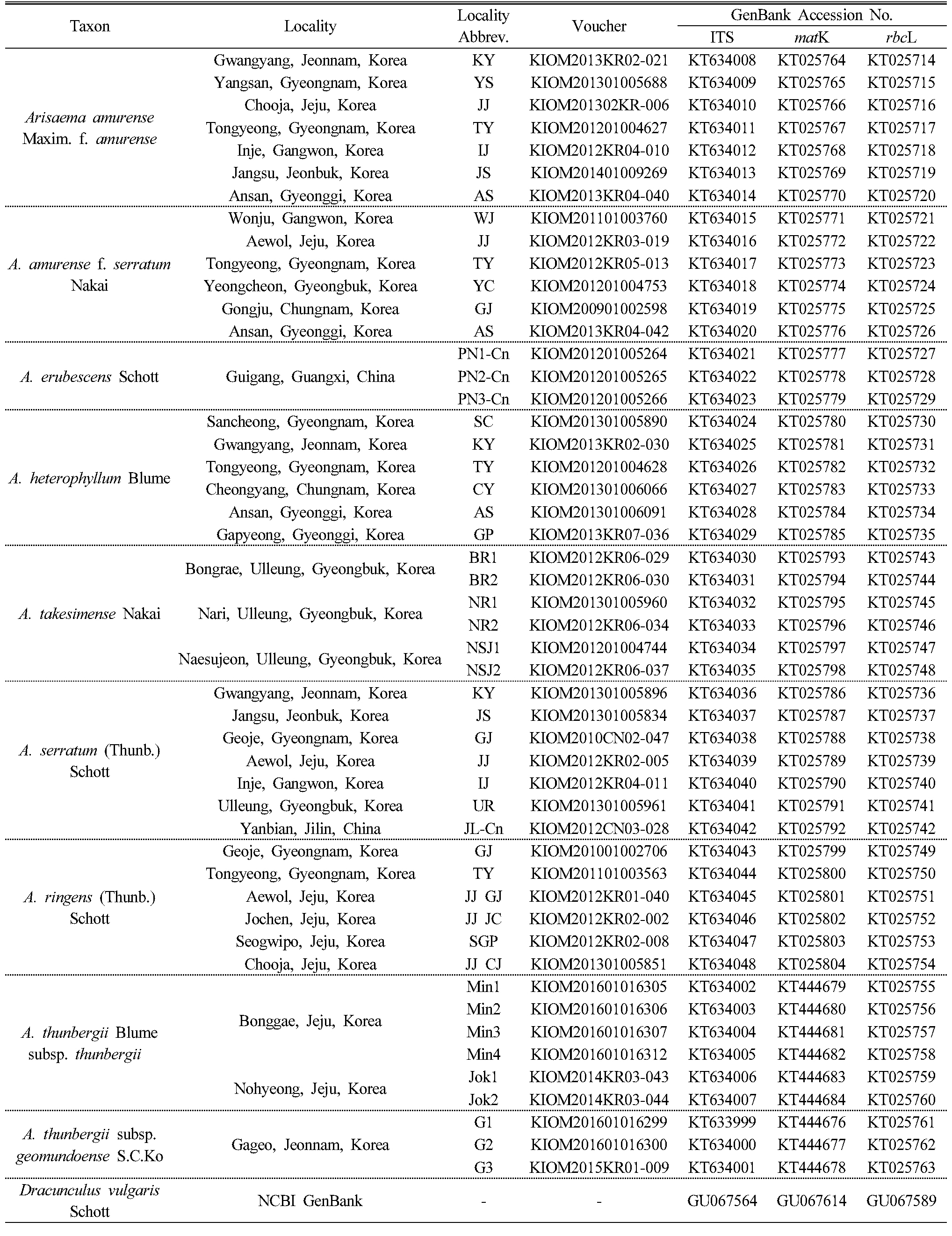
본 실험에 사용한 둥근잎천남성 7개체, 천남성 6개체, 두루미천남성 6개체, 섬남성 6개체, 점박이천남성 7개체, 큰천남성 6개체, 무늬천남성 6개체는 한국 또는 중국의 다양한 자생지에서 수집하였으며, 일파산남성 3개체 및 거문천남성 3개체는 각각 중국과 한국의 자생지에서 서로 다른 개체를 수집하여 총 50개체의 시료를 분석에 사용하였다(Table 1). 분석에 이용된 재료의 식물명은 The Plant List (http://www.theplantlist.org/)를 기준으로 정리하였으며, 약용과 비약용 천남성의 분류학적 특성을 확인하고자 중국천남성(일파산남성)을 포함하였다. 각 시료의 증거표본은 석엽표본으로 제작하여 한국한의학연구원 한약표준표본관(KIOM)에 보관하였다(Table 1).
DNA 추출 및 정제
국내·외 자생지에서 수집하여 –70℃에 보관한 기원식물 생체시료 약 100 ㎎을 Lysing matrix (MP biomedicals, USA)와 PrecellysTM Grinder (Bertin technologies, France)를 이용하여 마쇄한 후, DNeasy Plant Mini Kit (QIAGEN, USA)를 이용하여 제작자가 제공한 protocol에 따라 추출·정제하였다. 정제된 DNA의 순도와 품질을 확인하기 위하여 1.5% agarose gel에서 전기영동 후, EcodyeTM Nucleic Acid Staining Solution (Biofact, Korea)으로 염색하여 UV light 상에서 DNA band를 확인하였으며, UV spectrophotometer (Nanodrop, USA)를 이용하여 260 ㎚와 280 ㎚에서 흡광도를 측정하여 정량하였다.
DNA 바코드 부위 증폭 및 염기서열 결정
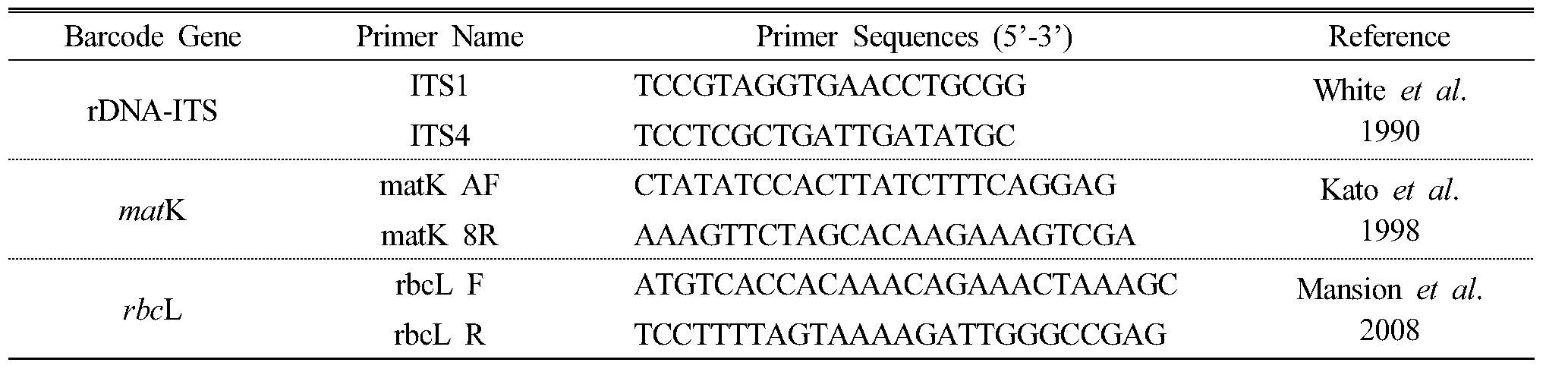
DNA 바코드 부위를 증폭하기 위하여, 각 DNA 바코드 영역에 특이적인 정방향과 역방향 10 pmole primer (Table 2) 각 2 ㎕, SolgTM 2XTaq PCR Smart-Mix I (Solgent, Korea) 20 ㎕, D.W. 15 ㎕, 그리고 15 ng의 genomic DNA 1 ㎕를 혼합하여 총 40 ㎕의 혼합물을 만들고, 이를 DNA Engine Dyad Thermal Cycler (MJ Research, USA)를 사용하여 증폭하였다. PCR 반응은 95℃에서 5분간 pre-denaturation한 후, 95℃에서 30초 denaturation, 53℃에서 40초 annealing, 72℃에서 1분 extension을 총 35회 반복 수행하고 마지막으로 72℃에서 5분간 final-extension을 거쳐 수행하였다.
DNA 바코드 부위 증폭산물의 확인을 위하여 각각의 증폭산물을 1.5% agarose gel 상에서 EcodyeTM Nucleic Acid Staining Solution (Biofact, Korea)으로 염색한 후, 100 bp DNA ladder (Solgent, Korea)와 함께 전기영동하였다. 정확하게 증폭된 rDNA-ITS 부위, matK 및 rbcL 유전자 증폭산물을 agarose gel로부터 회수하여 Gel Extraction Kit (QIAGEN, USA)를 이용하여 정제한 뒤, pGEM-Teasy Vector Systems (Promega, USA)에 삽입하였다. 삽입된 증폭산물은 XL1-Blue MRF’ competent cell (Stratagene, USA)에 형질전환한 뒤, ampicillin과 X-gal/ IPTG가 첨가된 LB agar 배지에 도말하여 37℃에서 약 20시간 배양하였다. 배양된 colony들을 대상으로 T7과 SP6 primer를 이용한 colony PCR을 통해 증폭산물이 정확히 삽입되었는지 확인하였다. PCR error, misreading, 지역적 염기서열 변이 등과 같은 요인들의 영향을 낮추기 위하여 각 시료별로 최소 3개의 white colony를 선별하여 각각 액체배양하고 Plasmid Mini Preparation Kit (QIAGEN, USA)를 이용하여 plasmid DNA를 분리한 후, T7과 SP6 primer를 이용하여 ABI3730 automatic DNA sequencer (Applied Biosystems, USA)에서 염기서열을 해독하였다. 염기서열의 정확성과 신뢰성을 확립하기 위한 Nilsson et al. (2012)의 가이드라인에 따라 각 시료별로 분석된 최소 3개의 colony의 염기서열을 비교하고 PCR 증폭과정에서의 오류를 확인한 후, NCBI GenBank BLAST 검색을 통하여 키메라의 존재 유무를 판별하고 종을 확인하는 과정을 거쳐 각 시료에 대한 최종 염기서열을 확정하였다.
분자계통학적 유연관계 분석
확보된 천남성 9분류군 50개체의 DNA 바코드 염기서열과 함께, 군외군으로는 같은 천남성과에 속해있으며 분석대상 부위(ITS, matK, rbcL)의 염기서열 정보가 모두 NCBI GenBank에 등록되어 있는 종인 Dracunculus vulgaris의 염기서열을 내려 받아 계통유연관계를 검토하였다. 총 51개체의 rDNA-ITS, matK, rbcL 부위의 염기서열을 각각, 그리고 합쳐서 MEGA version 7 (Kumar et al., 2016)의 ClustalW 방법으로 multiple alignment를 수행하여 정렬하였다. 그리고, 동 프로그램을 이용하여 Subtree-Pruning-Regrafting (SPR) 알고리즘으로 1,000회 반복의 bootstrapping method (Felsenstein, 1985)를 적용하여 Maximum parsimony 분석을 수행한 다음, 10개의 도출된 계통수를 합쳐 consensus tree를 최종적으로 도출하였다. 이때, matK와 rbcL 유전자의 Gaps/Missing data는 Complete deletion으로 처리하였고, 염기서열 상에 길이 변이가 많은 rDNA-ITS 부위는 Use all sites 방법으로 처리하였다. 그리고 이를 통해 CI 값(Consistency Index)과 RI 값(Retention Index)을 도출하였다. Neighbor-Joining 계통수(Saitou and Nei, 1987; Farris et al., 1996)는 동 프로그램에서 Kimura’s two- parameter method (Kimura, 1980) 모델로 계산된 염기변이 값을 기초로 하여, bootstrap 1000회 반복으로 도출하였다. GC 비율과 parsimony informative character, constant character, 그리고 variable character의 수는 DnaSP version 5.10.01 (Librado and Rozas, 2009) 프로그램을 사용하여 계산하였다. 도출된 계통수는 TreeGraph2 version 2.13 (Stöver and Müller, 2010) 프로그램을 사용하여 편집하였다. ITS 부위와 matK, rbcL의 염기서열을 유합한 combined data의 적합성을 판단하기 위하여 PAUP* version 4.0 (Swofford, 2002)에서 Incongruence Length Difference (ILD) test (Farris et al., 1995)를 수행하였다.
결과
염기서열 특징 및 변이
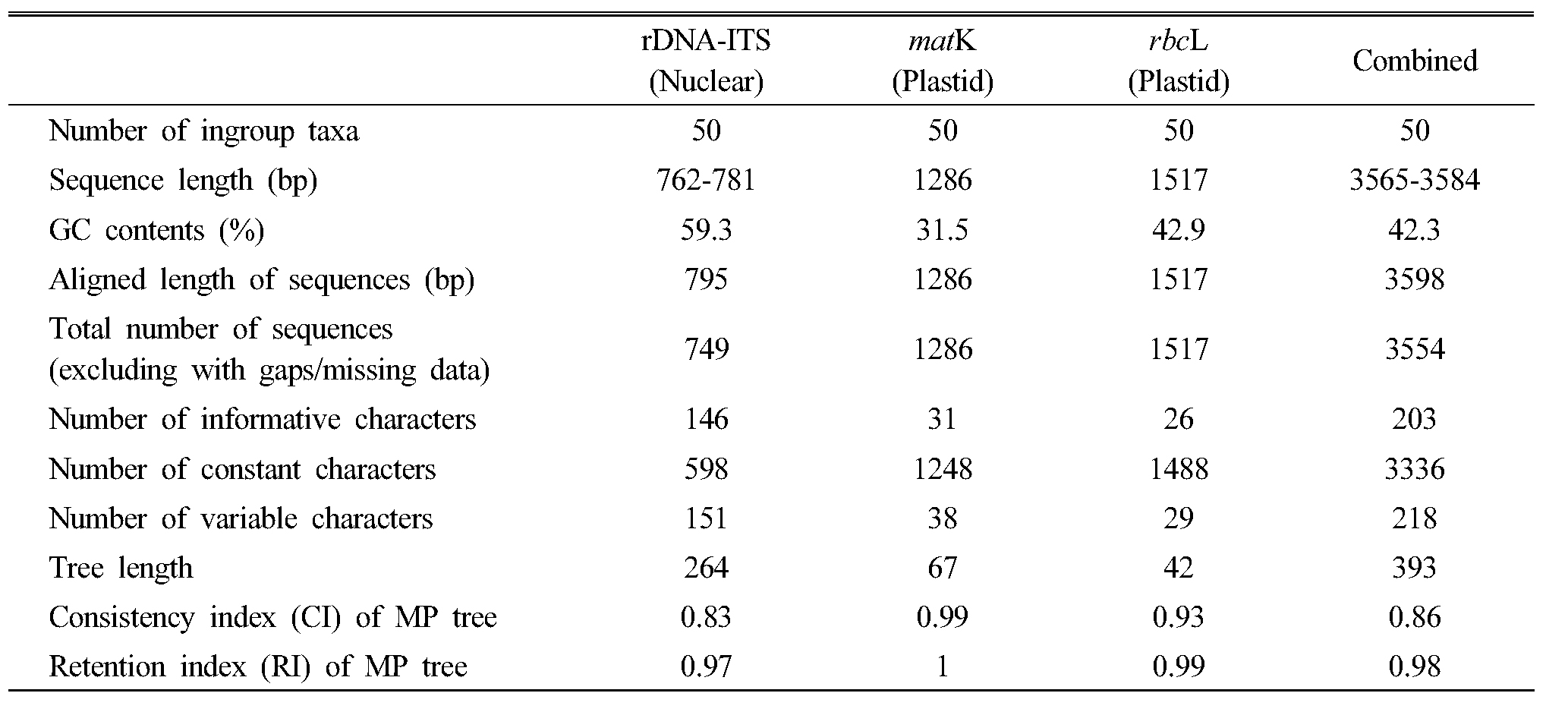
천남성 9분류군 50개체로부터 증폭된 rDNA-ITS 부위, matK 및 rbcL 유전자를 T-vector에 cloning하고 염기서열을 해독하여 각 개체별 증폭산물의 염기서열을 비교한 결과 PCR 과정에서의 오류나 염기서열 해독과정에서의 오류는 확인되지 않았으며, 이들 염기서열을 이용하여 NCBI GenBank BLAST 검색으로 그 종을 확인하였다. 이와 같은 검토를 통해 최종 확정된 각 개체의 rDNA-ITS, matK 및 rbcL 증폭산물 염기서열과 군외군 1개체를 포함한 전체 51개 시료의 DNA 바코드 염기서열을 분석한 결과, rDNA-ITS 부위는 762-781 bp, matK 유전자는 1,286 bp, 그리고 rbcL 유전자는 1,517 bp의 염기로 구성되어 있었으며, 이들 염기서열은 ClustalW 방식으로 최대 정렬하였을 경우 각각 795 bp, 1,286 bp, 1,517 bp의 길이로 정렬되었다(Table 3). 각 DNA 바코드별 염기서열 변이는 rDNA-ITS부위에서 151개의 염기쌍에서 변이가 확인되어 분석에 사용된 세 유전자 부위 중 가장 변이가 많았고, 그 다음으로 matK 유전자가 38개 염기쌍에 변이가 있었으며, rbcL 유전자가 29개 염기쌍으로 변이가 가장 적었다. 계통학적으로 유용한 형질은 rDNA-ITS 부위에서 146 bp, matK 및 rbcL 유전자에서 각각 31 bp와 26 bp로 확인되어 유용형질 역시 rDNA-ITS 부위가 가장 많은 것으로 나타났다. 각 DNA 바코드 구간의 G+C (%) 함량은 rDNA-ITS 부위 59.3%, matK 유전자 31.5% 그리고 rbcL 유전자 42.9%로 확인되었다(Table 3).
분자계통학적 유연관계 분석
천남성속 9 분류군의 rDNA-ITS 부위와 matK 유전자 개별 염기서열을 이용한 Maximum Parsimony (MP) 계통수 분석 결과, rDNA-ITS 부위를 이용한 계통수는 264단계로 구성되어 있었고, CI (Consistency Index) 값은 0.83, RI (Retention Index) 값은 0.97로 나타났다. matK 유전자의 경우 67단계로 구성되어 있었으며, CI 값과 RI 값은 각각 0.99, 1.0으로 나타났다(Table 3). rDNA-ITS 부위와 matK 유전자를 이용한 strict consensus tree에서는 두 DNA 바코드 구간 모두 세 개의 절(Pedatisecta, Sinarisaema, Tortuosa)이 뚜렷하게 분계조로 구분이 되었는데, 1차적으로 크게 Pedatisecta절 및 Sinarisaema절로 구성된 부분과 Tortuosa절로 구성된 부분으로 나뉘었다(Fig. 1-2). 첫 번째 분계조에서는 일파산남성이 rDNA-ITS 부위와 matK 유전자가 각각 bootstrap value 100%와 97%로 기부에서 독립적으로 분지되어(Clade IV) 단계통의 Sinarisaema절을 형성하였다(Fig. 1-2). Pedatisecta절에 해당되는 부분에서는 rDNA-ITS 부위의 경우에는 둥근잎천남성과 천남성이 하나의 독립된 분계조(Clade I)를 형성하였고, 큰천남성이 단일종으로 분계조를 형성하였으며(Clade III), 섬남성과 점박이천남성이 bootstrap value 99%로 하나의 분계조(Clade II)를 이루었다(Fig. 1). matK 유전자의 경우에는 큰천남성이 기부에서 1차적으로 독립된 분계조(Clade III)를 형성하였고, 둥근잎천남성과 천남성이 bootstrap value 100%로(Clade I), 섬남성과 점박이천남성이 bootstrap value 84%로(Clade II) 각각의 분계조를 이루었다(Fig. 2). Tortuosa절의 경우 rDNA-ITS에서 100%, matK 유전자에서 98-99%의 bootstrap value로 Clade V의 두루미천남성, Clade VI의 무늬천남성과 거문천남성이 각각 단계통을 이루었다(Fig. 1-2).
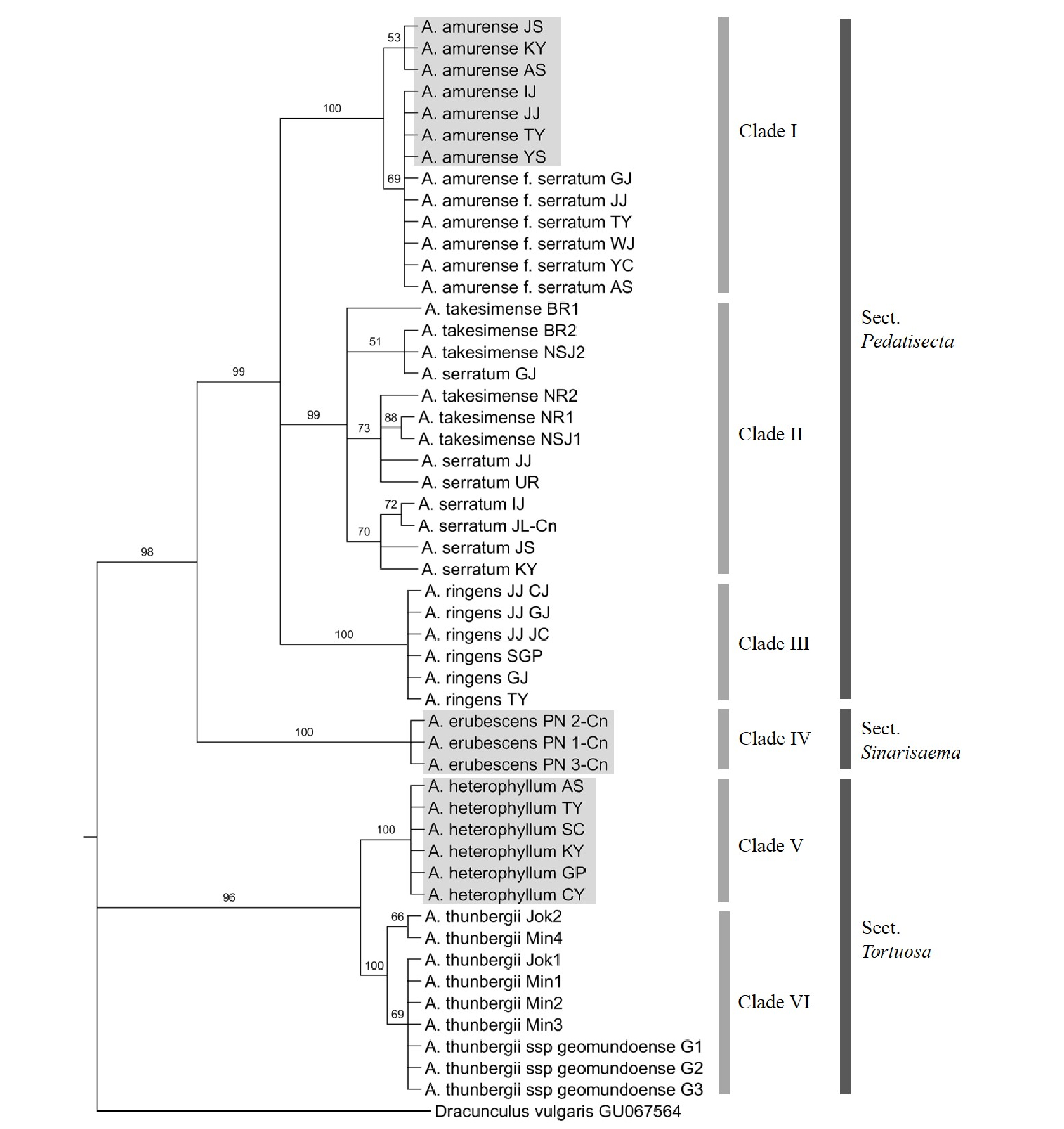
Fig. 1.
Bootstrap consensus tree inferred using the Maximum Parsimony method based on nuclear rDNA-ITS sequences of the Arisaema species. Branches in less than 50% bootstrap replicates are collapsed. The numbers above branches indicate bootstrap values. The samples in the grey rectangles are the authentic medicinal Arisaema species.
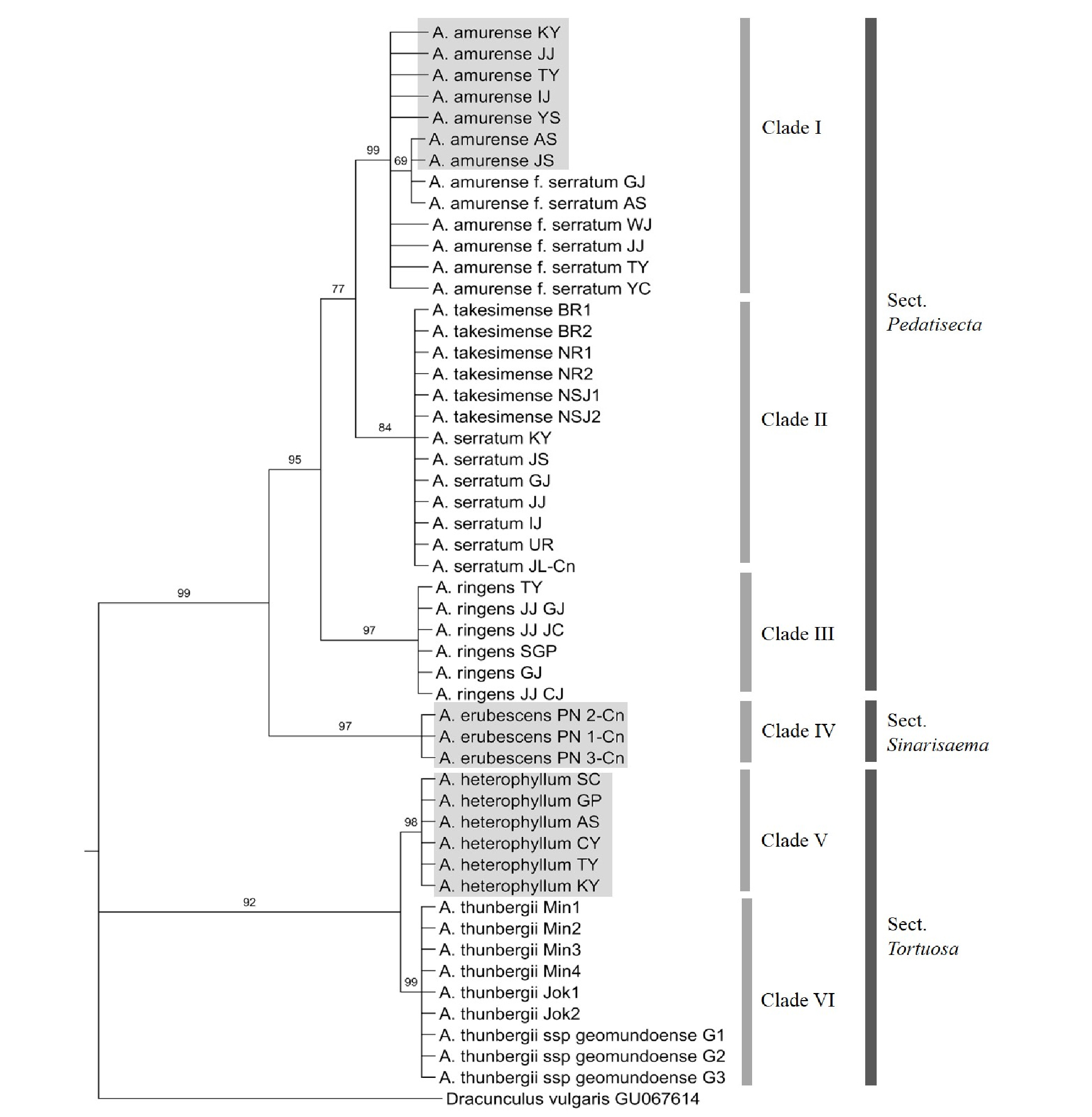
Fig. 2.
Bootstrap consensus tree inferred using the Maximum Parsimony method based on chloroplast matK sequences of the Arisaema species. Branches in less than 50% bootstrap replicates are collapsed. The numbers above branches indicate bootstrap values. The samples in the grey rectangles are the authentic medicinal Arisaema species.
rbcL 유전자를 이용한 분석에서는 42단계로 구성된 MP 계통수가 도출되었고, CI 값과 RI 값은 각각 0.93과 0.99로 나타났다(Table 3). Pedatisecta절의 경우, matK의 MP 계통수의 형태와 유사하게 큰천남성이 기부에서 1차적으로 독립된 분계조(Clade III)를 형성하였고, 둥근잎천남성과 천남성이 bootstrap value 92%로(Clade I), 섬남성과 점박이천남성이 bootstrap value 97%로(Clade II) 각각의 분계조를 이루었다(Fig. 3). 일파산남성(Clade IV), 두루미천남성(Clade V), 그리고 무늬천남성과 거문천남성이 형성한 단일의 분계조(Clade VI)는 군외군인 Dracunculus vulgaris와 함께 모두 basal node에서 각각 분지된 형태를 보이며, rDNA-ITS와 matK 유전자에서 Tortuosa절이 하나의 단계통군을 형성했던 것과는 다른 양상을 보였다(Fig. 1-3).
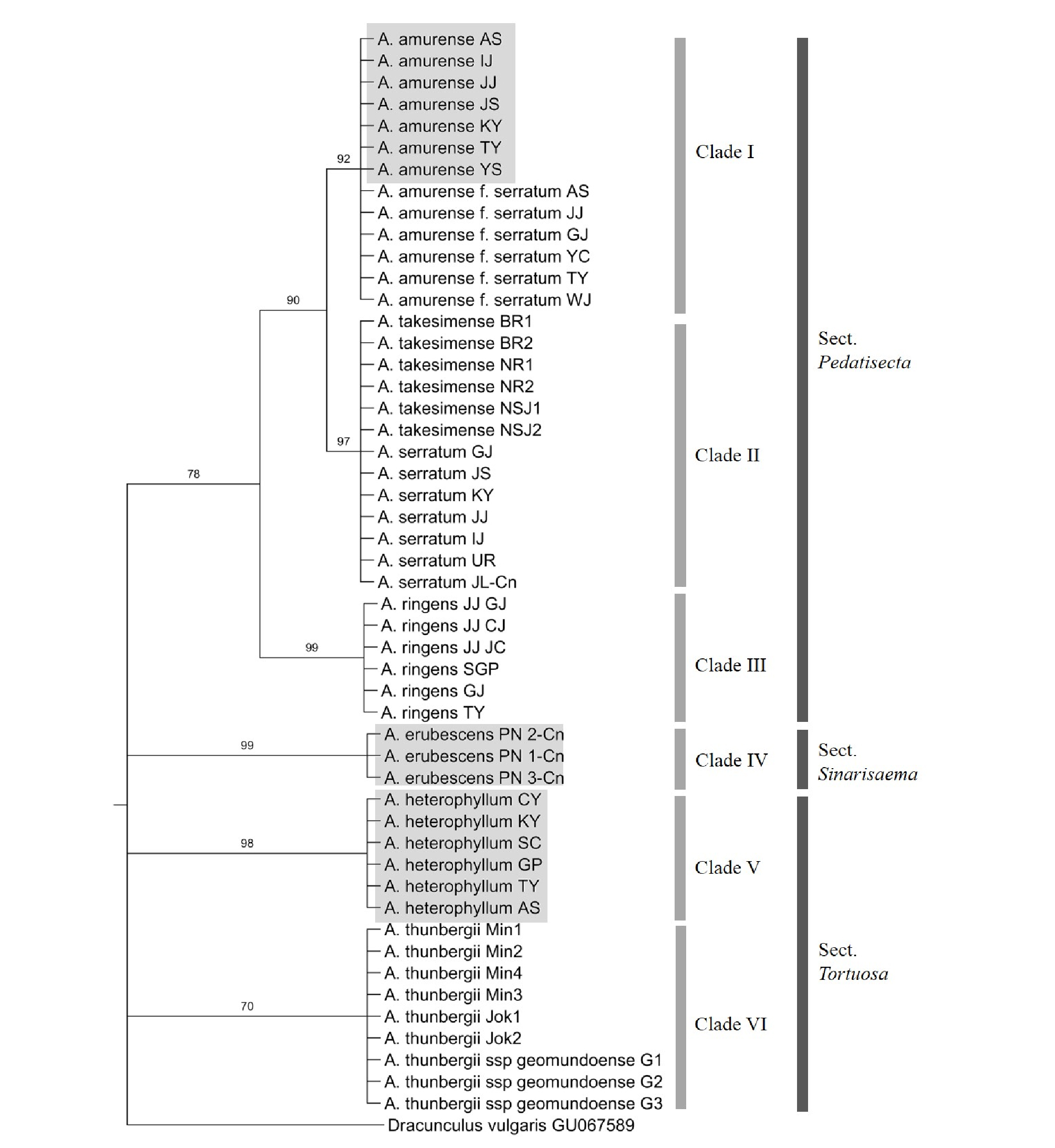
Fig. 3.
Bootstrap consensus tree inferred using the Maximum Parsimony method based on chloroplast rbcL sequences of the Arisaema species. Branches in less than 50% bootstrap replicates are collapsed. The numbers above branches indicate bootstrap values. The samples in the grey rectangles are the authentic medicinal Arisaema species.
rDNA-ITS, matK 및 rbcL 세 개의 부위를 유합한 combined data의 ILD test를 수행한 결과, p-value가 0.91로, 세 부위들이 homogeneous 한 관계에 있다는 귀무가설을 기각하지 못하므로 combined data로서 적합한 것으로 판단되었다. 이에 따라 천남성속 9개 분류군에 대한 MP 분석 결과, 393단계로 구성된 계통수를 도출하였으며, CI 값은 0.86, RI 값은 0.98로 나타났다(Table 3). 유합한 MP 계통수 역시 세 개의 절(Pedatisecta, Sinarisaema, Tortuosa)이 뚜렷하게 구분이 되었는데, 1차적으로 크게 Pedatisecta절 및 Sinarisaema절로 구성된 부분과 Tortuosa절로 구성된 부분으로 나뉘었다. 둥근잎천남성과 천남성, 점박이천남성과 섬남성은 모두 100%의 bootstrap value로 하나의 분계조를 이루며 단계통을 형성하고 큰천남성과 자매군을 이루며 Pedatisecta절로 분류되었다(Fig. 4). 국내 분포종이 아닌 일파산남성은 둥근잎천남성 및 천남성, 점박이천남성, 섬남성 및 큰천남성으로 구성된 Pedatisecta절과 하나의 분계조를 이루며 가장 먼저 분지하여 Sinarisaema절을 형성하였다(Fig. 4). 또한 무늬천남성과 거문천남성이 하나의 분계조를 이루고, 두루미천남성이 이들 분계조와 함께 단계통군을 형성하면서 Tortuosa절로 분류되었다(Fig. 4). 이러한 결과는 앞에서 설명한 rDNA-ITS와 matK 유전자로부터 얻은 계통수에서 분계조를 이루는 형태와 같은 결과이다. NJ 계통수 분석 결과에서도 마찬가지로 둥근잎천남성과 천남성, 그리고 점박이천남성과 섬남성이 100% bootstrap value로 하나의 계통을 형성하면서 자매군인 큰천남성과 함께 Pedatisecta절로 분류되었고, 거문천남성과 무늬천남성이 100%의 bootstrap value로 두루미천남성과 Tortuosa절을 이루었으며, 일파산남성 역시 Pedatisecta절과 분계조를 이루며 분류되었다(Fig. 5). 즉, 본 연구에서 분석한 rDNA-ITS, matK 및 rbcL 유전자 및 이들 세 개의 부위를 유합하여 도출한 MP 및 NJ 계통수 모두 유사한 형태로 종과 절을 분류하였으나, rDNA-ITS와 matK 유전자가 분계조를 이루는 형태와 rbcL 유전자가 분계조를 이루는 형태를 비교하였을 경우, 세 개의 범용성 DNA 바코드 구간 중 rbcL 유전자 보다 rDNA-ITS나 matK 유전자 부위가 천남성속의 계통분류와 유연관계 분석에 더 적합한 DNA 바코드 부위임을 지지하는 결과를 얻었다(Fig. 1-5).
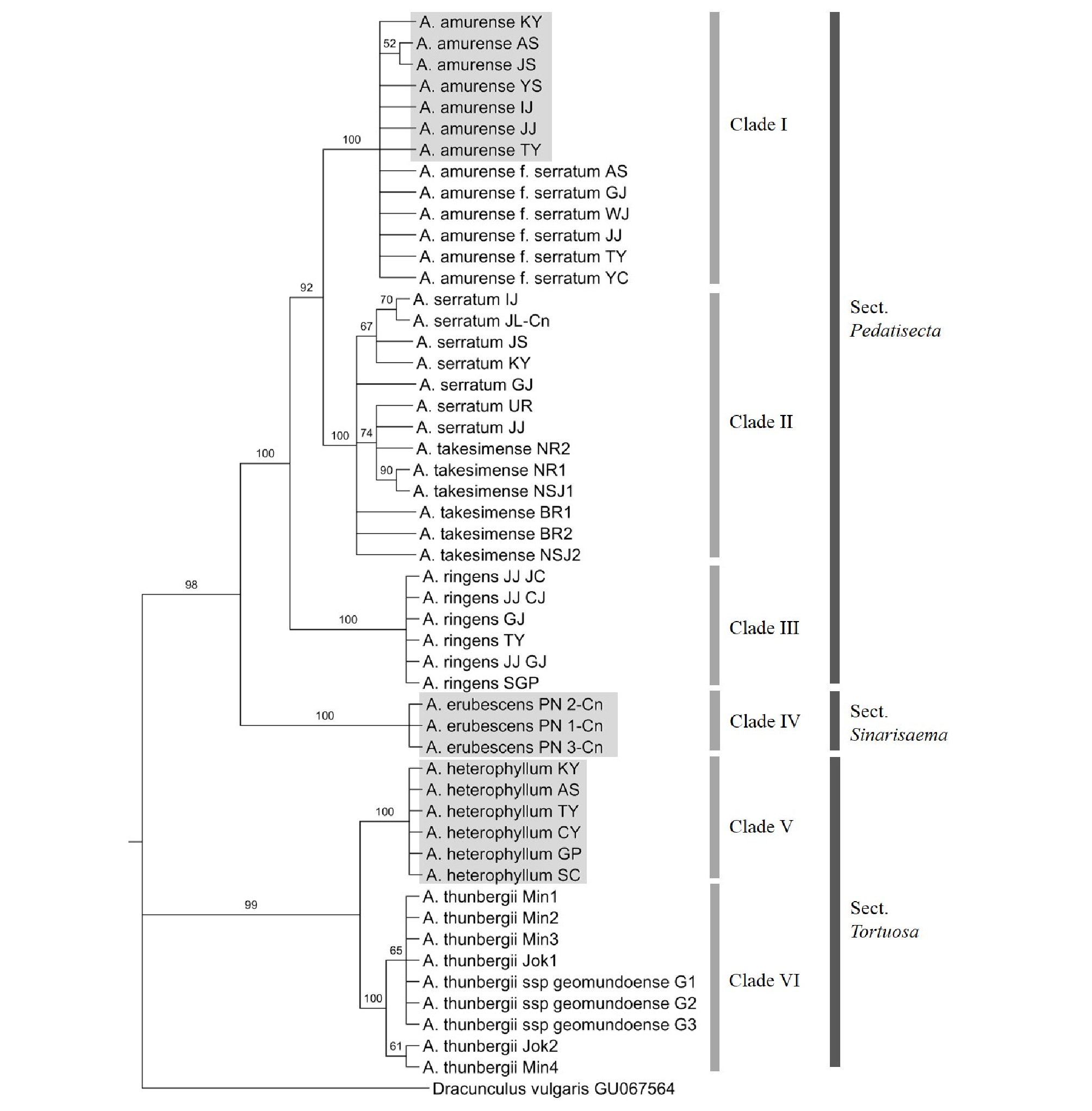
Fig. 4.
Bootstrap consensus tree inferred using the Maximum Parsimony method based on the combined sequences (rDNA-ITS, matK, and rbcL) of the Arisaema species. Branches in less than 50% bootstrap replicates are collapsed. The numbers above branches indicate bootstrap values. The samples in the grey rectangles are the authentic medicinal Arisaema species.
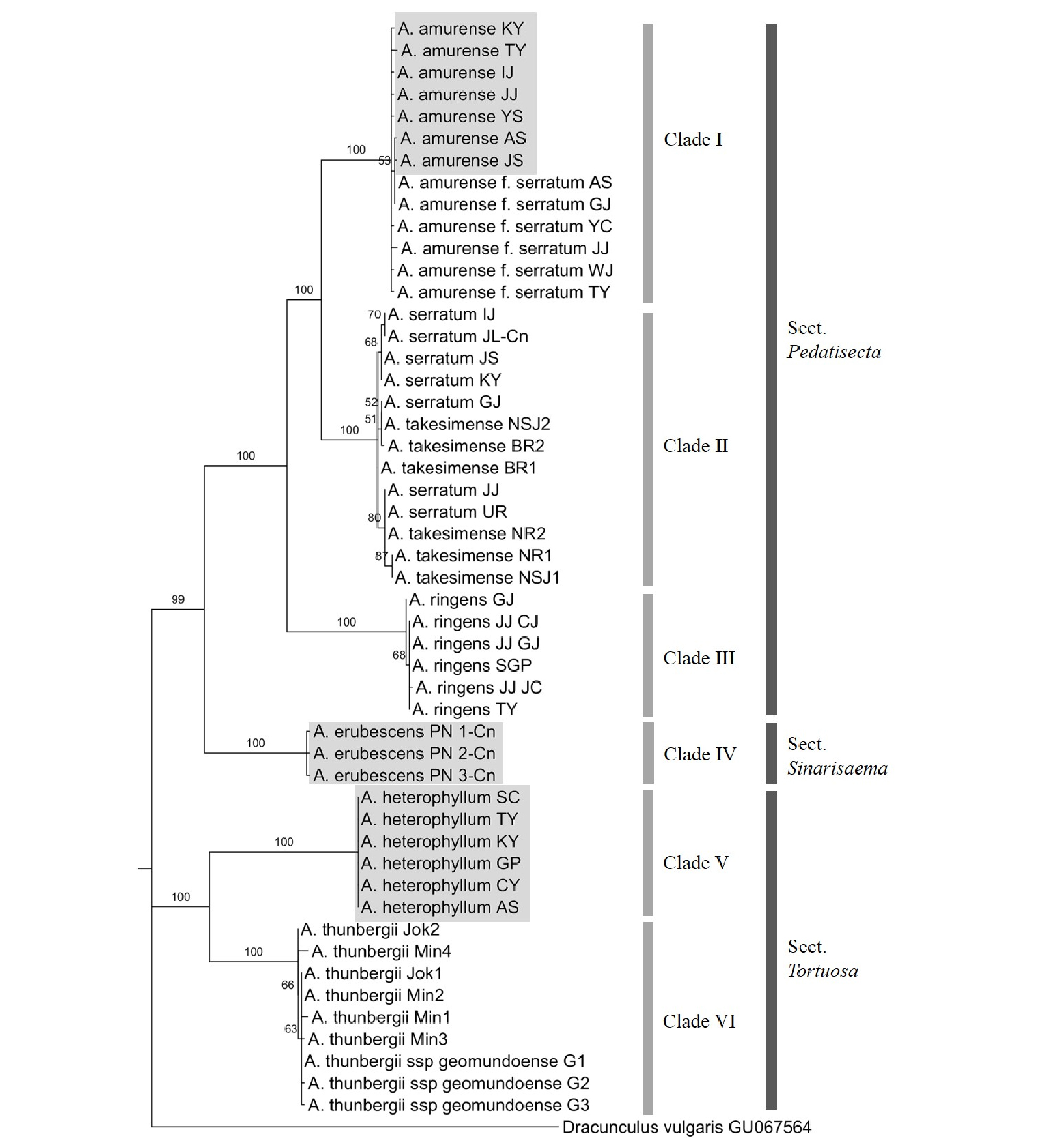
Fig. 5.
Phylogenetic tree inferred using the Neighbor-Joining method based on the combined sequences (rDNA-ITS, matK, and rbcL) of the Arisaema species. Branches in less than 50% bootstrap replicates are collapsed. The numbers above branches indicate bootstrap values. The samples in the grey rectangles are the authentic medicinal Arisaema species.
고찰
천남성속 식물의 분류체계와 계통학적 유연관계 분석에 있어서 잎의 수, 소엽편의 배열양상 및 화수부속체의 모양은 중요한 형태적 형질들로 알려져 있다(Ko, 2000). 이들 형태적 특징들에 대한 정성적·정량적 형질이 비교적 상세히 검토된 Murata (1984, 1990, 1991)의 분류 기준에 따라, 천남성속 식물은 화수부속체가 채찍모양으로 불염포 밖으로 길게 나오며 기부에 병이 없는 분류군인 Tortuosa절과, 화수부속체가 원주형 또는 곤봉형으로 불염포보다 짧으며 기부에 병이 있는 분류군인 Pedatisecta절로 세부분류 되었다(Ko, 2000). 본 연구에서 엽록체 게놈에 존재하는 matK와 rbcL 유전자 염기서열과 핵의 rDNA-ITS 염기서열을 이용하여 천남성속 식물에 대한 분자계통학적 유연관계를 분석한 결과, rbcL 유전자의 경우 종 및 절간 유연관계 분석에 있어 해상력이 다소 낮게 나타났으나, rDNA-ITS와 matK 유전자의 경우 천남성속의 속 이하 분류에 분자마커로서 충분히 활용할 수 있음을 알 수 있었다(Fig. 1-3). 뿐만 아니라 국내에 분포하는 천남성속 식물 중 둥근잎천남성, 점박이천남성, 큰천남성 등과 같이 화수부속체의 모양이 원주형이고 기부가 평저이며 병이 있는 형태와, 두루미천남성과 같이 기부가 비후되어 있으면서 직립하지만 sigmoid형으로 구부러진 형태, 그리고 무늬천남성과 같이 기부가 비후되어 있으며 가는 실 모양으로 길게 늘어진 형태의 3가지 화수부속체 모양에 따라 절이 분류되지 않았음을 확인하였다(Fig. 1-3)(Ko, 2000). 그리고 일파산남성이 Sinarisaema절로 분계조를 이루고 큰천남성이 둥근잎천남성이나 점박이천남성과 유전적 거리를 두고 독립된 분계조를 이루는 것으로 보아 화수부속체의 모양과 같은 하나의 형태학적 특징으로 절과 아절을 분류하는 것은 적절하지 않음을 분자계통 분석을 통해 다시 확인할 수 있었다(Gusman and Gusman, 2002).
Tortuosa절의 경우 무늬천남성을 하나의 type으로 하고 Flagellarisaema속과 두루미천남성을 하나의 type으로 하여 Heteroarisaema속이라는 새로운 속의 분류군으로 처리하기도 하였으며, Arisaema속의 Tortuosa절로 포함되었다가 Fagellarisaema절로 일부종이 옮겨지기도 하였고, 다시 Tortuosa절을 Tortuosa아절과 Flagellarisaema아절로 분류하기도 하였다(Nakai, 1950; Ko, 2000; Gusman and Gusman, 2002). 본 연구에서 세 가지 유전자 부위를 유합하여 얻은 계통학적 유연관계를 분석한 결과, 무늬천남성과 두루미천남성이 Clade V와 Clade VI를 아우르는 하나의 분계조로 묶이는 것으로 보아 위경의 길이와 화분 돌기 사이의 형태적 특징 등을 고려하여 Tortuosa절로 분류했던 기존의 연구결과를 지지하는 것으로 나타났다(Engler, 1920; Nakai, 1950; Ko, 2000; Gusman and Gusman, 2002). 그러나 최근 분자계통 연구와 세포학적 연구를 토대로 A. tortuosum만을 Tortuosa절에 포함시키고 나머지를 Flagellarisaema절로 처리하는 등 학자에 따라 이견이 있으므로, A. tortuosum이 포함된 추가적인 분자계통학적 유연관계 분석연구 수행을 통해 보다 명확하게 확인할 필요가 있을 것으로 사료된다(Murata et al., 2014).
Pedatisecta절의 경우에는 큰천남성(A. ringens)이 과거 Ringentia절로 분류되었으며, 학자에 따라 Pistillata절로 포함시키거나 Pedatisecta절 내 Pistillata아절로 세부분류하기도 하였고, Ringentiarum ringens로 새로운 속에 포함시키기도 하는 등 분류학적으로 그 위치에 대한 변화가 있었다(Engler, 1920; Nakai, 1950; Ko and Kim, 1985; Gusman and Gusman 2002). 최근 연구에는 세포학적 연구결과와 분자계통학적 연구결과에 의해 점박이천남성, 둥근잎천남성 등과 함께 Pistillata절에 포함시켰다(Murata et al., 2014). 과거 학자에 따라 trnL-trnF spacer 구간을 이용하여 큰천남성만을 Pistilata절에 포함시키기도 하였으나(Jung et al., 2004) 본 연구에서는 Fig. 1-5에서 보는 바와 같이 최근 발표된 논문과 같은 독립된 분계조를 형성하며 둥근잎천남성, 점박이천남성과 함께 유집되어 Pedatisecta절로 처리하는 것을 지지하는 결과를 얻었다(Gusman and Gusman, 2002).
거문천남성의 경우 무늬천남성과 유사하나 화수부속체의 색과 기부의 주름여부를 기준으로 무늬천남성의 아종으로 분류하였으나(Ko et al., 2006), rDNA-ITS, matK 및 rbcL 유전자를 이용하여 분석한 계통수 모두에서 무늬천남성과 하나로 유집되어 나타났다(Fig. 1-5). 이는 두 분류군의 유연관계가 종 이하 분류군이라는 기존의 연구를 지지하는 결과로 두 분류군간의 유전적 변이는 확인되지 않았다(Fig. 1-5). 천남성과 둥근잎천남성의 경우 품종 관계로서 형태상으로 엽연에 거치가 있는 것을 천남성, 거치가 없는 것을 둥근잎천남성으로 분류하였다(Lee 1996; Lee 2003; Lee 2006). 둥근잎천남성은 거치가 있는 것과 없는 것이 모두 있어 현재는 두 종을 따로 구분하지 않고 둥근잎천남성으로 통합하고 있다(Satake et al., 1982; Chang et al., 2014). 본 연구결과 얻어진 rDNA-ITS, matK 및 rbcL 유전자 염기서열을 이용한 계통분석 결과, 둥근잎천남성과 천남성을 따로 구분하지 않는 기존의 분류체계를 지지하였으며 이들의 종내 분류군과 종간 분류군의 유전적 거리 사이에 차이가 없었다. 이를 기준으로 두 종을 통합할 경우 과거 자주큰천남성(A. ringens)과 큰천남성(A. ringens f. praecox)을 구별하여 분류하지 않고 큰천남성(A. ringens)로 통합한 것처럼(Ko et al., 1993), 천남성(A. amurense f. serratum) 역시 둥근잎천남성(A. amurense)으로 처리를 검토해야 할 필요성이 있다(Ko and Kim, 1985; Ko, 2007). 또한 점박이천남성(A. serratum)과 특산종인 섬남성(A. takesimense)의 경우 matK 유전자와 rbcL 유전자 구간에서는 유전자 변이가 없고 rDNA-ITS 부위에서 일부 염기서열 변이가 확인되었으나 종 특이적인 변이가 아닌 개체간 변이로서 계통수에서는 두 분류군이 혼재되어 단계통을 이루었다(Fig. 1-5). 이러한 결과로 보아, 잎의 무늬의 유무로 종을 분류한 섬남성 역시 종의 지위에 대한 재검토가 필요할 것으로 사료된다.
현재 대한민국약전은 약용으로 사용할 수 있는 천남성 종류를 둥근잎천남성, 두루미천남성 및 천남성으로 규정하여 기재하고 있는데, 이중 학명이 A. erubescens (일파산남성)인 중국천남성을 천남성으로 잘못 표기하고 있어, 우리나라에 분포하는 천남성(A. amurense. f. serratum)과 혼동을 주고 있는 실정이다(Korea Institute of Oriental Medicine, 2016). 또한, 분포지역이 넓고 개체수가 많은 점박이천남성이나 큰천남성이 약용으로 혼·오용될 가능성이 매우 높다는 문제점이 있다. 본 연구에서 rDNA-ITS, matK 및 rbcL 염기서열 분석을 통해 이들 약전에 수재된 3종과 다른 천남성 종의 분류학적 특징을 분석한 결과, 속 이하의 분류체계에서 대한민국약전에 수재되어 있는 3종의 천남성이 같은 절에 속하지 않고 각각 다른 절에 속하는 것을 확인하였다(Fig. 1-5). 한방에서 널리 사용되는 한약재 중 하나인 감초(Glycyrrhizae Radix et Rhizoma)의 경우, 약전에 수재되어 있는 종인 감초(Glycyrrhiza uralensis Fischer), 광과감초(光果甘草. Glycyrrhiza glabra Linné) 및 창과감초(脹果甘草. Glycyrrhiza inflata Batal)가 rbcL 염기서열을 이용한 분자계통분석에서 단계통군을 이루며 동속의 다른 종들보다 이들 3종이 가까운 관계에 있는 것으로 나타났는데(Hayashi et al., 2000), 이와 달리 천남성속 식물은 한약재로 이용되는 3종(둥근잎천남성, 두루미천남성, 일파산남성)사이에 뚜렷한 연관성을 찾을 수 없었다(Fig. 1-5). 따라서 대한민국약전에 수재되어 있는 천남성 식물종과 다른 천남성속 식물의 본초학적 약성이론, 종간 성분 비교 분석, 효능비교 등과 연계된 계통분류학적 연구를 통해 대한민국약전에 수재된 한약재 천남성에 대한 기원종의 범위를 재설정할 필요가 있는 것으로 판단된다.
이상의 결과를 종합하면 rDNA-ITS, matK 및 rbcL 염기서열 분석을 통해 국내에는 2절 5분류군의 천남성속 식물이 분포하는 것으로 나타났으며, 둥근잎천남성과 천남성, 무늬천남성과 거문천남성, 그리고 점박이천남성과 섬남성에 대하여 종내 분류군에 대한 재검토가 필요할 것으로 사료된다. 하지만 DNA 바코드 분석을 통한 종 동정이나 계통분류학적 유연관계 분석이 종 이하의 분류군에 적합하지 않다는 기존의 보고를 고려한다면 전체 엽록체게놈 염기서열 분석, 전체 게놈을 이용한 RAPD 분석 및 AFLP 분석과 같은 DNA 지문분석 등을 통해 이들 분류군의 분류학적 위치에 대한 추가 연구가 필요할 것으로 사료된다.
적요
국내에 분포하는 천남성속의 계통학적 유연관계와 한약재 천남성(Arisaematis Rhizoma)으로 사용되는 천남성 3종(둥근잎천남성, 두루미천남성, 일파산남성)에 대한 분류학적 특징을 분석하기 위하여 천남성속 식물에 대한 분자계통학적 연구를 수행하였다. 3개의 범용성 DNA 바코드(ITS, matK, rbcL) 염기서열을 이용하여 국내 분포 천남성속 8분류군과 중국에 분포하는 약전수재 종 1분류군을 포함하는 9종 50개 시료와 같은 과의 Dracunculus vulgaris를 군외군으로 하여 유연관계를 분석하였다. 3개의 개별 DNA 바코드 염기서열과 이들을 유합한 염기서열로 계통학적 유연관계를 분석한 결과, 천남성속의 9 분류군은 6개의 독립적인 분계조를 형성하며 구별되었으며(Clade I, 둥근잎천남성 및 천남성; Clade II, 점박이천남성 및 섬남성; Clade III, 큰천남성; Clade IV, 일파산남성; Clade V, 두루미천남성; Clade VI, 무늬천남성 및 거문천남성), 이들 6개의 분계조는 각각 Pedatisecta절, Sinarisaema절, 및 Tortuosa절로 분류되었다. 또한 이들 DNA 바코드 구간의 비교 결과는 천남성속 식물의 종 및 종 이하 분류 단위의 분류학적 재검토의 필요성에 대한 중요한 정보를 제공하였다. 하지만 대한민국약전에 수재되어 한약재로 사용가능한 3종의 천남성 기원종의 종내 분류학적 연관성이나 분자계통학적 특징은 확인되지 않았다.