서 언
재료 및 방법
느릅나무버섯 공시균주 및 균사체 배양
느릅나무버섯 균사체 추출물 제조
세포배양 및 시료 처리
NO 및 PGE2 생성량 측정
세포생존율 측정
SDS-PAGE 및 Western blot analysis
통계분석
결 과
GIM-EAF의 NO 및 PGE2 생성 억제와 iNOS 및 COX-2 발현 감소 효과
GIM-EAF의 MAPK 및 NF-κB 신호전달 억제 효과
GIM-EAF의 PI3K-Nrf2-HO-1 축 활성화 효과
고 찰
적 요
서 언
염증은 외부의 유해 자극을 제거하고 손상된 조직의 회복을 유도하는 정상적인 생체 방어 반응이다(Lee et al., 2025; Soares et al., 2023). 그러나 이러한 반응이 과도하게 지속되거나 적절히 조절되지 못할 경우 대사증후군, 심혈관계 질환, 자가면역질환 및 다양한 퇴행성 질환의 발생과 진행에 관여하는 것으로 알려져 있다(Chen et al., 2017). 대식세포는 염증 반응의 유도와 증폭에 핵심적인 역할을 하며, inducible nitric oxide synthase (iNOS)와 cyclooxygenase-2 (COX-2)의 발현을 통해 nitric oxide (NO)와 prostaglandin E2 (PGE2) 등의 염증성 매개물질을 생성한다(Vane et al., 1994). 이들 매개물질의 과도하거나 지속적인 생성은 조직 손상과 염증성 병리의 진행을 촉진하므로(He et al., 2020; Je et al., 2021), 활성화된 대식세포에서 NO 및 PGE2 생성과 iNOS 및 COX-2 발현을 효과적으로 억제하는 것은 항염증 소재 개발의 중요한 전략으로 여겨진다.
Lipopolysaccharide (LPS)로 자극된 RAW264.7 대식세포는 항염증 활성을 평가하는 대표적인 in vitro 모델로 널리 사용되고 있다(Lin et al., 2003). 이 모델에서 LPS는 extracellular signal-regulated kinase 1/2 (ERK1/2), p38, c-Jun NH2-terminal kinase (JNK) 등의 mitogen-activated protein kinases (MAPKs)와 nuclear factor kappa B (NF-κB) 신호전달계를 활성화시키며, 그 결과 iNOS, COX-2 및 각종 염증성 사이토카인의 전사적 발현을 증가시킨다(Lai et al., 2011). 따라서 MAPK 및 NF-κB 활성화를 억제하는 것은 천연물 유래 항염증 물질의 대표적인 작용 기전으로 알려져 있다(Azab et al., 2016). 한편, nuclear factor erythroid 2-related factor 2 (Nrf2)/heme oxygenase-1 (HO-1) 축은 강력한 항산화 및 항염증 효과를 매개하는 핵심 신호경로로 주목받고 있으며(Lv et al., 2024; Saha et al., 2025), MAPK/NF-κB 경로를 억제함과 동시에 Nrf2/HO-1 경로를 활성화하는 물질은 보다 효과적인 항염증 보호작용을 나타낼 수 있는 것으로 보고되고 있다(Kaminska, 2005; Liu et al., 2017; Zhang et al., 2021).
현재 임상적으로 널리 사용되는 비스테로이드성 항염증제(non-steroidal anti-inflammatory drugs, NSAIDs)는 cyclooxygenase를 억제하여 prostaglandin 생성을 감소시킴으로써 통증, 발열 및 염증을 빠르게 완화시키는 장점이 있다(Gunaydin and Bilge, 2018). 그러나 장기간 또는 고강도로 사용될 경우 위점막 손상, 소화성 궤양, 위장관 출혈, 신기능 저하 등 심각한 부작용이 동반될 수 있어(Sohail et al., 2023), 만성 염증성 질환 환자에게는 안전성 측면에서 한계가 있다(Saadati et al., 2024). 이에 따라 위장관 및 전신 독성이 상대적으로 낮으면서도 효과적으로 염증 반응을 조절할 수 있는 천연 유래 항염증 소재 발굴의 필요성이 더욱 강조되고 있다(Nakadate et al., 2025).
최근 식용 및 약용 버섯은 기능성 식품 및 천연물 기반 신약 후보물질의 공급원으로서 높은 관심을 받고 있으며, 다양한 생리활성 물질을 함유하여 항염증 효과를 나타내는 것으로 보고되고 있다(Anusiya et al., 2021). 느릅나무버섯(Gloeostereum incarnatum)은 국내 산림자원으로 활용 가능성이 있는 버섯 자원 중 하나이나, 항염증 활성 및 작용기전 연구는 아직 충분히 이루어지지 않았다. 따라서 본 연구에서는 느릅나무버섯 균사체의 항염증 활성을 평가하고 그 분자기전을 규명하고자 하였다. 특히 MAPK/NF-κB 신호전달계 억제 및 PI3K-Nrf2-HO-1 축 활성화 여부를 중심으로 느릅나무버섯 균사체의 항염증 작용 메커니즘을 검토하였다.
재료 및 방법
느릅나무버섯 공시균주 및 균사체 배양
본 연구에 사용한 느릅나무버섯 균주(NIFoS 1949)는 국립산림과학원으로부터 분양받았다. 해당 균주는 2012년 9월 강원도 홍천군 동면 노천리에서 채집한 느릅나무(Ulmus davidiana var. japonica (Rehder) Nakai)로부터 분리되었으며, 산림생물자원보존센터에 보존되어 있었다. 확보한 균주의 동정은 ITS 1 (5′-TAGGTGAACCTGCT-3′) 및 ITS 4 (5′-TCCTCCGCTTATTGATATGC-3′) primer를 이용하여 ITS 영역을 분석한 후, NCBI GenBank DNA database에 등록된 MH992520 (Gloeostereum incarnatum)과 비교하여 확인하였다. YM 배지(Yeast Mold Broth, Difco) 100 mL를 250 mL Erlenmeyer flask에 분주한 후 분양받은 균주(NIFoS 1949)를 접종하고, 25℃ 암조건의 진탕배양기에서 30일간 배양하였다. 배양된 균사체는 homogenizer (IKA T25 digital ULTRA-TURRAX, USA)로 분산시켜 종균으로 사용하였다. 이후 종배양액 100 mL를 2 L Erlenmeyer flask에 담긴 YM 배지 1 L에 접종하고, 25℃에서 30일간 진탕배양하여 균사체를 생산하였다. 배양이 완료된 균사체는 여과를 통해 배지로부터 분리한 후 증류수로 3회 세척하고 동결건조하여 추출 시료로 사용하였다.
느릅나무버섯 균사체 추출물 제조
느릅나무버섯 균사체 분말은 각각 비이커에 넣고 시료 무게의 3배 부피에 해당하는 70% ethanol을 가하여 추출하였다. 초음파 추출기(KODO Co., Ltd., Korea)를 이용하여 1시간씩 총 3회 초음파 추출을 수행하였다. 추출액은 감압농축기(Rotavapor R-114 System, BUCHI, Switzerland)로 농축하여 조추출물을 얻었다. 균사체 조추출물은 증류수에 현탁한 후 separatory funnel을 이용하여 hexane, dichloromethane, ethyl acetate 순으로 순차 분획하였다. 각 유기용매층은 회수하여 감압농축한 뒤 후속 실험에 사용하였다.
세포배양 및 시료 처리
Murine macrophage RAW264.7 세포(American Type Culture Collection, cat. no. TIB-71)는 10% heat-inactivated fetal bovine serum (FBS) 및 1% penicillin/streptomycin이 첨가된 고농도 glucose Dulbecco’s modified Eagle’s medium(DMEM; 4.5 g/L glucose)에서 37℃, 5% CO2 조건의 습윤 배양기에서 배양하였다. 세포는 입수 즉시 증식시켜 master stock으로 동결보존하였고, 약 15 passage 이내의 세포만 실험에 사용하였다. 배양 세포는 정기적으로 형태를 확인하였으며, 매월 mycoplasma 오염 여부를 점검하여 음성으로 확인된 세포만 사용하였다. RAW264.7 세포는 trypsin 처리 없이 cell scraper를 이용하여 회수 및 계대배양하였다. 모든 시료는 dimethyl sulfoxide (DMSO)에 용해한 후 배지로 희석하여 사용하였고, 최종 vehicle 농도는 0.01%(v/v)를 초과하지 않도록 하였으며, 모든 처리군에서 동일하게 유지하였다.
NO 및 PGE2 생성량 측정
RAW264.7 세포를 12-well plate에 well당 2.0-3.0 × 105 cells/well가 되도록 분주하고, 하룻밤 동안 부착시켰다. 다음날 시료가 포함된 새로운 DMEM 배지로 교체한 후 2시간 전처리하고, LPS (1 ㎍/mL)를 처리하여 24시간 자극하였다. 배양 상등액은 회수 후 원심분리(10,000 × g, 5 min, 4℃)하여 불순물을 제거하고 즉시 NO 및 PGE2 분석에 사용하였다. NO 생성량은 Griess 반응을 이용하여 측정하였다. 세포배양 상등액과 Griess reagent를 동일 부피로 혼합하여 96-well plate에 분주한 후, 암실에서 실온 10분간 반응시켰다. 이후 540 ㎚에서 UV/visible spectrophotometer (SpectraMax M2, Molecular Devices, San Jose, CA, USA)로 흡광도를 측정하였다. PGE2 함량은 동일한 상등액을 사용하여 Prostaglandin E2 ELISA Kit (Cayman Chemical, Ann Arbor, MI, USA)를 제조사의 지침에 따라 정량하였다.
세포생존율 측정
세포생존율은 MTT assay를 이용하여 평가하였다. RAW264.7 세포를 96-well plate에 well당 1.0-2.0 × 104 cells/well가 되도록 분주하고 하룻밤 동안 부착시켰다. 이후 시료가 포함된 새로운 배지로 교체하여 24시간 배양하였다. MTT stock solution (5 ㎎/mL in PBS)을 배지에 희석하여 well 내 최종농도가 0.5 ㎎/mL가 되도록 처리하고, 37℃ 암조건에서 4시간 반응시켜 formazan 결정을 형성시켰다. 상등액을 제거한 뒤 각 well에 DMSO 100 μL를 가하여 결정을 용해시키고, 실온에서 10분간 진탕한 후 570 ㎚에서 흡광도를 측정하였다.
SDS-PAGE 및 Western blot analysis
세포는 ice-cold PBS로 2회 세척한 후, protease inhibitor cocktail 및 phosphatase inhibitors (Sigma-Aldrich, St. Louis, MO, USA)가 첨가된 RIPA buffer (Thermo Fisher Scientific, Waltham, MA, USA)로 ice 상에서 용해하였다. 세포 용해액은 원심분리(14,000 × g, 10 min, 4℃)하여 상등액을 회수하였고, 단백질 정량은 Pierce™ BCA Protein Assay Kit (Thermo Fisher Scientific, Waltham, MA, USA)를 사용하여 수행하였다. 동일한 양의 단백질(30 ㎍/well)은 5 × SDS sample buffer와 혼합하여 95℃에서 5분간 가열한 후, 12% SDS-polyacrylamide gel에서 전기영동하였다. 분리된 단백질은 wet transfer 방식(100 V, 120 min, 4℃)으로 nitrocellulose membrane에 전이하였다. Membrane은 5% non-fat milk가 포함된 TBST에서 실온 1시간 blocking한 후, 1차 항체와 함께 4℃에서 overnight 반응시켰다. 이후 TBST로 10분씩 3회 세척한 다음, HRP-conjugated 2차 항체와 실온에서 1시간 반응시켰다. 다시 세척한 후 ECL Select Western Blotting Detection Reagent (Cytiva, Wilmington, DE, USA)로 발색하고, LI-COR C-DiGit Blot Scanner (LI-COR Biosciences, Lincoln, NE, USA)를 이용하여 이미지를 획득하였다. 밴드의 정량분석은 UN-SCAN-IT gel analysis software version 5.1 (Silk Scientific Inc., Vineyard, UT, USA)을 이용하였다. 인산화 단백질은 해당 total protein으로 먼저 정규화한 후 loading control로 보정하였고, 비인산화 단백질은 loading control에 직접 정규화하였다.
통계분석
모든 실험은 최소 3회 반복하여 수행되었다. 통계 분석은 GraphPad Prism 버전 5.0 (GraphPad Software, Inc.)을 사용하여 수행하였으며, 데이터는 평균 ± 표준편차로 표시하였다. 데이터 분석은 일원배치분산분석(one-way ANOVA)을 수행한 후 Bonferroni 사후 검정을 통해 진행하였다. P<0.05는 통계적으로 유의한 차이를 나타내는 기준으로 간주하였다.
결 과
GIM-EAF의 NO 및 PGE2 생성 억제와 iNOS 및 COX-2 발현 감소 효과
활성 분획을 규명하기 위하여 느릅나무버섯 균사체(Gloeostereum incarnatum) 균사체의 70% ethanol 조추출물을 n-hexane, dichloromethane 및 ethyl acetate로 순차 분획한 후, 각 분획의 LPS 유도 NO 생성 억제 효과를 비교하였다(Fig. 1A). LPS 처리군은 CON 대비 약 7.95배의 NO 생성 증가를 나타내었고, 조추출물(CE)과 n-hexane 분획(HEF)은 각각 6.28배 및 6.87배 수준으로 중등도의 억제 효과를 보였다. Dichloromethane 분획(DCMF)은 NO 생성량을 CON 대비 4.69배 수준까지 감소시켜 보다 강한 억제 활성을 나타내었다. 특히 ethyl acetate 분획(EAF)은 NO 생성량을 CON 대비 2.49배 수준으로 낮추어 가장 우수한 항염증 활성을 보였다. 따라서 이후 기전 연구에는 EAF를 선택하였으며, 이를 GIM-EAF (Gloeostereum incarnatum mycelial ethyl acetate fraction)으로 명명하였다. Fig. 1A의 분획 비교 결과를 바탕으로 가장 우수한 활성을 나타낸 GIM-EAF를 대상으로 농도 의존적 항염증 효과를 평가하였다. 먼저 NO 생성량을 측정한 결과(Fig. 1B), LPS 단독 처리군은 CON 대비 약 9.18배 증가한 반면, GIM-EAF를 25, 50 및 100 ㎍/mL 농도로 처리한 군에서는 각각 약 4.39배, 1.53배 및 1.03배 수준으로 감소하여 뚜렷한 농도 의존적 억제 효과를 나타내었다. PGE2 생성량 또한 유사한 경향을 보였다(Fig. 1C). LPS 처리군은 CON 대비 약 4.29배 증가하였으나 GIM-EAF 25, 50 및 100 ㎍/mL 처리군에서는 각각 약 2.95배, 2.03배 및 1.19배 수준으로 감소하였다. 이어서 Western blot analysis를 통해 NO 및 PGE2 생성의 주요 효소인 iNOS와 COX-2의 단백질 발현을 확인한 결과(Fig. 1D), LPS 처리군에서 iNOS와 COX-2 발현이 각각 약 3.70배 및 4.67배 증가한 반면, GIM-EAF 25 ㎍/mL 처리군에서는 각각 약 1.99배 및 2.68배, 50 ㎍/mL 처리군에서는 약 1.13배 및 1.39배 수준까지 감소하였다. 이는 GIM-EAF가 염증성 매개물질의 생성 자체뿐 아니라 그 생성에 관여하는 효소 단백질의 발현도 효과적으로 억제함을 의미한다. 한편 MTT assay 결과(Fig. 1E), GIM-EAF 25–100 ㎍/mL 농도 범위에서는 RAW264.7 세포의 생존율에 유의적인 변화가 나타나지 않았다. 따라서 GIM-EAF의 항염증 효과는 세포독성에 기인한 비특이적 결과가 아니라 염증 반응 조절에 의한 특이적인 효과임을 확인하였다.
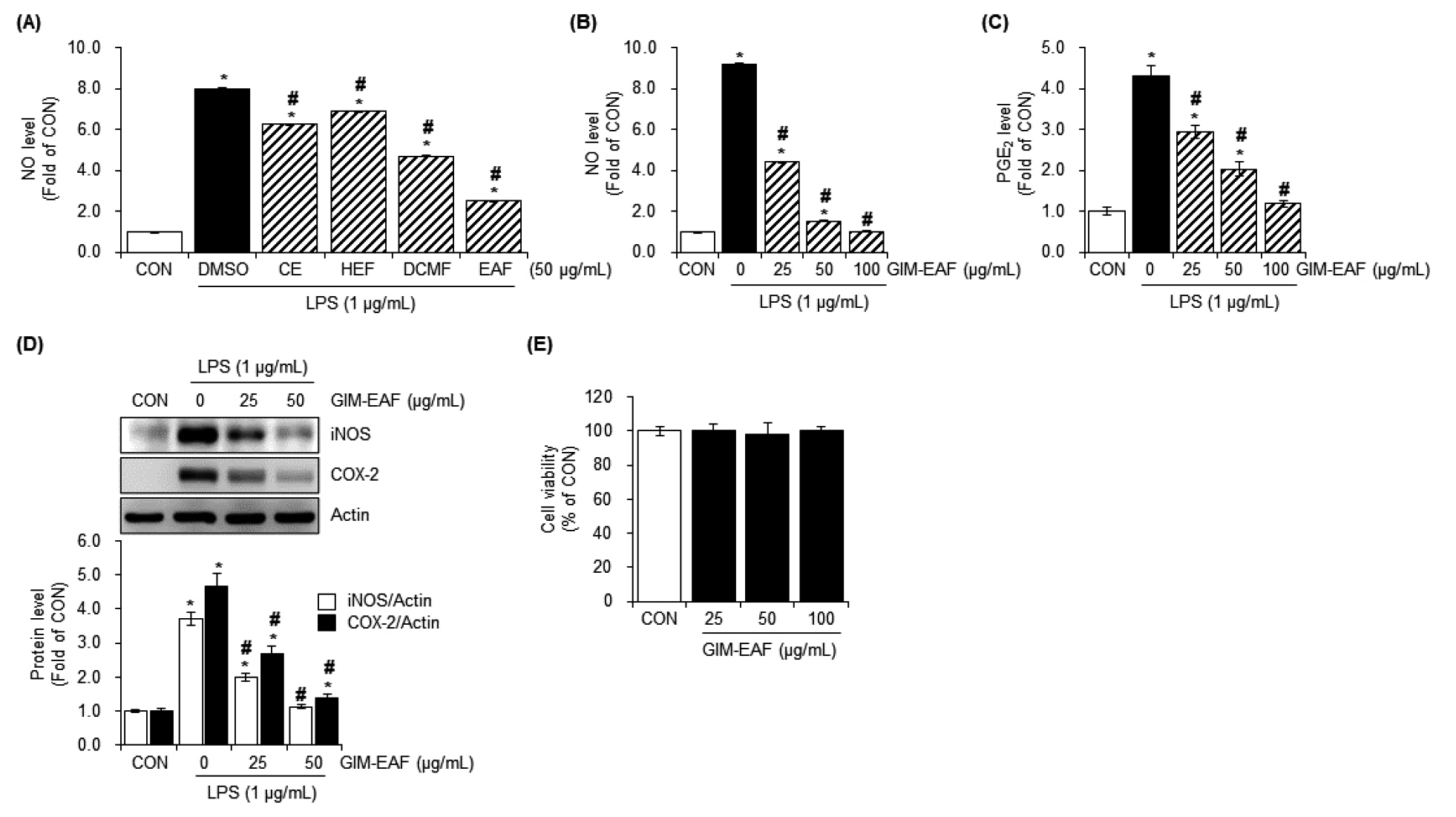
Fig. 1.
GIM-EAF suppresses LPS-induced NO/PGE₂ production and iNOS/COX-2 expression without cytotoxicity in RAW264.7 macrophages. (A) The 70% ethanolic extract of G. incarnatum mycelia was sequentially fractionated with n-hexane (HEF), dichloromethane (DCMF), and ethyl acetate (EAF), and the inhibitory effects of each fraction on LPS-induced NO production were evaluated. RAW264.7 cells were pretreated with each fraction (50 ㎍/mL) for 2 h, followed by stimulation with LPS (1 ㎍/mL) for 24 h. NO levels in the culture supernatants were determined using the Griess assay. (B) Dose-dependent inhibition of NO production by GIM-EAF. RAW264.7 cells were pretreated with GIM-EAF (25, 50 and 100 ㎍/mL) for 2 h and then stimulated with LPS (1 ㎍/mL) for 24 h. NO in culture supernatants was quantified (Griess assay). (C) Dose-dependent reduction of PGE₂under the same treatment conditions as in (A); PGE₂ levels in supernatants were measured using Prostaglandin E2 ELISA Kit. (D) Western blot analysis of iNOS and COX-2 after LPS stimulation with/without GIM-EAF (25 and 50 ㎍/mL). (E) RAW264.7 cells were treated with GIM-EAF (25, 50 and 100 ㎍/mL) without LPS for 24 h. Cell viability assessed by MTT following exposure to GIM-EAF (25-100 ㎍/mL). *p < 0.05 versus untreated control (CON) and #p < 0.05 versus LPS-treated group.
GIM-EAF의 MAPK 및 NF-κB 신호전달 억제 효과
GIM-EAF가 NO 및 PGE2 생성과 iNOS 및 COX-2 발현을 억제하는 기전을 규명하기 위하여, 이들 유전자의 상위 조절 신호로 알려진 MAPK 및 NF-κB 경로를 분석하였다. 먼저 MAPK 경로에서 ERK1/2, p38, JNK 및 이들의 하위 전사조절인자인 ATF2의 인산화 수준을 확인한 결과(Fig. 2A), LPS 처리군은 CON에 비해 모든 단백질의 인산화를 현저하게 증가시켜 MAPK 신호전달계가 활성화되었음을 보여주었다. 이에 반해 GIM-EAF를 함께 처리한 군에서는 ERK1/2, p38, JNK 및 ATF2의 인산화가 농도 의존적으로 감소하였다. 또한 NF-κB 경로의 핵심 구성인자인 p65의 인산화 수준을 측정한 결과(Fig. 2B), LPS 처리에 의해 p65 인산화가 뚜렷하게 증가하였으나, GIM-EAF 처리에 의해 농도 의존적으로 감소하였다. 이러한 결과는 GIM-EAF가 MAPK 및 NF-κB의 대표적인 염증성 신호전달 경로를 동시에 억제함으로써 iNOS 및 COX-2 발현 저하와 NO 및 PGE2 생성 억제를 유도하는 것으로 해석된다.
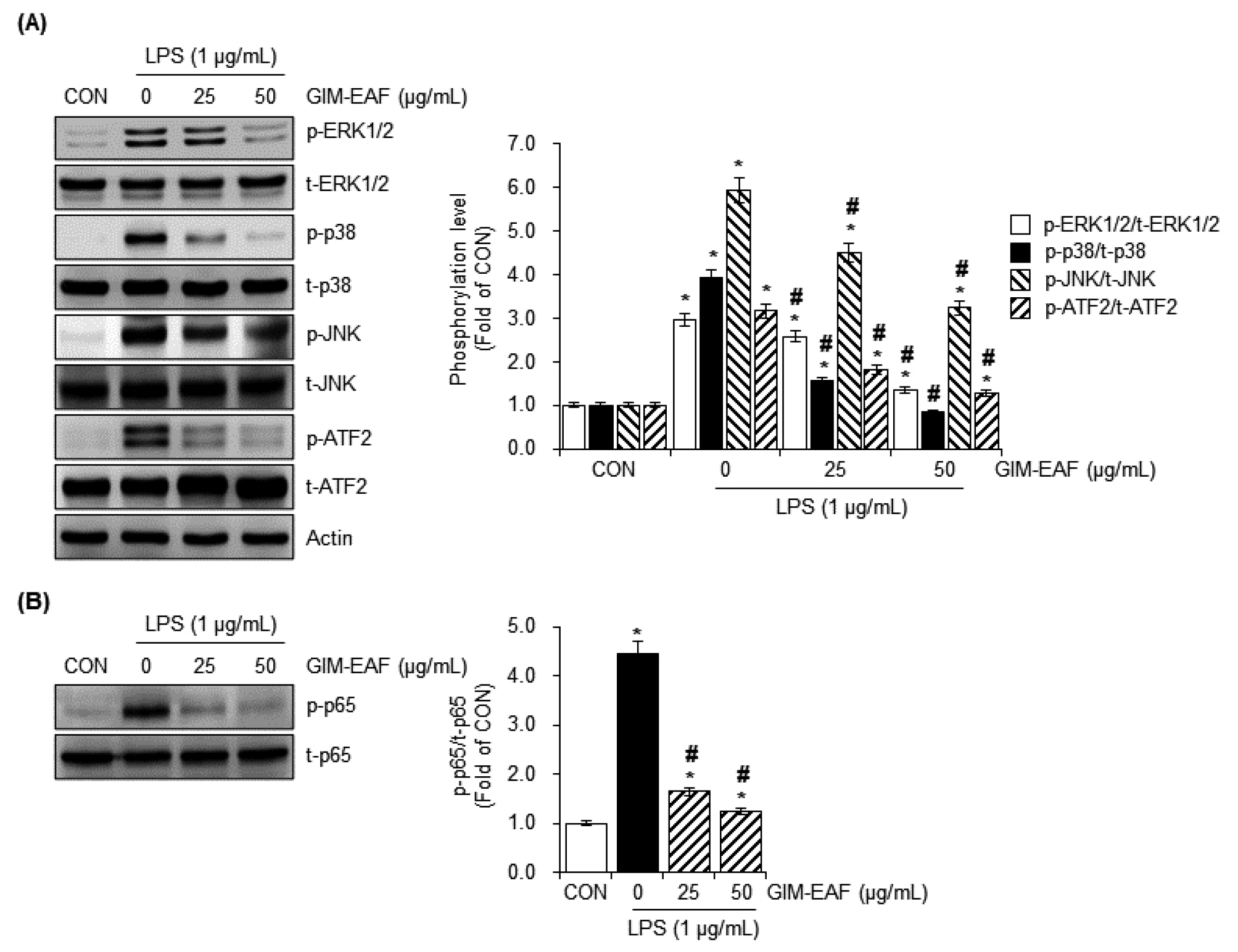
Fig. 2.
GIM-EAF inhibits LPS-activated MAPK and NF-κB signaling in RAW264.7 macrophages. (A) RAW264.7 cells were pretreated with GIM-EAF (25 and 50 ㎍/mL) for 2 h and then stimulated with LPS (1 ㎍/mL) for 30 min. The phosphorylation levels of ERK1/2, p38, JNK, and ATF2 were investigated using Western blot analysis. (B) RAW264.7 cells were pretreated with GIM-EAF (25 and 50 ㎍/mL) for 2 h and then stimulated with LPS (1 ㎍/mL) for 30 min. The phosphorylation level of p65 was investigated using Western blot analysis. *p < 0.05 versus untreated control (CON) and #p < 0.05 versus LPS-treated group.
GIM-EAF의 PI3K-Nrf2-HO-1 축 활성화 효과
GIM-EAF가 염증성 신호 억제뿐 아니라 세포 보호성 신호전달 경로를 활성화하는지 확인하기 위해 PI3K-Nrf2-HO-1 축을 분석하였다. 먼저 GIM-EAF 처리 시 Nrf2 및 HO-1 단백질 발현이 농도 의존적으로 증가하는 것이 확인되었다(Fig. 3A). 시간 경과에 따른 변화를 조사한 결과(Fig. 3B), Nrf2 단백질의 축적은 처리 후 1시간부터 관찰되었으며, HO-1 발현 증가는 3시간 이후부터 뚜렷하게 나타났다. 이는 Nrf2 활성화 이후 HO-1이 후속적으로 유도되는 전형적인 양상과 일치한다. 이러한 경로 활성화에 PI3K가 관여하는지를 확인하기 위하여 PI3K inhibitor인 LY294002를 사용하였다(Fig. 3C). LY294002가 없는 조건에서는 GIM-EAF 처리에 의해 Nrf2 및 HO-1 발현이 뚜렷하게 증가하였으나 LY294002 존재 하에서는 이러한 유도가 현저히 감소하였다. 또한 GIM-EAF 처리 후 1시간부터 PI3K 인산화가 유도되는 것이 확인되었다(Fig. 3D). 종합하면, GIM-EAF는 PI3K를 활성화시키고, 이를 통해 초기 Nrf2 안정화 및 후속적인 HO-1 발현 유도를 촉진하는 것으로 판단된다.
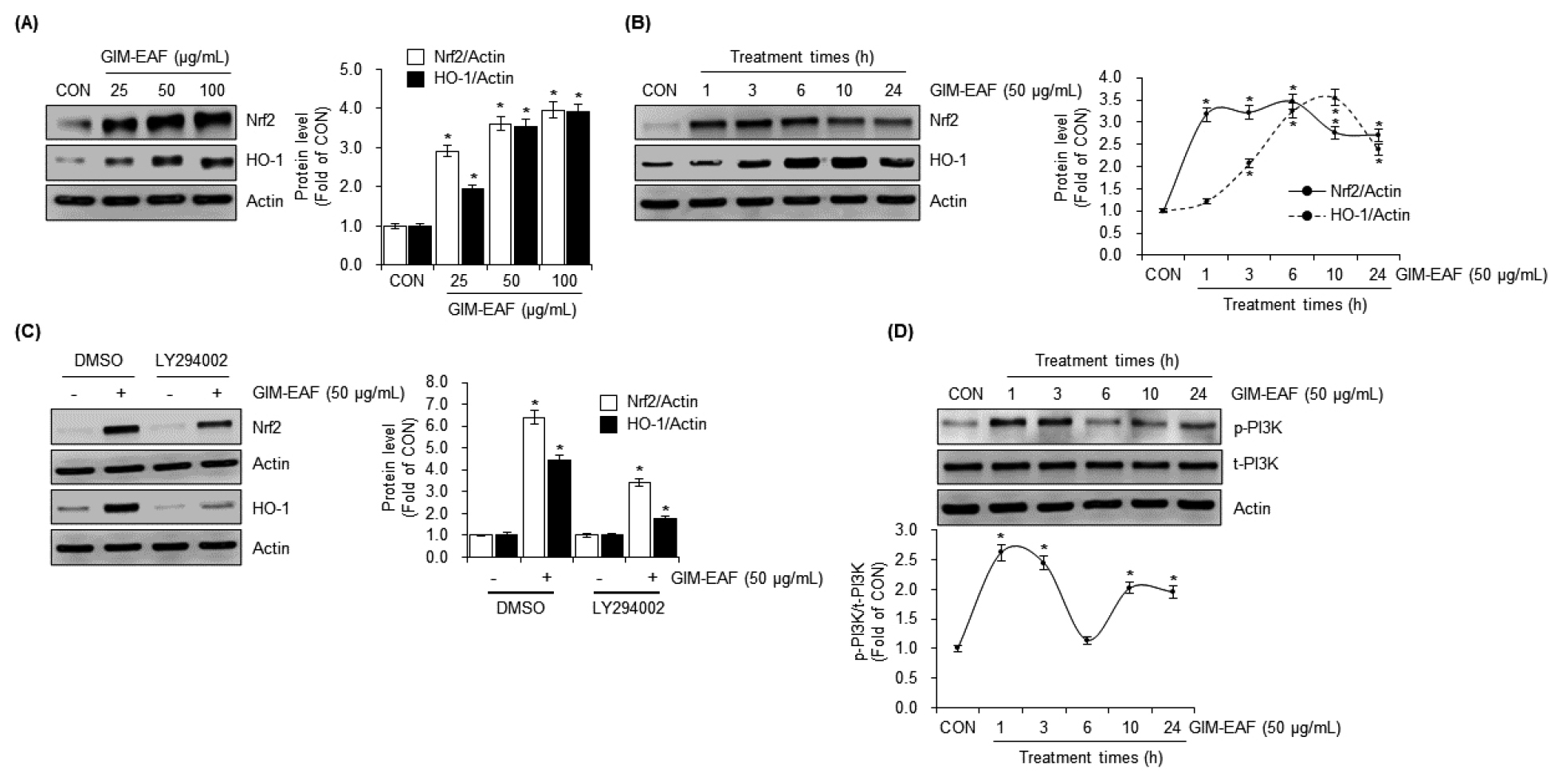
Fig. 3.
GIM-EAF activates the PI3K-Nrf2-HO-1 cytoprotective axis in RAW264.7 macrophages. (A) RAW264.7 cells were treated with GIM-EAF (25, 50, 100 ㎍/mL) for 24 h, and then the protein levels of Nrf2 and HO-1 were investigated using Western blot analysis. (B) RAW264.7 cells were treated with GIM-EAF (50 ㎍/mL) for 1, 3, 6, 10, or 24 h, and then the protein levels of Nrf2 and HO-1 were investigated using Western blot analysis. (C) RAW264.7 cells were pretreated with LY294002 (20 µM) for 2 h, and then co-treated with GIM-EAF (50 ㎍/mL) for 1 h (Nrf2 analysis) or 6 h (HO-1 analysis), and then the protein levels of Nrf2 and HO-1 were investigated using Western blot analysis. (D) RAW264.7 cells were treated with GIM-EAF (50 ㎍/mL) for 1, 3, 6, 10, or 24 h, and then the protein levels of p-PI3K and t-PI3K were investigated using Western blot analysis. *p < 0.05 versus untreated control (CON).
고 찰
본 연구는 느릅나무버섯 균사체의 ethyl acetate 분획인 GIM-EAF가 LPS로 자극된 RAW264.7 대식세포에서 강한 항염증 활성을 나타냄을 보여준다. 특히 GIM-EAF는 조추출물 및 다른 용매 분획들에 비해 가장 우수한 NO 억제 활성을 나타냈으며, 이후 농도 의존적으로 NO와 PGE2 생성을 감소시키고, 이들 염증성 매개체의 생성에 직접 관여하는 iNOS 및 COX-2 단백질 발현을 유의적으로 억제하였다. 대식세포에서 LPS는 TLR4를 통해 선천면역 반응을 활성화하고, 그 결과 iNOS와 COX-2 발현이 유도되어 각각 NO와 PGE2 생성이 증가하는 것으로 잘 알려져 있다(Akira and Takeda, 2004; Kim et al., 2007; MacMicking et al., 1997). 따라서 본 연구에서 관찰된 GIM-EAF의 효과는 단순한 분비 억제가 아니라, 염증성 매개체 생성의 상위 조절단계를 제어한 결과로 해석될 수 있다. 또한 실험 농도 범위에서 세포독성이 관찰되지 않았다는 점은, 이러한 억제 효과가 비특이적 세포 손상에 의한 것이 아니라 염증 반응 조절에 기인한 특이적 작용임을 뒷받침한다.
본 연구의 또 다른 중요한 의의는 GIM-EAF의 항염증 효과가 MAPK 및 NF-κB 신호전달 억제와 긴밀히 연결되어 있다는 점이다. LPS 자극에 의해 ERK1/2, p38, JNK 및 ATF2의 인산화가 증가하고, 동시에 NF-κB p65의 인산화가 촉진되는 것은 전형적인 염증 반응 양상이다. 본 연구에서 GIM-EAF는 이러한 MAPK 구성요소들과 p65의 인산화를 모두 농도 의존적으로 억제하였다. 이는 GIM-EAF가 단일 말단 표적이 아니라, 염증 반응의 핵심 상위 신호망을 동시에 조절함으로써 iNOS 및 COX-2 발현 저하를 유도했음을 시사한다. 실제로 RAW264.7 세포에서 NF-κB 비활성화는 iNOS와 COX-2 발현 감소와 직접 연결되며, MAPK 억제 역시 염증성 유전자 전사를 약화시키는 주요 기전으로 보고되어 있다(Kim et al., 2007). 따라서 본 연구 결과는 GIM-EAF의 NO 및 PGE2 억제 효과가 MAPK–NF-κB 축 차단에 의해 매개된다는 해석을 강하게 지지한다.
한편, GIM-EAF의 작용은 단순히 염증성 신호를 억누르는 데 그치지 않고, 세포 보호성 항산화 경로인 PI3K-Nrf2-HO-1 축을 활성화한다는 점에서 더욱 의미가 크다. Nrf2는 산화·염증 스트레스에 대응하는 대표적 전사인자로서, 활성화되면 HO-1을 포함한 다양한 세포보호 유전자의 발현을 유도한다(Wang et al., 2010). 본 연구에서 GIM-EAF 처리 후 Nrf2 단백질 축적이 1시간부터 관찰되고, 이후 3시간부터 HO-1 발현이 증가한 것은 Nrf2 활성화가 선행되고 HO-1 유도가 뒤따르는 전형적 시간적 순서와 일치한다. 또한 PI3K inhibitor인 LY294002가 GIM-EAF에 의한 Nrf2 및 HO-1 유도를 현저히 약화시켰고, PI3K 인산화 역시 초기부터 증가하였으므로 GIM-EAF는 PI3K 활성화를 매개로 Nrf2 안정화 및 HO-1 발현을 촉진하는 것으로 판단된다. 이러한 결과는 PI3K/Akt 신호가 Nrf2/HO-1 활성의 상위 조절자로 작동한다는 기존 보고들과 잘 부합한다.
Nrf2/HO-1 경로의 활성화는 본 연구에서 관찰된 항염증 효과를 설명하는 중요한 보완 기전으로 볼 수 있다. 선행연구들에 따르면 HO-1 유도는 NO, PGE2, iNOS, COX-2 및 염증성 cytokine 생성을 억제하는 방향으로 작용하며, 이러한 효과는 때로 NF-κB 억제와도 기능적으로 연결된다. 예를 들어 sulfuretin, brazilin 및 chitosan oligosaccharides들은 RAW264.7 대식세포에서 Nrf2/HO-1을 유도함으로써 염증성 매개체 생성을 감소시킨 바 있다(Hu et al., 2009; Hyung et al., 2016; Lee et al., 2010). 따라서 GIM-EAF는 MAPK/NF-κB 억제를 통한 염증 신호 차단과 동시에 PI3K–Nrf2–HO-1 활성화를 통한 세포 보호 반응 유도라는 이중 기전을 통해 항염증 활성을 발휘하는 것으로 해석된다. 이는 염증 조절 물질로서 GIM-EAF의 생리활성이 단순 억제제가 아니라, 염증-산화 스트레스 균형을 재조정하는 복합적 조절자일 가능성을 시사한다
느릅나무버섯 자체의 생리활성과 관련해서도 본 결과는 의미가 있다. 선행연구에서는 느릅나무버섯이 Nrf2/NF-κB 조절을 통해 DSS 유도 궤양성 대장염을 완화할 수 있음이 보고되었고, 이 버섯이 다양한 생리활성 저분자 화합물을 생산하는 것으로 알려져 있다(Li et al., 2020). 또한 느릅나무버섯에서는 hirsutanol A 및 hirsutanol C와 같은 sesquiterpene 계열 대사체가 보고된 바 있는데, 이러한 화합물들은 일반적으로 ethyl acetate와 같은 중간 극성 유기용매 분획에서 농축될 가능성이 있다(Asai et al., 2011). 따라서 본 연구에서 EAF가 다른 분획보다 우수한 활성을 나타낸 것은 GIM-EAF 내에 이러한 중간 극성의 저분자 활성 성분들이 상대적으로 풍부하게 존재할 가능성을 시사한다. 다만 현재 결과만으로 특정 활성 성분을 단정할 수는 없으므로, 향후 LC-MS/MS 기반 성분 분석 및 bioassay-guided isolation을 통해 실제 유효물질을 규명할 필요가 있다. 이 부분은 본 연구의 중요한 후속 과제이다.
본 연구에는 몇 가지 한계도 존재한다. 첫째, 본 연구는 RAW264.7 세포 기반의 in vitro 결과이므로, GIM-EAF의 항염증 효능이 실제 조직 또는 동물 수준에서도 동일하게 재현되는지는 추가 검증이 필요하다. 둘째, LY294002를 이용하여 PI3K가 Nrf2/HO-1 유도의 상위 조절자임을 제시하였으나 Nrf2 또는 HO-1 자체가 GIM-EAF의 NO/PGE2 억제 효과에 필수적인지에 대해서는 직접적인 기능 억제 실험이 수행되지 않았다. 따라서 향후에는 Nrf2 knockdown, HO-1 inhibitor(SnPP 또는 ZnPP) 또는 유전자 발현 분석을 병행하여, PI3K–Nrf2–HO-1 축이 실제 항염증 효과에 어느 정도 기여하는지 보다 인과적으로 규명할 필요가 있다. 셋째, 본 연구는 단백질 수준의 변화를 중심으로 분석하였으므로, iNOS, COX-2, HO-1 및 관련 cytokine들의 전사 수준까지 확장하면 기전적 완성도가 더욱 높아질 것이다.
종합하면, GIM-EAF는 LPS로 활성화된 대식세포에서 iNOS/COX-2 발현과 NO/PGE2 생성을 억제하고, 그 기전으로 MAPK 및 NF-κB 신호전달 억제와 PI3K–Nrf2–HO-1 축 활성화를 동시에 유도하는 것으로 나타났다. 이러한 결과는 GIM-EAF가 염증성 신호 억제와 세포 보호성 항산화 반응 유도를 함께 매개하는 다중표적 항염증 소재임을 보여주며, 향후 활성 성분 규명과 in vivo 효능 검증이 이루어진다면 기능성 식품 또는 천연물 기반 항염증 후보물질로서 활용 가능성이 높을 것으로 판단된다.
적 요
본 연구는 느릅나무버섯(Gloeostereum incarnatum) 균사체 유래 ethyl acetate 분획물(GIM-EAF)의 항염증 활성을 확인하고 그 작용기전을 규명하고자 수행되었다. 느릅나무버섯 균사체의 70% ethanol 조추출물을 n-hexane, dichloromethane 및 ethyl acetate로 순차 분획한 후, LPS로 자극한 RAW264.7 대식세포에서 NO 생성 억제 활성을 비교한 결과, ethyl acetate 분획이 가장 우수한 활성을 나타내어 GIM-EAF로 명명하였다. GIM-EAF는 NO 및 PGE2 생성을 농도 의존적으로 억제하였으며, 이에 상응하여 iNOS와 COX-2의 단백질 발현도 감소시켰다. 반면 동일 농도 범위에서 세포독성은 관찰되지 않았다. 기전 분석 결과, GIM-EAF는 LPS에 의해 유도된 ERK1/2, p38, JNK, ATF2 및 NF-κB p65의 인산화를 억제하여 MAPK 및 NF-κB 신호전달 경로를 효과적으로 차단하였다. 또한 GIM-EAF는 PI3K의 인산화를 유도하고, 이에 따라 Nrf2의 축적과 HO-1의 발현을 증가시켰다. PI3K inhibitor인 LY294002는 GIM-EAF에 의한 Nrf2 및 HO-1 발현 유도를 현저히 억제하여 PI3K가 해당 경로의 상위 조절자로 작용함을 시사하였다. 이상의 결과는 GIM-EAF가 LPS로 활성화된 RAW264.7 세포에서 MAPK 및 NF-κB 신호전달을 억제하는 동시에 PI3K-Nrf2-HO-1 축을 활성화함으로써 염증성 매개물질의 생성과 관련 효소 발현을 효과적으로 조절함을 보여준다. 따라서 GIM-EAF는 항염증 기능성 소재 또는 천연물 유래 항염증 후보물질로서 활용 가능성이 있는 것으로 판단된다.




