서 언
재료 및 방법
실험재료
추출물 조제
세포배양 및 MTT assay
Nitric oxide (NO) assay
ELISA (PGE2, TNF-α and IL-6) 측정
Western blot 분석을 통한 MAPK 발현 측정
통계 처리
결과 및 고찰
RAW264.7 대식세포 생존율
NO와 PGE2 생성에 미치는 영향
전 염증성 사이토카인(pro-inflammatory cytokines)의 생성에 미치는 영향
Mitogen activated protein kinases (MPAKs) 신호전달 경로에 미치는 영향
적 요
서 언
지칭개(Hemistepta lyrata Bunge)는 강과 야지에서 쉽게 볼 수 있는 되는 두해살이풀이다. 동남아시아, 오스트레일리아, 인도, 일본, 중국 등에 분포하며, 우리나라 전역에 나고 있다. 지칭개의 줄기는 최대 0.8 m까지 자라며, 곧게 자라난다. 꽃은 붉은 보라색 또는 분홍색을 띄며 5 ~ 7월에 핀다(Gao et al., 2009; Lin and Shi, 1987). 지칭개는 암, 염증, 출혈, 치질, 발열의 치료제로 민간요법에 사용되었고, 잎과 새순은 기근식품으로 사용되었다(Kim, 2015). 지칭개에서 분리된 화합물로는 lignans, flavonoids, sesquiterpene lactones 등이 있다고 보고되어있다(Dong et al., 2010; Ha et al., 2003; Huang et al., 1991; Ren and Yang, 2001; Zou et al., 2006). Kim et al. (2019)의 보고에 따르면 지칭개 전초 클로로포름 추출물이 염증효과가 있음을 알 수 있었으나 지칭개 지상부 에탄올 추출물에 대한 보고는 없었다. 본 연구에서는 기근식품으로 사용된 잎이 포함되는 지칭개 지상부를 에탄올로 추출하여 mitogen-activated protein kinase (MAPK) 신호경로에 미치는 영향에 대한 연구를 진행하였다.
염증은 유해한 물리적 또는 화학적 자극에 의해 활성화되는 방어기작이다(Cho et al., 2009; Kim et al., 2013). 그러나 과도한 염증반응은 관절염 또는 다발성 경화증, 암과 같은 질병과 관련된 만성 상태로 발전한다.(Guzik et al., 2003; Nathan, 2002). 대부분의 과도한 염증반응은 전 염증성 사이토카인[tumor necrosis factor α (TNF-α)와 interleukin-6 (IL-6)]과 염증 매개체[reactive oxygen species (ROS), nitric oxide (NO), 및 prostaglandin E2 (PGE2)]를 생성하는 염증성 세포를 활성화 시킨다(Cho et al., 2009; Kim et al., 2017). 과도한 염증반응은 각종 질병을 악화시키게 된다(Kim and Kang, 2019). NO의 과잉생성은 숙주에 유해하고, 심각한 자가 면역질환을 일으킬 수 있다(Guzik et al., 2003). NO의 생성은 iNOS 단백질에 의해 조절되고, PGE2는 COX-2 단백질의 발현에 의해 합성된다. iNOS와 COX-2에 의해 생성된 NO와 PGE2는 널리 알려진 염증 매개체로 염증반응 정도를 판단하는 척도로 이용되고 있고(Lee et al., 2019), TNF-α와 IL-6는 염증성 사이토카인으로 알려져 있고, 이와 같은 유전자들을 발현시킴으로써 염증반응이 일어난다(Lee, 2011; Lee and Kang, 2018).
Lipopolysaccharide (LPS)는 대표적인 염증 유도 물질로 알려져 있고, 세균으로부터 유래된 내독소(endotoxin)다(Akira and Takeda, 2004; Lee et al ., 2019). 대표적인 패턴 인식 수용체(pattern recognition receptor)인 toll-like receptor 4(TLR4)에 의해 인식된 LPS는 MAPK라는 세포 내 주요 신호전달 경로를 인산화에 의해 활성화시켜 염증을 유발 시킨다(Anderson and Borlak, 2008; Cheng et al., 2014). TLR4는 대식세포 활성을 증가시키기 위해 염증성 사이토카인(TNF-α, IL-6, iNOS)에 의한 MAPK 활성을 증가시킨다고 보고된 바 있다(Nyati et al., 2017). 또한, LPS로 유도된 iNOS 발현과 관련된 MAPK 활성화는 RAW 264.7 대식세포에서 p38, ERK, 및 JNK의 발현을 조절한다고 보고되었다(Chan and Riches, 2001). MAPK를 통해 발생되는 염증성 질환은 복잡하고 새로운 치료제를 발굴하기 위해서는 연구가 필요하다.
본 연구에서는 약용 식물의 항염증 잠재력을 평가하기 위한 지속적인 검사 프로그램의 일환으로써, 우리는 지칭개 지상부의 항염증제 특성과 LPS를 처리한 RAW 264.7 대식세포에서 기본 분자 메커니즘에 대해 연구하였다. 우리는 지칭개가 MAPK 신호전달 경로, 염증 매개체(inflammatory mediators) 및 전 염증성 사이토카인(pro-inflammatory cytokine)에 어떠한 영향을 미치는지 조사하여 유의적인 결과를 얻었기에 이를 보고하는 바이다.
재료 및 방법
실험재료
Lipopolysaccharide (LPS), thiazoly blue tetrazolium bromide (MTT), sulfanilamide, phosphoric acid, N-(1-naphthyl)ethylene diamine dihydrochloride 등은 Sigma (St. Louis, MO, USA)에서 구입하여 사용하였다. JNK, phospho (P)-JNK, ERK, P-ERK, p38, P-p38 항체(Goat anti-rabbit antibodies)는 Cell Signaling (Beverly, MA, USA)에서 구입하여 사용하였으며, Dulbecco’s modified Eagle’s medium (DMEM)와 fetal bovine serum (FBS)는 GIBCO (Gaithersburg, MD, USA)에서 구입하여 사용하였으며, Phosphate buffered saline (PBS)는 WeLGENE Inc. (Daegu, Republic of Korea)에서 구입하여 사용하였다. 다른 시약들은 Sigma grade로 구입하여 사용하였다.
추출물 조제
본 실험에 사용한 지칭개(H. lyrata) 시료는 경북 문경시 농암면 화산리(2016년 5월)에서 인식형질이 있는 개체를 직접 채집하여 건조 파쇄하였으며, 본 표본은 국립낙동강생물자원관 수장고에 보관하고 있다(NNIBRVP59997). 식물의 동정은 ‘Korea Biodiversity Information System’에 의거하여 분류를 실시하였다(국가생물종지식정보시스템-Korea Biodiversity Information System, 2014). 지칭개 지상부 에탄올 추출물을 조제하기 위해 건조 분말을 10배 중량의 70% 에탄올로 실온에서 24시간 동안 추출하였다. 에탄올 추출물을 여과지(Whatman No. 2, Advantec Co., Japan)로 여과한 후 용매를 Rotary evaporator (Tokyo Rikakikai Co., Tokyo, Japan)를 이용하여 제거하였고, 동결건조(Ilshin, Korea)를 거쳐 건조중량 대비 9.6%의 분말 시료를 얻었다. 이후 에탄올 추출시료는 dimethyl sulfoxide (DMSO)에 25 ㎎/mL의 농도로 녹여 –20℃에서 보관하였으며, 실험에 따라 적절하게 희석하여 사용하였다.
세포배양 및 MTT assay
RAW264.7 대식세포는 10% fetal bovine serum (FBS)가 함유된 DMEM 배지(Gaithersburg, MD, USA)를 이용하여 37℃, 5% CO2 조건에서 배양하였다. HL 처리에 따른 세포생존율 정도를 측정하기 위하여 24-well plate에 RAW 264.7 대식세포를 well당 2 × 105개를 분주하고 12시간 배양하였다. 이후 HL을 농도별(25, 50, 75, 100 ㎍/mL)로 전처리 후 1시간 뒤 LPS (500 ng/mL)를 처리하고 24시간 배양하였다. 이후 MTT 시약을 0.5 ㎎/mL 농도가 되게 처리하여 2시간 동안 배양하고, 배지를 제거한 후 DMSO를 1 mL씩 분주하여 생성된 formazan을 모두 녹인 후 ELISA reader (Biotek, Shoreline, WA, USA)로 540 ㎚에서 흡광도를 측정하였다.
Nitric oxide (NO) assay
염증 활성을 확인하기 위해 염증 매개체인 NO 생성에 미치는 영향을 확인하였다. HL 처리에 따른 NO 억제 정도를 측정하기 위하여 24-well plate에 RAW 264.7 대식세포를 well당 2 × 105개를 분주하고 12시간 배양하였다. 이후 HL을 농도별(25, 50, 75, 100 ㎍/mL)로 전처리 후 1시간 뒤 LPS (500 ng/mL)를 처리하고 24시간 배양하였다. 상층액을 회수하여 Griess reagent [1% (w/v) sulfanilamide in 5% (v/v) phosphoric acid와 0.1% (w/v) naphthyl ethylene diamine dihydrochloride]와 1:1로 혼합하여 실온에서 10분간 반응시킨 후 ELISA reader (Biotek, Shoreline, WA, USA)로 540 ㎚에서 흡광도를 측정하였다.
ELISA (PGE2, TNF-α and IL-6) 측정
염증 매개체인 PGE2와 전염증성 사이토카인인 TNF-α와 IL-6에 미치는 영향을 확인하기 위하여 ELISA kits를 이용하여 발현량을 측정하였다. 24-well plate에 RAW 264.7 대식세포를 well당 2 × 105개를 분주하고 12시간 배양하였다. 이후 HL을 농도별(25, 50, 75, 100 ㎍/mL)로 전처리 후 1시간 뒤 LPS (500 ng/mL)를 처리하고 24시간 배양하였다. 배양액을 취한 뒤 ELISA kit manual에 따라 PGE2, TNF-α, 및 IL-6의 발현량을 측정하였다. ELISA kits와 PGE2는 Cayman Chemical Co. (Ann Arbor, MI, USA), TNF-α와 IL-6는 R&D Systems Inc. (Minneapolis, MN, USA) kit를 이용하였다.
Western blot 분석을 통한 MAPK 발현 측정
RAW 264.7 대식세포에 HL (100 ㎍/mL)을 전처리 후 1시간 뒤 LPS (500 ng/mL)을 처리하고 30분간 배양하였다. RAW 264.7 대식세포를 모은 다음, PBS로 세척하고 100 ㎕ PRO-PREP lysis buffer를 사용하여 20분간 부드럽게 용해시켰다. 용해물을 1400 rpm, 4℃에서 20분간 원심 분리시켰다. 단백질 측정을 위해 상층액을 사용했다. 단백질 농도는 Bio-Rad protein assay kit (Bio-Rad, Hercules, CA, USA)를 사용하여 측정하였다. 단백질을 10% SDS-polyacrylamide gel에서 분리하고, Nitrocellulose membranes (Schleicher & Schuell, Keene, NH, USA)으로 옮겼다. 이후 Chemidoc imaging system (Bio-Rad, Hercules, CA, USA)을 사용하여 단백질을 검출하였다.
통계 처리
실험 결과들의 유의성을 검정하기 위하여 분산분석(ANOVA)을 실시한 후 p < 0.05 수준에서 Duncan’s multiple range tests를 실시하였으며, 그 결과는 평균(mean) ± 표준편차(standard deviation, SD)로 표시하였다. 이때 사용한 모든 통계분석은 SPSS 17.0 (IBM SPSS Inc, NY, USA) 통계 프로그램을 이용하여 처리하였다.
결과 및 고찰
RAW264.7 대식세포 생존율
HL의 항염증 활성(Anti-inflammatory activity)을 분석하기 전에 RAW 264.7 대식세포에서 MTT assay를 통해 독성을 나타내지 않는 최적의 처리용량을 확인했다. Cell viability가 최소 90% 이상 되는 농도를 처리용량으로 설정하고자 했고, RAW 264.7 세포에 HL을 농도별로(25, 50, 75, 100 ㎍/mL) 처리했을 때 독성은 나타나지 않았다(Fig. 1). 또한, LPS (500 ng/mL)를 처리한 세포에서도 생존율이 90% 이상으로 독성을 나타나지 않았다. 이러한 결과는 사용한 HL 농도가 RAW 264.7 세포에서 무독성임을 나타내고, 무독성 조건에서 항염증 활성 및 메커니즘을 확인하고자 했다.
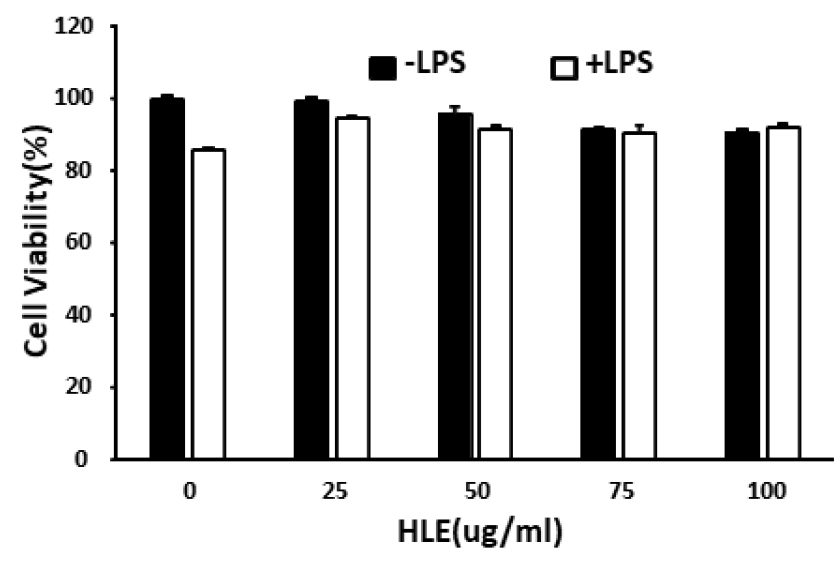
Fig. 1
Cell viability of RAW 264.7 cell treated with the extract of H. lyrata. RAW 264.7 cells (2 × 105 cells/mL) were incubated for 12 hr at 37℃ in 5% CO2. Cells were pretreated with the extract 1 hr prior to stimulation with LPS (500 ng/mL). After 24 hr incubation, cell viability was determined by an MTT assay. Data represent relative mean values ± SD of three independent experiments. The significance was determined by the Student's t-test (*p < 0.05, compared with control).
NO와 PGE2 생성에 미치는 영향
항염증 효과를 확인하기 위해 RAW 264.7 대식세포에 HL을 농도별(25, 50, 75, 100 ㎍/mL)로 처리하여 NO와 PGE2의 생성 조절에 영향을 미치는지 확인하였다. NO는 염증에 대한 다중 조절 효과를 발휘하고 면역조절에 중요한 역할을 하고, 거의 모든 단계의 염증에 영향을 미친다. NO 주요 합성효소인 iNOS에 의해 생성된 과량의 NO는 독성을 가지고 있고 염증을 유발할 수 있다(Coleman, 2001). McDonald et al. (2002)는 NO 생성과 생체이용률이 염증질환 관리에 중요하다고 이야기하였다. LPS (500 ng/mL) 처리 시 NO 생성이 증가하였지만, HL (25, 50, 75, 100 ㎍/mL) 전처리 후 LPS를 처리한 RAW 264.7 대식세포에서는 NO 생성이 농도 의존적으로 억제되었다(Fig. 2A).
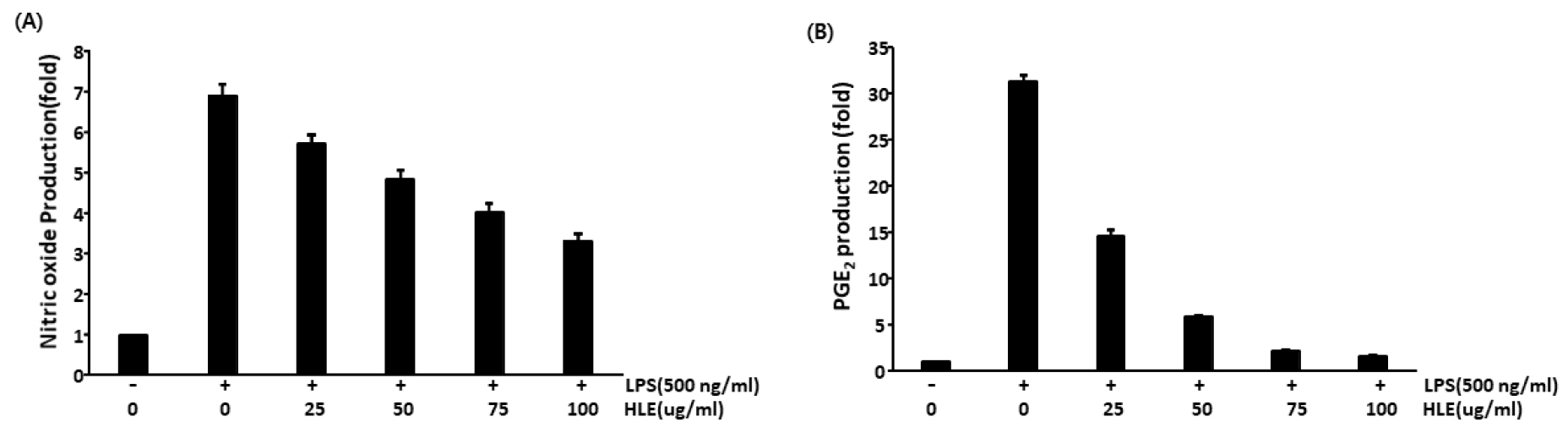
Fig. 2
Effect of H. lyrata extract on LPS-induced NO production (A), PGE2 expression (B) in RAW 264.7 cells. Cells (2×105 cells/mL) were pretreated with the extract 1 hr prior to stimulation with LPS (500 ng/mL). (A) After 24 hr incubation, cell supernatants were analyzed for NO production. NO production was detected using Griess reagent. (B) After 24 hr incubation, cell supernatants were analyzed for PGE2 production. The levels of PGE2 were detected using ELISA kit according to the instructions of ELISA kit. Data represent relative mean values ± SD of three independent experiments. The significance was determined by the Student's t-test (*p < 0.05, compared with control).
PGE2는 신체의 많은 세포와 조직에서 합성되며, 급성염증뿐만 아니라 류마티스(rheumatism) 및 골관절염과 같은 관절염 질환에서 주요 프로스타글란딘(prostaglandin)으로 이야기되어왔다. COXs 효소와 말단 PGE-synthases에 의해 아라키돈산(arachidonic acid)으로부터 전환된 PGE2는 혈관 확장, 혈관 투과성 및 통증을 매개하고 염증성 관절 질환의 발병에 중요한 역할을 한다(Westman et al., 2004). 이 프로스타노이드(prostanoid)는 전구체 줄기세포로부터 파골세포형성을 자극하여 뼈 재흡수를 조절하여 관절염 질환의 조직 파괴 특성에 관여한다. 또한, PGE2는 류마티스 관절염 및 골관절염 환자에서 활액, 활막, 및 혈정에서 matrix metalloproteinase (MMP)와 다른 염증 매개체로 고농도로 검출된다(Jia et al., 2014; Martel-Pelletier et al., 2003). NO 생성과 유사하게, LPS로 RAW 264.7 대식세포를 자극시켰을 때 염증 매개체인 PGE2의 생성이 증가되었고, HL 전처리 후 LPS를 처리했을 때 PGE2 증가가 유의적으로 억제됨을 확인하였다(Fig. 2B). 이러한 결과는 HL이 LPS로 자극된 RAW 264.7 대식세포에서 염증매개체인 NO와 PGE2의 생성을 감소시킴을 나타낸다.
이러한 결과는 HL가 LPS로 유도된 NO, PGE2의 발현을 억제함을 나타냈다. Wang et al. (2011)이 보고한 바에 의하면 HL은 arctiin과 tracheloside 성분을 함유하고 있다고 한다. 그리고 arctiin과 tracheloside는 항염증 활성을 나타낸다고 보고되었다(Lee et al., 2007; Lee et al., 2010; Nishibe, 1997). HL의 염증 효과는 염증 활성을 가진 arctiin과 tracheloside 성분 때문인 것으로 판단된다. 이에 전 염증성 사이토카인(pro-inflammatory cytokine) 분비에도 유의성 있는 효과를 나타낼 것으로 판단되어 추가로 실험을 진행하였다.
전 염증성 사이토카인(pro-inflammatory cytokines)의 생성에 미치는 영향
앞선 연구로 HL이 전 염증성 매개체의 강력한 억제제로 밝혀졌기 때문에, 우리는 ELISA를 통해 HL이 전 염증성 사이토카인(IL-6, TNF-α) 분비에 미치는 영향을 추가로 조사하였다. 전 염증성 사이토카인 중 하나인 Interleukin 6(IL-6)는 감염 및 조직 손상에 반응하여 빠르게 생성되고, 급성기 반응, 조혈, 및 면역반응의 자극을 통해 숙주 방어에 기여한다. IL-6 발현은 전사 및 전사 후 메커니즘에 의해 엄격하게 제어되지만, IL-6의 발현이 적절히 조절되지 않으면 만성 염증 및 자가 면역 질환을 유발할 수 있다(Tanaka et al., 2014). 또 다른 염증성 사이토카인인 TNF-α는 염증 과정 중에 대식세포에 의해 생성되며(Laksmitawati et al., 2016; Seo et al., 2018), 광범위한 림프, 비 림프 세포, 및 종양 세포에서 염증 및 세포독성을 발휘할 수 있는 다기능 사이토카인으로 보고되어있다(Laksmitawati et al., 2016). 염증 매개물질들이 과량 생산된 경우 염증반응이 활발히 일어나며 과도한 면역반응을 일으키게 되고, 각종 질환을 악화시키는 원인이 된다(Kim and Kang, 2019). 전 염증성 사이토카인을 억제할 수 있다면 염증뿐만 아니라 다양한 질병을 억제할 수 있을 것이다.
이러한 이유로 만성 염증을 조절 할 수 있을지 확인하기 위해 HL이 전 염증성 사이토카인(IL-6, TNF-α)에 미치는 영향을 확인하고자 하였다. Fig. 3을 보면 알 수 있듯이 LPS를 단독으로 처리한 RAW 264.7 대식세포를 대조군과 비교하였을 때 IL-6와 TNF-α 생산이 상당히 증가함을 알 수 있었고, HL 전처리 후 LPS를 처리한 경우 IL-6의 생산을 농도 의존적으로 감소시킴을 확인할 수 있었다(Fig. 3A). 그러나 LPS로 유도된 염증반응에서 HL의 처리는 TNF-α 생성에 아무 영향을 주지 않았다(Fig. 3B). 이러한 결과로 HL이 전 염증성 사이토카인 중 TNF-α 조절에 관여하지 않고, IL-6 생성 축적만을 방지함을 알 수 있었다. Kim et al. (2019)에 보고에 따르면 지칭개 전초를 이용한 클로로포름 추출물을 이용한 결과에서는 전 염증성 사이토카인(IL-6, TNF-α)이 모두 감소함을 보였다. TNF-α에 미치는 영향이 다르다는 것을 알 수 있었고, 이는 연구에 사용된 시료의 차이(전초, 지상부)로 비롯된 것으로 추측하였다.
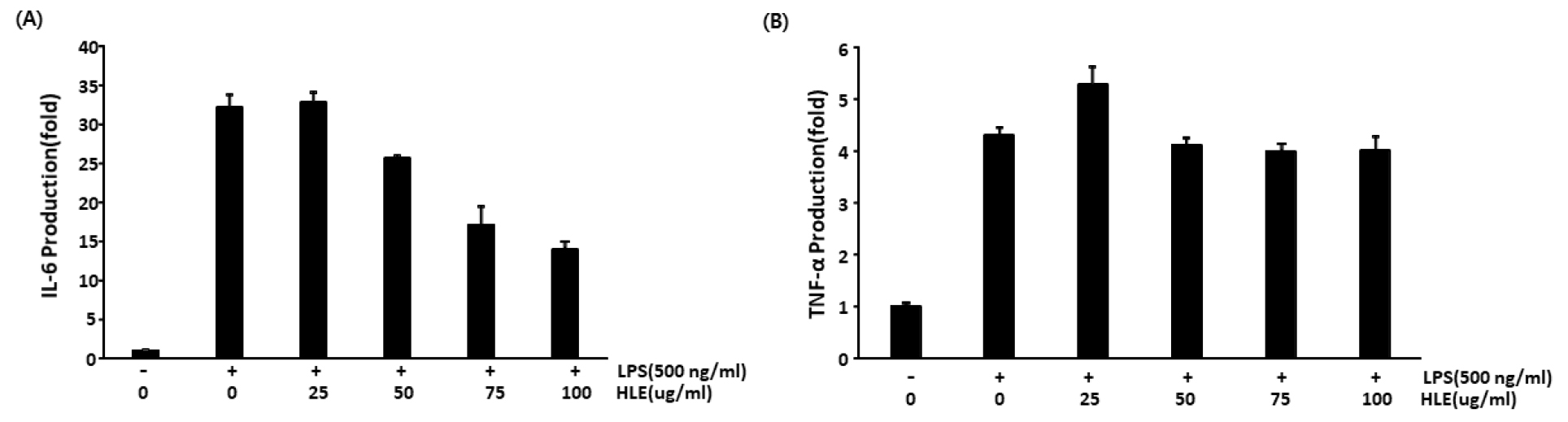
Fig. 3
Effect of H. lyrata on LPS-induced IL-6 (A) and TNF-α (B) expression in RAW 264.7 cells. Cells (2×105 cells/mL) were pretreated with the extract 1 hr prior to stimulation with LPS (500 ng/mL). (A) After 24 hr incubation, cell supernatants were analyzed for IL-6 production. The levels of IL-6 were detected using ELISA kit according to the instructions of ELISA kit. (B) After 24 hr incubation, cell supernatants were analyzed for TNF-α production. The levels of TNF-α were detected using ELISA kit according to the instructions of ELISA kit. Data represent relative mean values ± SD of three independent experiments. The significance was determined by the Student's t-test (*p < 0.05, compared with control).
Mitogen activated protein kinases (MPAKs) 신호전달 경로에 미치는 영향
NO, PGE2, 및 IL-6는 MAPK cascade의 활성화에 의해 유도된다고 알려져 있다(Bromberg and Wang, 2009; Peter et al., 2003). 따라서, 본 연구는 HL에 의해 억제된 NO, PGE2, 및 IL-6가 상위 시그널인 MAPK cascade의 억제를 통해 나타난 효과인지 알아보았다. LPS로 염증반응이 유도된 RAW 264.7 대식세포에서 MAPK 활성화가 HL에 의해 조절되는지 확인하였다. 1시간 전에 HL을 전처리하고 30분간 LPS 자극으로 MAPK의 모든 구성원을 활성화시켜 MAPK의 인산화의 억제 정도를 확인하였다. HL은 ERK과 p38의 활성화를 상당히 약화시켰지만, JNK는 p38과 ERK보다 덜 민감하게 조절하였다(Fig. 4).
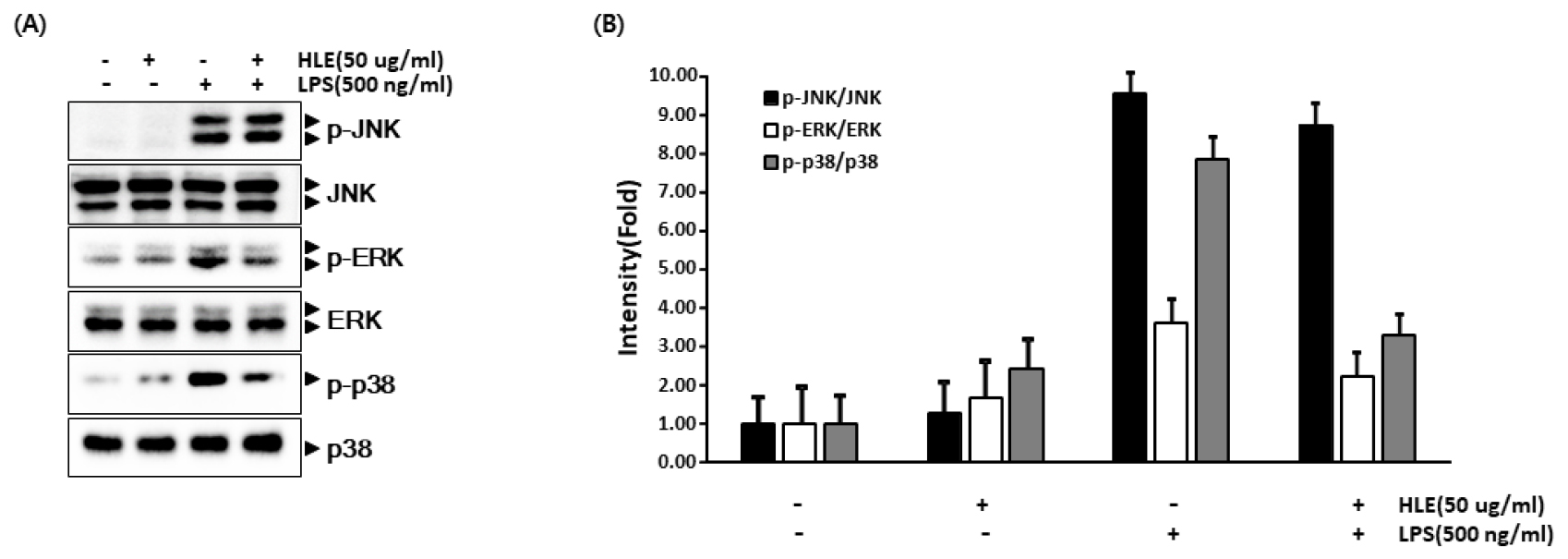
Fig. 4
Effects of H. lyrata on LPS-induced phosphorylation of MAPKs in RAW 264.7 cells. (A) Cells (2 × 105 cells/mL) were pretreated with the extract 1 hr prior to stimulation with LPS (500 ng/mL). After 30 min incubation, the nuclear extracts were prepared and resolve the levels of p-JNK, JNK, p-ERK, ERK, p-p38 and p38 by western blot assay. (B) The levels of p-JNK/JNK, p-ERK/ERK and p-p38/p38 were expressed as intensity (fold) values.
MAPKs는 세포에서 단백질 사슬로 존재하고, 진핵세포에서 신호의 통신을 조절한다(Manzoor et al., 2014). MAPK 경로는 다양한 세포에서 여러 전염증성 사이토카인의 활성화에 중요한 조절제로 알려져 있다(Bromberg and Wang, 2009). ERK, p38, 및 JNK를 포함한 MAPK의 인산화는 염증성 발현인자로 알려진 activator protein 1(AP-1)과 nuclear factor kappa B (NF-kB)를 활성화시킨다(Kawai and Akira, 2007). 따라서, HL은 MAPK에서 ERK와 p38의 인산화를 억제하여 AP-1, 염증 발현 인자를 억제하고, 항염증효과를 나타내는 것으로 추측하였다.
적 요
본 연구에서는 LPS로 자극을 유도한 RAW 264.7 대식세포에서 지칭개 추출물의 항염증 효능을 알아보기 위해 이와 연관된 다양한 인자(NO, PGE2, IL-6, 및 TNF-α)와 MAPK 신호전달 경로에 대해서 조사하였다. 먼저 HL 처리에 따른 세포 생존율에 대해 조사한 결과, HL을 농도별로 처리했을 때 저농도인 25 μg/mL에서부터 고농도인 100 μg/mL까지 모두 90% 이상의 생존율이 나타났으며, LPS를 처리한 RAW 264.7 대식세포에서도 90% 이상의 생존율을 나타내 실험에 사용된 HL의 농도가 RAW 264.7 대식세포에서 무독성임을 확인할 수 있었다. 이러한 무독성 조건에서 HL의 항염증 활성을 확인하기 위하여 염증 매개체(inflammatory mediators)로 잘 알려진 NO와 PGE2의 생성 변화를 확인한 결과, LPS로 염증반응이 유도된 RAW 264.7 대식세포에서 NO와 PGE2의 생성이 농도 의존적으로 억제됨을 확인하였다. HL이 NO와 PGE2를 억제하는 항염증 효과가 있음을 관찰하였고, 이에 전 염증성 사이토카인 분비에도 유의성 있는 효과를 나타낼 것이라 판단되어 전 염증성 사이토카인(IL-6와 TNF-α)에 어떠한 영향을 미치는지 조사하였다. HL은 LPS로 유도된 RAW 264.7 대식세포의 염증반응에서 IL-6의 생산을 유의적으로 억제함을 관찰할 수 있었다. 한편 다른 전 염증성 사이토카인인 TNF-α 생산에는 아무 영향을 주지 않았다. 이러한 결과는 HL이 전 염증성 사이토카인 중 TNF-α 조절에 관여하지 않고, IL-6 생성을 억제하여 염증 매개체의 생성을 억제한다고 추측 할 수 있었다. HL이 NO, PGE2, 및 IL-6의 조절에 작용하는 메커니즘이 상위 시그널인 MAPK cascade의 억제를 통해 나타나는 효과인지 알아보기 위해 염증과 관련된 MAPK 시그널인 p38, ERK, 및 JNK의 발현 변화를 관찰하였다. HL은 p38과 ERK의 발현 활성화를 상당히 약화시켰지만 JNK는 p38과 ERK보다 덜 민감하게 조절함을 관찰할 수 있었다. 이상의 결과를 종합해 보면 LPS로 유도된 RAW 264.7 대식세포에서 HL은 MAPK 신호경로인 JNK 발현에 유의적인 영향을 주지 못해서 JNK와 관련된 TNF-α 생산에 영향을 주지 못한 것으로 판단된다. 다른 MAPK 신호경로인 p38과 ERK의 발현을 약화시킴으로써 그 다음 기작인 IL-6, NO, 및 PGE2의 생산을 억제시켜 염증반응을 억제한 것으로 추측되어 진다. 이상의 결과를 종합해 보면 HL이 항염 활성을 가지고 있음을 확인할 수 있었으며, 이를 기반으로 HL의 MAPK 신호경로를 통한 염증성 사이토카인과 염증 매개체와의 연관성에 대한 기초자료로 활용할 수 있는 근거 자료가 될 수 있을 것으로 생각된다. 또한, 다양한 경로를 통한 염증 조절 기전 연구는 추가적으로 이루어져야 할 것으로 사료된다.




