서 언
재료 및 방법
리기다 솔방울 추출물
항산화 활성
세포 배양 및 독성 평가
UVB 조사
Western Blot
통계분석
결과 및 고찰
추출물의 항산화 활성
ECRT의 세포 독성 평가 및 자외선에 의한 DNA 손상 억제 효과
UV-B 조사에 따른 ECRT의 항주름 효과
적 요
서 언
인간의 피부는 외부 환경으로부터 신체를 보호하는 중요한 역할을 하지만, 자외선(UV), 오염물질, 스트레스 등 다양한 외부 요인에 의해 손상을 입을 수 있다(Biniek et al., 2012). 특히 자외선은 피부 노화의 주요 원인으로, UVB (280 ~ 320 ㎚)는 피부 표피층에 도달하여 활성산소종(ROS: reactive oxygen species)을 생성하고, 이로 인해 산화적 스트레스가 발생하여 피부세포의 DNA 손상, 세포 자멸사, 콜라겐 분해 및 주름 형성 등을 초래한다(Fisher et al., 1997). UVB의 지속적인 노출은 피부의 세포와 조직에 심각한 영향을 미치며(Lee et al., 2023) 이를 방지하기 위한 다양한 예방 및 치료 전략이 필요하다.
산화적 스트레스는 피부 노화와 질병의 주요 원인으로, 이를 완화할 수 있는 항산화제의 필요성이 커지고 있다. 항산화제는 활성산소를 제거하거나 산화적 손상을 억제하여 피부 건강을 유지하는 데 중요한 역할을 한다(Masaki, 2010). 특히, 천연 유래 항산화제는 낮은 독성과 높은 안전성 덕분에 화장품 및 의약품 산업에서 주목받고 있다.
리기다 소나무(Pinus rigida)는 북미 동부 지역에서 자생하는 소나무과 식물로, 국내에서는 산림 녹화용으로 도입되었다. 소나무과 식물은 항산화 및 항염증에 효과가 있다고 알려진 다양한 페놀 화합물과 camphene, α-pinene, β -pinene 등의 terpene계의 정유 성분들을 함유하는 것으로 보고되었다(An et al., 2013; Kuk et al., 1997; Otto et al., 2007). 기존 연구에 따르면, 리기다 소나무에는 항산화 성분이 풍부하게 함유되어 있어 항염증, 항산화, 항균 효과가 보고되었다(Choi et al., 2020; Jang et al., 2008). 따라서 이러한 연구배경을 기반으로 리기다 소나무 솔방울 추출물(P. rigida cone extract, ECRT)의 피부 노화 완화 효과를 기대할 수 있다
활성산소는 세포 대사 과정에서 자연적으로 생성되지만, 과도하게 축적되면 세포막 지질 과산화, DNA 손상, 단백질 변성 등을 유발할 수 있다(Therond, 2006). 이를 평가하기 위해 DPPH 및 ABTS 라디칼 소거 활성을 사용하여 항산화 활성을 측정한다(Re et al., 1999). 또한 자외선으로 인한 산화적 스트레스는 matrix metalloproteinase (MMP) 발현을 증가시켜 피부 탄력과 구조를 손상시킨다(Fisher et al., 1997; Quan and Fisher, 2015). 뿐만 아니라, 자외선에 의한 산화적 스트레스는 DNA 이중가닥 절단(double-strand breaks, DSB)을 유발하여 DNA 손상의 주요 분자 지표인 γ-H2AX의 인산화를 초래한다(Dinant and Luijsterburg, 2009). γ-H2AX의 발현 증가는 세포 노화 및 세포주기 정지와 직접적으로 연결되며, 이 과정에서 p53 단백질이 활성화되어 손상된 세포의 생존 경로를 조절하거나 세포사멸(apoptosis)을 유도한다(Chen et al., 2008; Tavana et al., 2010). p53의 지속적인 활성화는 세포 노화 촉진에 핵심적인 역할을 하며, 이는 피부 노화의 분자적 특징 중 하나로 간주된다(Tavana et al., 2010; Vousden and Lane, 2007). 따라서 γ-H2AX 및 p53 발현 수준은 자외선에 의한 피부세포 노화를 평가하는 데 중요한 분자 지표로 활용된다.
본 연구는 리기다 솔방울 추출물(ECRT)의 항산화 활성, 자외선으로 유발된 DNA 손상 방어 효과, 그리고 MMP 발현 억제를 통한 항주름 효과를 분석하여 ECRT가 피부 노화 방지에 미치는 영향을 규명하고자 한다. 연구 결과는 천연 유래 항산화 소재의 활용 가능성을 확장하고, ECRT 기반의 바이오헬스 제품 개발에 기초 자료를 제공할 것이다.
재료 및 방법
리기다 솔방울 추출물
본 연구에서 사용된 ECRT는 선행된 연구를 통해 확보된 추출물을 동일하게 사용하였다(Choi et al., 2020). 잘 건조된 리기다 소나무의 솔방울 500 g을 5 L의 80% 메탄올(methanol, Duksan, Korea)에 5일간 매일 2시간 동안 2회 초음파를 가해 추출하였다. 추출물의 상등액을 여과하여 진공회전농축기(vacuum rotary evaporator, N-1110S, EYELA, Japan)를 이용하여 메탄올을 증발시켜 농축한 다음, 농축물과 동일한 비율의 석유에테르(petroleum ether, Duksan, Korea)와 혼합하여 분획 추출한 다음 상층인 석유에테르층을 제거하고 남은 추출물(수층)에 다시 에틸아세테이트(ethyl acetate, Duksan, Korea)를 이용하여 동일한 방법으로 추출한 다음 에틸아세테이트 분획물을 회수하였다. 에틸아세테이트 분획물을 농축한 다음 동결건조하여 분말화한 다음 효능 평가를 위한 시료(ECRT)로 사용하였다.
항산화 활성
1,1-diphenyl-2-picryl hydrazyl (DPPH, Sigma-Aldrich, United States)를 이용한 전자공여능(Bondet et al., 1997)과 2,2'-azinobis- (3-ethylbenzothiazoline-6-sulfonate) (ABTS, Sigma-Aldrich, USA) 라디칼 소거 활성(Van den Berg et al., 1999)을 통해 추출물의 항산화활성을 평가하였다. DPPH 용액은 515 ㎚에서 흡광도가 1.00이 되도록 희석하여 준비한다. ABTS 원액은 7 mM의 2,2'-azinobis-(3-ethylbenzothiazoline-6-sulfonate)와 potassium persulfate (Sigma- Aldrich, United States) 2.45 mM를 혼합한 뒤 24 h동안 방치하여 ABTS+ 를 형성시켜 원액을 준비하였다. 그리고 원액은 증류수를 이용하여 734 ㎚에서 흡광도가 0.70이 준비하였다. 각 용액 760 μL와 농도별 추출시료(4 ㎎/mL) 40 μL를 혼합하여 20 min 동안 37℃에서 반응시킨 후 UV/Visible spectrophotometer (X-ma 3000 Human Cop, Korea)를 이용하여 515 ㎚ (DPPH)와 734 ㎚ (ABTS)에서 흡광도를 측정하였다. 시료처리에 의한 항산화 활성은 대조구의 흡광도와 비교하여 %로 표시하였다.
세포 배양 및 독성 평가
본 연구에서 사용된 human foreskin fibroblasts (Hs68세포)는 American type culture collection (ATCC, Manassas, USA)에서 분양받아 실험하였다. 세포는 penicillin/streptomycin 1%와 fetal bovine serum (FBS, Cytiva, USA) 10%가 포함된 Dulbecco’s Modified Eagle Medium (DMEM, WELGENE, USA)에서 37℃, 5% CO2 조건하에 배양 하였다. 세포 독성을 평가하기 위해 Hs68 세포를 96 well plate에 1.0 × 104 cells/well의 밀도로 분주하여 24시간 배양한 후 농도 별로 시료를 처리하였다. 시료 처리 24시간 후 CellTiter 96® AQueous One solution (Promega, USA)을 배지의 총량의 20%씩 처리하여 2시간 배양하였다. 반응 후 UV/Visible spectrophotometer를 이용하여 570 ㎚에서 흡광도를 측정하여 무처리구와 비교하여 세포독성을 확인하였다.
UVB 조사
Hs68 세포를 6-well plate에 1.0 × 105 cells/well의 밀도로 분주한 후, 24시간 동안 안정화 배양하였다. 이후 세포에 ECRT를 농도별(0, 25, 50, 100, 200 μg/mL)로 처리하고 2시간 동안 전처리하였다. 전처리 후 배지를 제거하고, 세포를 인산완충용액(phosphate-buffered saline, PBS)으로 1회 세척하여 배지 내 성분이 UVB 흡수에 미치는 영향을 최소화하였다. 세척된 세포에 UV Crosslinker (XL-1000, Artisan Technology Group, Champaign, IL, USA)를 이용하여 60 mJ/㎠의 UVB를 조사하였다. UVB 조사 후 즉시, 동일한 농도의 ECRT를 포함한 신선한 배지를 첨가하여 24시간 동안 추가 배양하였다. 모든 실험은 빛을 차단한 조건에서 수행하였다.
Western Blot
시료 처리 24시간 후, 각 처리별 Hs68 배양세포는 PBS로 2회 세척한 뒤, protease inhibitor cocktail (Sigma-Aldrich, USA)을 포함한 RIPA buffer (Thermo Scientific, USA)로 용해하고 얼음에서 30분 동안 정치하였다. 세포 용해액은 4℃, 12,000 rpm에서 20분 동안 원심분리하였으며, 상층액은 Bradford protein assay kit (Bio-rad, USA)를 이용하여 단백질 농도를 정량하였다. 상층액은 2 × Lamilae buffer와 혼합하여 95℃에서 5분 동안 가열하고, 각 20 μg 단백질량에 해당하는 시료를 10% sodium dodecyl sulfate polyacrylamide gel electrophoresis (SDS-PAGE)에서 전기영동하였다. 전기영동한 뒤 polyvinylidene difluoride (PVDF) membrane (Bio- rad, USA)으로 단백질을 전이하였다. 단백질이 전이된 PVDF막은 TBST 용액(5% skim milk in Tris-buffered saline with 0.1% Tween-20)으로 상온에서 1시간 동안 blocking하였다. 이후 각 단백질에 대한 1차 항체를 적정 농도로 희석하여 4℃에서 overnight 처리한다. 1차 항체 반응 후, TBST로 10분 간격으로 3회 세척하고, HRP-conjugated 2차 항체를 적정 농도로 희석하여 1시간 동안 반응시켰다. 이어서 동일하게 TBST로 10분 간격으로 3회 세척한 후, enhanced chemiluminescence (ECL) western blotting detection kit (Bio-rad, USA)를 이용하여 단백질 밴드를 검출하였다. 단백질 band는 Chemi-Doc Imaging System (Bio-Rad, USA)로 촬영하였으며, band intensity는 ImageJ Software (NIH, USA)를 이용하여 분석하였다.
통계분석
모든 실험은 3회 이상 반복 수행되었으며, 데이터 분석은 통계 프로그램(GraphPad Prism 5.02, GraphPad Software, USA)을 사용하여 진행되었다. 각 데이터는 일원분석법(ANOVA)을 통해 분석되었으며, 실험의 유의성을 검증하기 위해 Dunnett 사후 검정을 실시하였다. p < 0.05는 통계적으로 유의미한 결과로 간주하였다.
결과 및 고찰
추출물의 항산화 활성
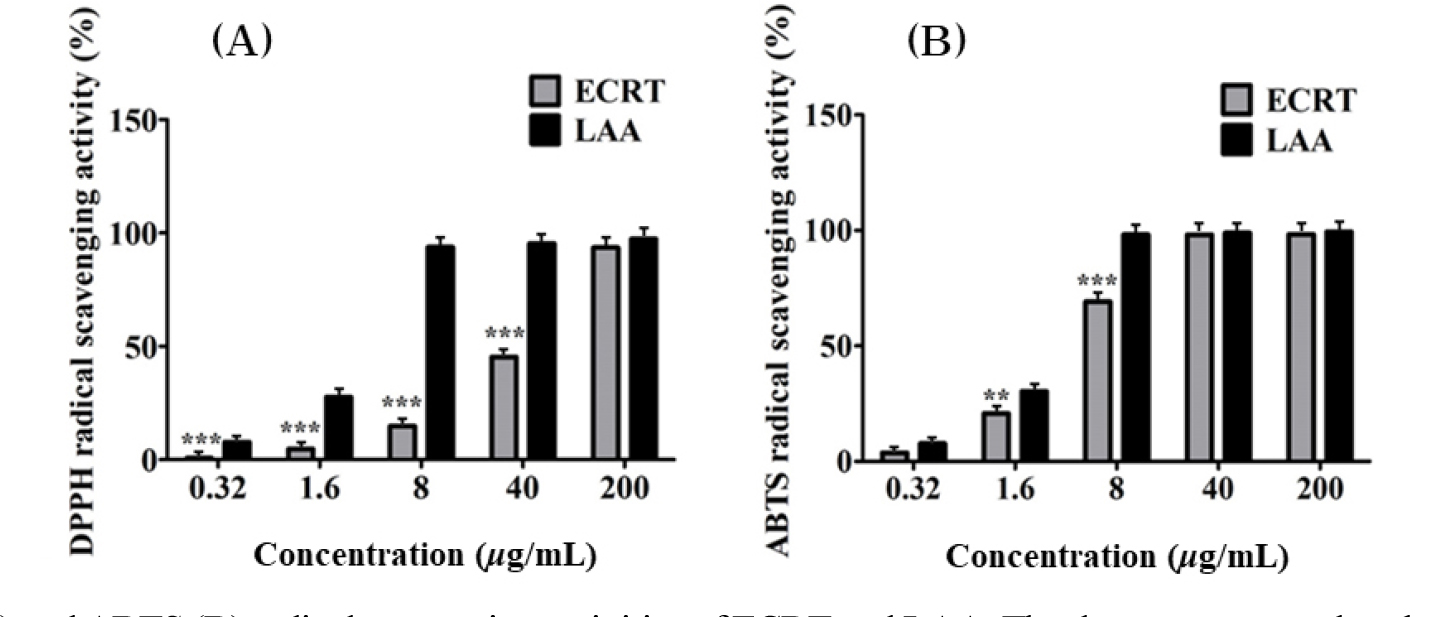
리기다 솔방울 추출물(ECRT)의 항산화 활성을 DPPH 및 ABTS 라디칼 소거 활성에 의한 평가 결과(Fig. 1), ECRT는 농도가 증가함에 따라 항산화 활성이 증가하였다. 낮은 농도(1 μg/mL)에서는 L-아스코르브산(L-ascorbic acid, LAA)과 비교해 소거 활성이 낮았으나 200 μg/mL 이상에서 LAA와 유사한 DPPH 활성을 보였고(Fig. 1A), ABTS 라디칼 소거 활성에서도 40 μg/mL 이상의 농도에서 LAA와 비슷한 활성을 나타냈다(Fig. 1A). 이러한 결과는 ECRT가 일정 농도 이상에서 유의미한 항산화 효과를 발휘할 수 있음을 시사하며, 이러한 결과는 ECRT에 포함된 플라보노이드(flavonoid)와 폴리페놀(polyphenol) 등의 항산화 성분 때문으로 판단된다. 이전 연구들에서도 식물 추출물의 항산화 효과가 플라보노이드 함량과 연관이 있다는 사실이 보고된 바 있다(Brand-Williams et al., 1995). 이는 ECRT가 피부 산화 손상 방지에 효과적으로 작용할 가능성을 시사한다.
ECRT의 세포 독성 평가 및 자외선에 의한 DNA 손상 억제 효과
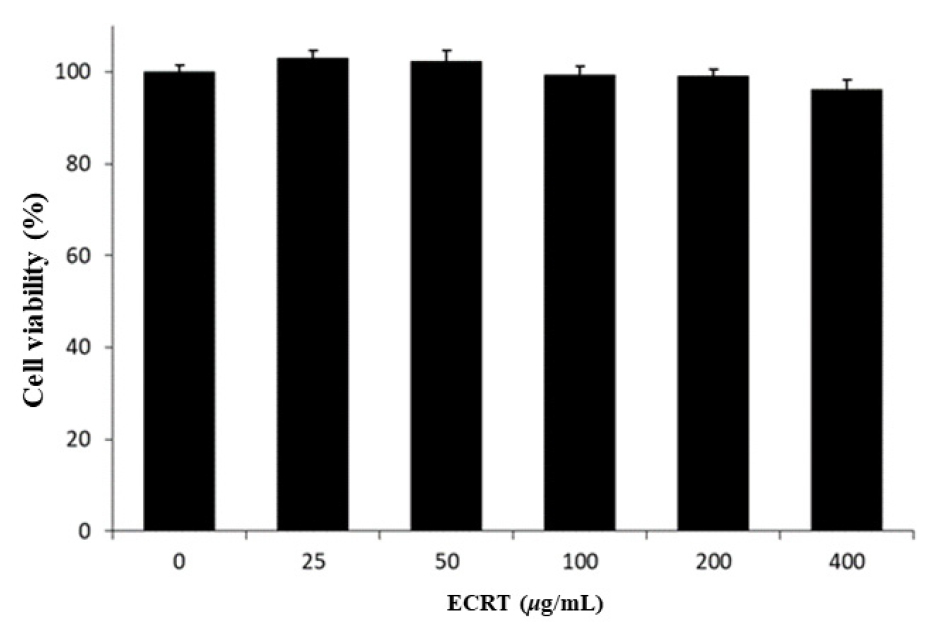
ECRT의 세포 독성 평가에서, Hs68 세포를 사용하여 다양한 농도(25, 50, 100, 200, 400 μg/mL)에서 세포 생존율을 측정하였다(Fig. 2). 그 결과, ECRT 처리군은 모든 농도(25 ~ 400 μg/mL)에서 ECRT 무처리 대조군과 비교하여 유의한 세포 독성을 나타내지 않았다. 이는 ECRT가 피부 섬유아세포에 생리적 범위 내에서 안전하게 적용될 수 있으며, 다양한 농도 범위에서 사용 가능함을 보여준다.
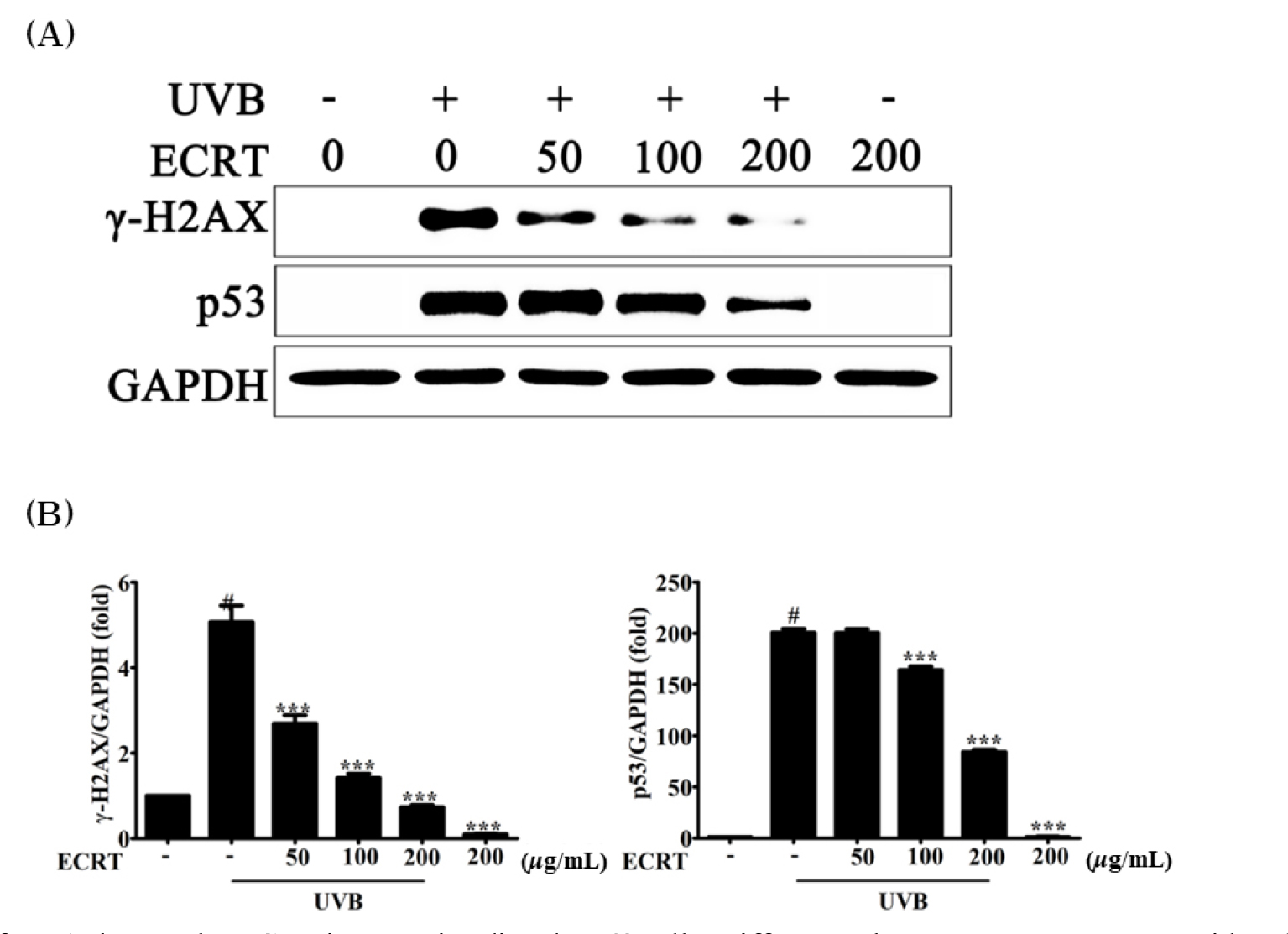
ECRT의 UVB 조사에 의한 세포 내 DNA 손상 방어 효과를 평가하기 위해 γ-H2AX와 p53 단백질 발현 변화를 immunoblotting으로 분석하였다(Fig. 3). UVB만 조사한 ECRT 무처리 대조군에서는 UVB 비조사 대조군에 비해 γ-H2AX와 p53 발현이 유의하게 증가하였다(p < 0.05). 그러나 UVB 조사 후 ECRT를 처리한 군에서는 γ-H2AX와 p53 발현이 농도의존적으로 감소하였으며, 특히 100 μg/mL 및 200 μg/mL 농도에서 발현 억제가 통계적으로 유의하였다(p < 0.001).
γ-H2AX는 DNA 이중 가닥 절단(double-strand breaks, DSB)의 대표적인 분자 지표로, UVB에 의해 생성된 활성산소종(reactive oxygen species, ROS) 등 산화 스트레스가 주요 유도 인자 중 하나로 작용한다(Falaschi et al., 2023; Sinha and Häder, 2002; Wei et al., 2024). 본 연구에서 ECRT는 항산화 활성에 의해 UVB로 인한 산화 스트레스를 억제함으로써 γ-H2AX 발현을 감소시켰을 가능성이 있다. 그러나 γ-H2AX 발현은 산화 스트레스 외에도 다양한 스트레스 경로에 의해 조절될 수 있으므로, 본 연구 결과는 ECRT가 산화 스트레스 완화와 관련하여 γ-H2AX 발현 억제에 기여했을 가능성을 제시한다.
한편, p53은 DNA 손상, 산화 스트레스, 염증 신호 등 다양한 세포 스트레스에 반응하여 세포주기 정지(cell cycle arrest)나 세포 사멸(apoptosis)을 유도하는 주요 전사조절자로 알려져 있다(Vousden and Prives, 2009). 본 연구에서 ECRT 처리군에서 p53 발현 감소가 관찰된 것은 ECRT가 UVB에 의한 세포 스트레스를 완화하여 p53 매개 반응을 억제했을 가능성을 시사한다. 이러한 결과는 ECRT가 피부 세포의 손상 방어 및 생존 유지에 기여할 수 있는 잠재력을 가짐을 보여준다.
UV-B 조사에 따른 ECRT의 항주름 효과
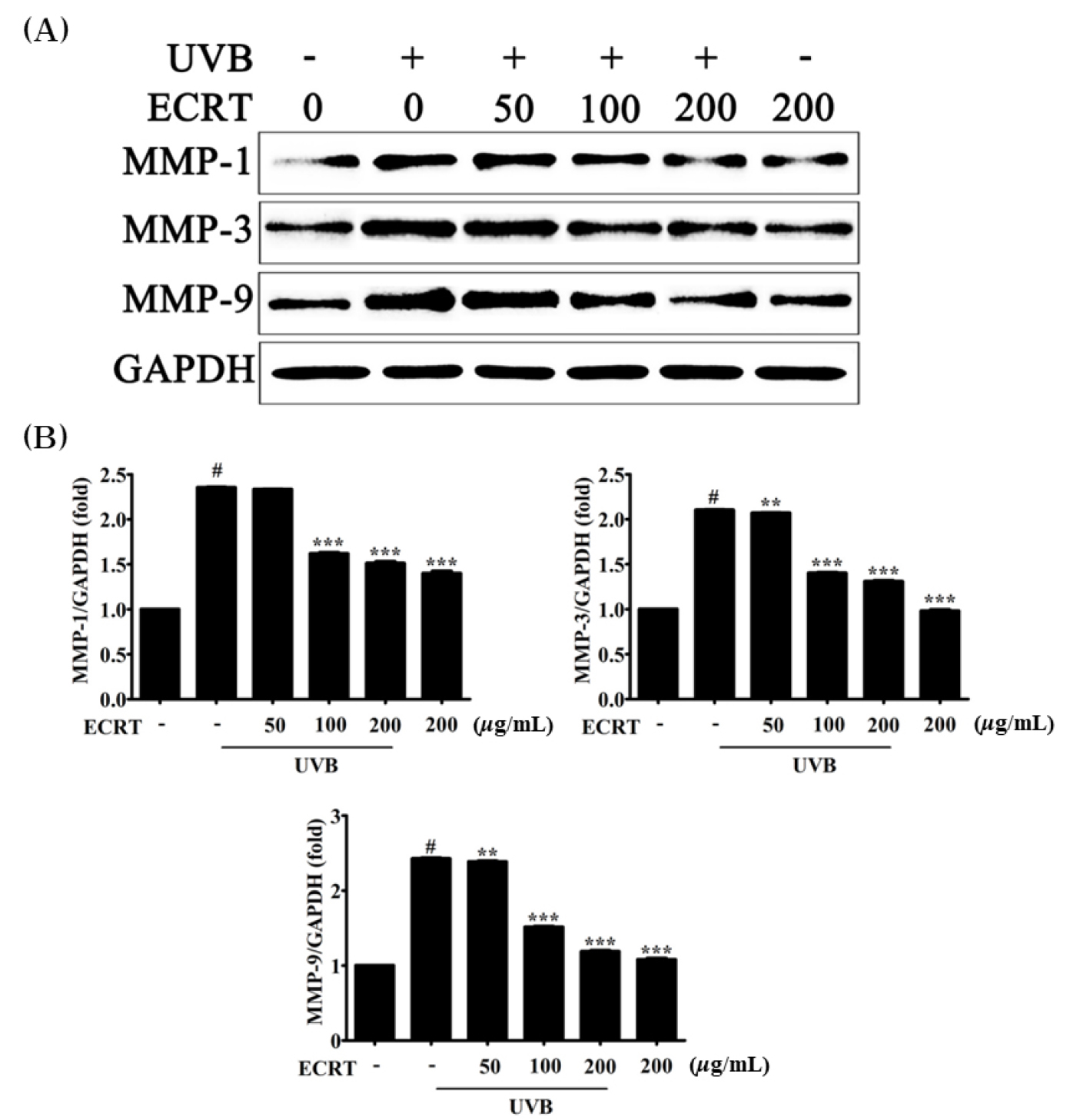
UV-B 조사에 의해 피부의 세포외 기질(extracellular matrix, ECM)을 분해하는 MMP-1, MMP-3, MMP-9의 발현이 증가함에 따라 주름 형성이 촉진된다. 본 연구에서는 ECRT가 농도 의존적으로 MMP 발현을 억제하는 효과를 보였다(Fig. 4). 특히, 100 ~ 200 μg/mL 농도에서 MMP-1, MMP-3, MMP-9의 발현이 UVB만 처리한 대조군에 비해 통계적으로 유의하게 감소하였다(p < 0.001). 활성산소종(ROS)은 MMP 발현을 촉진하는 주요 인자로 알려져 있으며(Jang et al., 2023; Kim et al., 2018) 항산화제를 통해 ROS를 억제함으로써 MMP 활성화를 간접적으로 조절할 수 있다. ECRT의 항산화 활성은 이러한 기전과 밀접하게 연관되어 있을 것으로 추정된다. 따라서 ECRT는 UVB로 유발된 산화적 손상을 방어하고 ECM 손실을 최소화하여 항노화 및 항주름 효과를 발휘할 수 있을 것으로 해석된다(Fisher et al., 1997). 본 결과는 ECRT가 피부 보호제로서 적용될 수 있는 잠재력을 뒷받침한다.
적 요
본 연구에서는 리기다 솔방울 추출물(ECRT)의 피부세포 노화 완화 효과를 평가하였다. ECRT는 자외선(UVB)에 의한 DNA 손상 방어와 MMP 발현 억제를 통한 항주름 효과가 있음을 확인하였다. ECRT는 농도 의존적으로 항산화 활성을 나타내었으며, 200 μg/mL 농도에서 가장 높은 항산화 효과를 보였다. 특히, ECRT 처리 시 UV-B 자극에 의해 유발된 γ-H2AX와 p53 단백질 발현이 유의미하게 감소하여, ECRT가 DNA 손상을 효과적으로 완화할 수 있음을 보여주었다. 이러한 결과는 세포 내 DNA 복구 기전과 세포 스트레스 반응을 조절하는 중요한 역할을 한다는 것을 시사하며, 피부 보호제로서의 가능성을 제시한다. 또한 MMP-1 및 MMP-3 발현 억제 실험에서도 ECRT가 피부의 세포외 기질(ECM) 보호 및 항주름 효과에 중요한 역할을 하였으며, 특히 200 μg/mL 농도에서 두드러진 항주름 효과를 보였다. ECRT의 항산화 활성이 활성산소종(ROS)을 억제함으로써 MMP 발현을 감소시키고 피부 탄력과 구조를 보호하는 기전을 제시하였다. 이러한 기전은 ECRT가 피부 노화 방지와 항주름 효과를 발휘하는 중요한 메커니즘임을 뒷받침한다. 향후 연구에서는 ECRT의 성분 분석 및 작용 메커니즘을 보다 세부적으로 연구하여 주요 활성 물질과 정확한 분자적 기전을 밝혀내고, 다양한 환경적 스트레스에 대한 피부 보호 효과를 명확히 규명할 필요가 있다. 또한, 콜라겐 발현 변화 분석을 포함한 ECM 손상에 대한 추가 연구를 통해 ECRT의 항주름 효과를 보다 세밀하게 규명할 수 있을 것이다. 본 연구는 ECRT가 피부 보호제 개발에서 중요한 후보 물질이 될 수 있음을 시사하며, 향후 화장품 및 의약품 개발에 중요한 기초 자료를 제공할 것으로 기대된다.