서 언
재료 및 방법
식물 시료 및 추출물 제조
항산화 활성
총페놀 및 총플라보노이드 함량 분석
HPLC 분석
세포 배양 및 세포 생존율 평가
NO 생성 억제 분석
iNOS 및 COX-2 단백질 발현 분석
통계학적 분석
결과 및 고찰
미선나무 꽃 추출물의 항산화 활성
총페놀(TPC) 및 총플라보노이드(TFC) 함량
미선나무 꽃 추출물의 유효성분 함량
세포 생존율 평가
NO 생성 억제 효과
iNOS 및 COX-2 단백질 발현 억제 효과
적 요
서 언
미선나무(Abeliophyllum distichum Nakai)는 1속 1종이자 오직 한국에만 자생하는 물푸레나무과(Oleaceae)의 낙엽관목으로, 이른 봄 백색 또는 연분홍색의 꽃을 개화하는 관상적 가치가 높은 식물자원이다(Lee et al., 1983). 좁은 분포범위와 제한된 자생지로 인해 희귀성이 높으며, 식물형태학·유전학·원예학·자원식물학 분야에서 다양한 연구가 수행되어 왔다(Kim et al., 2002; Lee et al., 2008; Lee et al., 2024; Park et al., 2019). 최근에는 완전한 엽록체 게놈서열의 해석이 보고되면서 미선나무의 분류학적 위치, 계통유연관계, 유전적 변이 분석이 진전되고 있다(Kim et al., 2016; Park et al., 2019).
미선나무 부위별 분석 결과, 꽃과 잎 등에서 acteoside, isoacteoside와 같은 phenylethanoid glycoside 계열의 2차 대사산물이 확인되었으며(Lee et al., 2020; Lee et al., 2024), 이러한 성분에 기인하여 미선나무 추출물은 항산화, 항염증 및 항암 활성을 나타내는 것으로 알려져 있다(Choi et al., 2024; Jang et al., 2020; Nam et al., 2015; Park et al., 2014). 특히 미선나무 추출물은 DPPH 및 hydroxyl radical 소거능을 통해 항산화 활성을 나타내었으며(Lee et al., 2020), RAW264.7 대식세포 모델에서 NO 생성 억제와 함께 MAPKs 및 NF-κB 신호전달계 조절을 통한 항염증 효과도 보고된 바 있다(Lee, 2018; Nam et al., 2015). 이와 같은 연구 결과는 미선나무가 생리활성 소재로서의 잠재적 우수성을 시사하며, 기능성 식품·건강기능소재·화장품 원료 등 다양한 응용 가능성을 제시한다.
그러나 미선나무는 야생 집단 간 변이가 매우 큰 것으로 알려져 있으며, 특히 꽃색·꽃형·개화시기 등의 표현형 변이뿐만 아니라 대사체 수준에서도 차이가 존재하는 것으로 보고되고 있다(Lee et al., 2024). 이러한 변이는 유전적 다양성 측면에서는 긍정적일 수 있으나 산업적 소재 개발 측면에서는 성분 표준화, 품질 재현성 확보, 규제 대응 등에서 한계를 야기할 수 있다. 따라서 기능성 소재로 활용하기 위해서는 안정된 유전적 배경과 재현 가능한 대사체 구성을 보유한 품종 기반 연구가 요구된다.
천연물 유래 기능성 소재 개발에 있어 원료의 균일한 공급은 산업화의 필수 전제 조건이며, 이를 위해 기원 식물의 분류학적 명확성 확보와 더불어 유효성분의 표준화(standardization) 및 안정적인 대량 재배 시스템 구축이 선행되어야 한다. 특히 ‘옥황1호’와 같은 미선나무의 유전적 형질이 고정된 품종을 활용하는 것은 원료의 재현성과 품질 관리 측면에서 매우 중요한 의의를 지닌다(KSVS, 2014). 따라서 미선나무 소재 개발 전략을 불분명한 야생 개체군 단위에서 품종 기반 접근 방식(cultivar-based approach)으로 전환하는 것은 국내 고유 생물 자원의 고부가가치화 및 기능성 소재화 전략을 고도화하는 핵심적인 방안이라 할 수 있다.
이에 본 연구에서는 품종 등록된 미선나무 ‘옥황1호’ 꽃 추출물을 대상으로 추출 용매별 항산화 및 항염증 활성을 정량적으로 분석함으로써 미선나무 신품종 유래 소재의 생물학적 잠재력을 검증 하였다. 이를 통해 미선나무 품종 기반 소재의 화장품 또는 건강기능성 소재로의 활용 가능성을 고찰하고자 한다.
재료 및 방법
식물 시료 및 추출물 제조
본 연구에 사용된 미선나무(Abeliophyllum distichum Nakai) 품종 ‘옥황(Okhwang)’의 꽃은 2024년 3월 충청북도 괴산군 소재의 품종관리권자가 재배하는 분재 농원에서 채취하였다. 채취한 생체 꽃 시료 100 g에 증류수(FEP-0), 30% 에탄올(FEP-30), 50% 에탄올(FEP-50), 100% 에탄올(FEP-100) 용매 각각 1 L를 첨가하여 실온에서 7일간 침지 추출하였다. 추출 기간 동안 매일 초음파 수조를 이용하여 2시간씩 2회 초음파 처리를 수행하였다. 추출액은 여과 후 진공 회전농축기(Vacuum rotary evaporator, N-1110S, EYELA, Japan)를 이용하여 에탄올을 제거 및 농축하였으며, 이후 동결건조하여 분말 형태의 시료를 획득하였다. 제조된 각 용매 추출물은 생리활성 분석을 위한 실험에 사용하였다.
항산화 활성
각 추출물의 항산화 활성은 1,1-diphenyl-2-picryl hydrazyl (DPPH, Sigma-Aldrich, United States)를 이용한 전자공여능(Bondet et al., 1997)과 2,2'-azinobis-(3-ethylbenzothiazoline-6-sulfonate) (ABTS, Sigma-Aldrich, USA) 라디칼 소거 활성(Van den Berg et al., 1999)를 통해 추출물의 항산화활성을 평가하였다. DPPH 라디칼 소거능 평가는 1,1-diphenyl-2-picrylhydrazyl 용액을 515 ㎚에서 흡광도 1.00이 되도록 조절하여 실시하였다. 준비된 DPPH 용액 760 μL에 각 추출물 시료를 최종 50, 100, 200 ㎍/mL 농도로 되도록 첨가한 후, 37℃에서 20분간 반응시켰다. 반응 종료 후 UV-Vis spectrophotometer (X-ma 3000, Human Co., Korea)를 이용하여 515 ㎚에서 흡광도를 측정하였다. 항산화 활력은 시료 미처리군 대비 흡광도 감소율을 산출하여 백분율(%)로 표시하였다. ABTS 라디칼 소거능 분석은 7 mM ABTS 시약과 2.45 mM potassium persulfate (Sigma-Aldrich, USA)를 혼합하여 실온에서 24시간 동안 반응시켜 ABTS⁺ 용액을 형성하였다. 생성된 ABTS⁺ 용액은 734 ㎚에서 흡광도 0.70이 되도록 증류수로 희석하여 사용하였다. 희석된 ABTS⁺ 용액 760 μL에 각 추출물을 동일하게 최종 50, 100, 200 ㎍/mL 농도로 혼합하여 37 ℃에서 20분간 반응시킨 후 734 ㎚에서 흡광도를 측정하였다. 항산화 활성은 시료 무처리 대조군과 비교하여 백분율(%)로 환산하였다.
총페놀 및 총플라보노이드 함량 분석
총페놀 함량(Total Phenolic Content, TPC): 총페놀 함량은 Folin-Ciocalteu reagent를 이용하여 정량하였다. 각 추출물(EFP-0, EFP-30, EFP-50, EFP-100) 100 μL를 취하여 0.5 mL의 Folin-Ciocalteu reagent와 혼합하였다. 혼합물을 5 min간 실온에서 반응시킨 뒤, 1.5 mL의 7.5% Na2CO3 용액을 첨가하고 암소에서 30 min간 반응시켰다. 반응 후, 765 ㎚에서 흡광도를 측정하였으며, 표준물질인 탄닌산(tannic acid)을 이용한 표준곡선을 작성하여 각 추출물의 총페놀 함량을 ㎎ TAE/g (Tannic Acid Equivalent per g extract) 단위로 계산하였다. 모든 측정은 3회 반복하여 평균값과 표준편차로 표시하였다.
총플라보노이드 함량(Total Flavonoid Content, TFC): 총플라보노이드 함량은 aluminum chloride (AlCl3) 색소법을 이용하여 정량하였다. 각 추출물 500 μL에 1.5 mL의 2% AlCl3 용액을 혼합하고, 실온에서 30분간 반응시킨 후 415 ㎚에서 흡광도를 측정하였다. 표준물질로 루틴(rutin)을 사용하여 표준곡선을 작성하고, 각 추출물의 총플라보노이드 함량을 ㎎ RE/g (Rutin Equivalent per g extract) 단위로 산출하였다. 측정은 모두 3회 반복하여 평균값과 표준편차를 기록하였다.
HPLC 분석
각 추출물의 유효성분 분석을 위하여 HPLC (Waters 2695 Alliance System, Waters, Milford, MA, USA)를 사용하였으며, 검출기는 PDA (Waters 2996 Photodiode Array Detector)를 이용하여 분석을 수행하였다.
분석용 컬럼은 Xbridge C18 (250 × 4.6 ㎜, 5 ㎛, Waters Co.)을 사용하였으며, 이동상 용매는 0.1% formic acid가 함유된 증류수(Solvent B)와 acetonitrile (Solvent A)을 이용하였다. 분석 시간은 총 40분으로 설정하였으며, 이동상의 농도 구배(Gradient program)는 0분(99% B), 0~10분(99~75% B), 10~20 (75% B 유지), 20~40분(75~40% B), 40~45분(40~99% B), 45~55분(99% B 유지)의 조건으로 가동하였다. 시료의 유량(Flow rate)은 분당 1 mL, 시료 주입량(Injection volume)은 10 μL로 설정하여 분석을 실시하였다.
세포 배양 및 세포 생존율 평가
RAW 264.7 마우스 유래 대식세포는 American Type Culture Collection (ATCC, Manassas, VA, USA)으로부터 확보하였다. 세포는 10% fetal bovine serum (FBS)과 1% penicillin/streptomycin이 첨가된 Dulbecco’s Modified Eagle’s Medium (DMEM)을 사용하여 37°C, 5% CO₂ 조건의 배양기에서 유지하였다.
실험을 위해 세포를 24시간 동안 안정화한 뒤, 시료를 농도별(50, 100, 200 μg/mL)로 처리하였다. 시료 처리 24시간 후 CellTiter 96® AQueous One solution (Promega, USA)을 배지의 총량의 20%씩 처리하여 2시간 배양하였다. 반응이 종료된 후 UV/Visible spectrophotometer를 이용해 570 ㎚ 파장에서 흡광도를 측정하였으며, 세포 생존율은 무처리 대조군을 기준으로 백분율(%)로 환산하여 산출하였다.
NO 생성 억제 분석
RAW 264.7 세포는 24시간 동안 배양하여 안정화시킨 뒤 시료를 농도별로 처리하였다. 1시간 후 lipopolysaccharide (LPS)를 첨가하여 추가로 24시간 배양하였다. 배양 후 얻은 세포 상등액을 회수하여 Nitric oxide (NO) 생성량 분석에 사용하였다. 상등액에 Griess reagent (1% sulfanilamide, 0.1% N-1-naphthylenediamine dihydrochloride, 5% phosphoric acid)를 반응시킨 뒤 540 ㎚에서 흡광도를 측정하였으며, 무처리군 대비 상대적인 NO 생성량을 산출하였다.
iNOS 및 COX-2 단백질 발현 분석
RAW 264.7 세포는 24시간 배양 후 시료를 농도별로 처리하고 LPS (Sigma-Aldrich, USA)를 추가하여 24시간 동안 배양하였다. 배양이 종료된 세포는 phosphate-buffered saline (PBS, Gibco, USA)으로 2회 세척한 뒤 protease inhibitor cocktail (Sigma-Aldrich, USA)이 포함된 RIPA buffer (Sigma-Aldrich, USA)를 사용하여 용해하였고, 얼음 위에서 30분 정치시켰다. 용해된 시료는 4℃, 12,000 rpm 조건에서 20분 원심분리하여 상층액을 회수하였다. 단백질 정량은 Bradford Protein Assay (Bio-Rad, USA)를 사용하여 수행하였다.
정량된 단백질은 2 × Laemmli sample buffer (Bio-Rad, USA)를 혼합하여 95℃에서 5분 가열 처리한 후 10% SDS-PAGE에서 분리하였다. 전기 영동된 단백질은 PVDF membrane (Millipore, USA)에 전이한 뒤 5% skim milk (Bio-Rad, USA)를 함유한 TBST 용액에서 1시간 동안 실온에서 blocking하였다. 이후 membrane은 1차 항체를 처리하여 4℃에서 overnight 반응시킨 뒤 TBST로 세척하고, horseradish peroxidase (HRP)-conjugated 2차 항체(Bio-Rad, USA)를 1시간 동안 실온에서 반응시켰다. 세척 후 enhanced chemiluminescence (ECL) Western blotting detection kit (Bio-Rad, USA)를 사용하여 신호를 발현시켰으며, 밴드는 ChemiDoc Imaging System (Bio-Rad, USA)을 이용하여 검출하였다.
통계학적 분석
모든 실험은 3회 이상 반복 수행되었으며, 데이터 분석은 통계 프로그램 GraphPad Prism (version 5.02, GraphPad Software, USA)을 이용하여 수행하였다. 실험군 간의 차이는 일원분산분석(one-way ANOVA)을 통해 검정하였으며, 대조군과의 유의적 차이를 확인하기 위해 Dunnett 사후 검정을 실시하였다. p < 0.05는 통계적으로 유의미한 결과로 간주하였다.
결과 및 고찰
미선나무 꽃 추출물의 항산화 활성
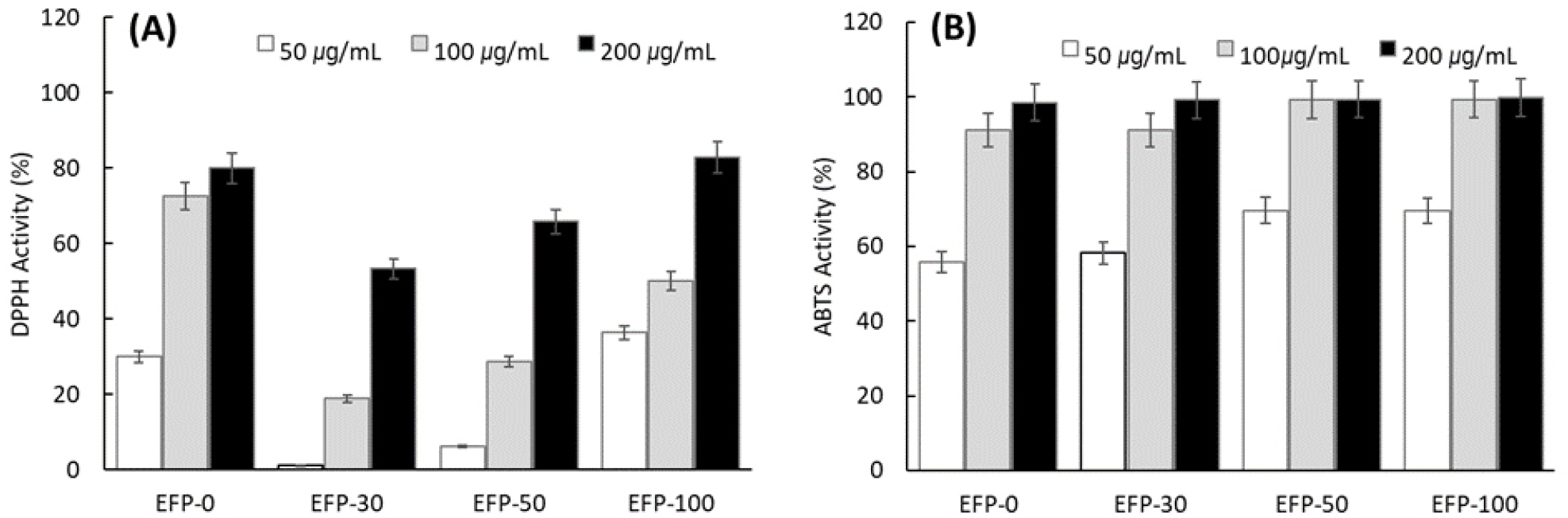
미선나무 꽃의 주정 농도별 추출물의 항산화 활성을 평가하기 위해 50, 100 및 200 ㎍/mL 농도에서 DPPH 및 ABTS radical 소거 활성을 분석하였다(Fig. 1). 미선나무 꽃 추출물은 낮은 농도(50~100 ㎍/mL)에서도 비교적 높은 radical 소거 활성을 나타내었으며, 특히 EFP-0 및 EFP-100에서 우수한 항산화 활성이 확인되었다. 반면 200 ㎍/mL에서는 모든 시료에서 95% 이상 활성에 도달하여 항산화 반응이 포화되는 경향을 보였으며, 이에 따라 시료 간 차별성이 감소하였다. 항산화 반응은 기질(radical)의 양이 제한적이기 때문에 일정 농도 이상에서 반응이 plateau에 도달하는 것으로 알려져 있으며, 이는 추출물 간 활성을 비교하기 위해서는 낮은 농도 구간에서 분석하는 것이 보다 타당함을 시사한다(Brand-Williams et al., 1995).
추출 용매에 따른 활성의 차이는 주정 농도의 비율이 0% 또는 100%인 조건에서 활성이 높게 나타났으며, 이는 페놀 계통 물질 중 일부는 극성 용매에서, 일부는 비극성 또는 약극성 용매에서 더 효율적으로 용출되는 특성과 관련이 있는 것으로 보인다. 식물성 소재의 항산화 활성은 용매 극성과 밀접한 상관성을 보이는 것으로 보고되어 있으며(Do et al., 2014), 본 연구에서도 유사한 경향이 확인되었다.
총페놀(TPC) 및 총플라보노이드(TFC) 함량
총페놀 및 총플라보노이드는 항산화 활성을 유도하고 지표 기능성 성분으로 활용되는 대표적인 천연물 소재 기반 바이오마커로 알려져 있다(Brand-Williams et al., 1995; Pietta, 2000). 각 농도별 추출액을 이용한 TOC 및 TFC를 측정한 결과(Table 1), 총 페놀성 화합물의 함량은 용매의 주정 비율이 증가함에 따라 증가하는 경향을 보였으며, 50% 주정 추출물(EFP-50)에서 가장 높은 함량(63.24 ㎎ TAE/g)을 나타내었다. 이는 페놀성 화합물이 극성도가 완전한 수용성 또는 완전한 주정보다 혼합 용매 조건에서 보다 효율적으로 용출되는 일반적인 추출 양상과 일치한다. 반면, 100% 주정 조건(EFP-100)에서는 소폭 감소하는 경향을 보였으며, 이는 물에 상대적으로 존재하는 수용성 페놀 물질이 100% 주정 조건에서 충분히 용출되지 않은 결과로 판단된다.
Table 1.
Total phenolic and total flavonoid contents of FEPA.
| Extracts |
TPCz (㎎ TAEy/g) |
TFCx (㎎ REw/g) |
| EFPv-0 | 51.65±0.78u | 6.08±1.12 |
| EFP-30 | 54.32±0.84 | 7.8±0.42 |
| EFP-50 | 63.24±1.08 | 12.12±0.53 |
| EFP-100 | 61.03±1.21 | 17.86±0.49 |
총 플라보노이드 함량 역시 주정 농도가 증가할수록 높아지는 경향을 나타냈으며, 특히 EFP-100에서 가장 높은 값(17.86 ㎎ RE/g)을 나타냈다. 플라보노이드는 페놀계 화합물의 하위 군에 속하지만 상대적으로 비극성에 가까운 분자구조를 가지는 경우가 많아 고농도 주정 조건에서 다량 용출되는 것으로 보고된 기존 천연물 연구내용과 일치한다(Do et al., 2014).
미선나무 꽃 추출물의 유효성분 함량
HPLC 분석에 각 추출물의 미선나무의 주요 유효성분 함량을 비교한 결과(Table 2, Fig. 2), EFP-0에서는 rutin (84.93 ㎎/g)과 caffeic acid (21.96 ㎎/g)가 가장 높은 수준으로 확인 되었으며, acteoside 또한 19.76 ㎎/g로 확인되었다. 반면 isoquercitrin은 검출되지 않았다(ND). EFP-30에서는 rutin (85.34 ㎎/g)이 물 추출과 유사하게 가장 높은 함량을 나타냈으며, isoquercitrin (11.80 ㎎/g)과 isoacteoside (14.21 ㎎/g)가 새롭게 검출되었다. EFP-50에서는 caffeic acid (6.16 ㎎/g) 및 rutin (31.27 ㎎/g)이 감소하는 경향을 보였으나 isoquercitrin (20.91 ㎎/g)이 최대치를 나타냈다. 반면 EFP-100에서는 모든 분석 성분이 감소하여 acteoside 4.86 ㎎/g, rutin 0.86 ㎎/g 등 전반적으로 낮은 수준을 보였다.
Table 2.
Analysis of functional component contents in FEP according to ethanol concentrations.
| Extracts | Caffeic acid | Rutin | Acteoside | Isoquercitrin | Isoacteoside |
| EFPz-0 | 21.96±0.35y | 84.93±1.01 | 19.76±0.54 | NDw | 11.73±0.35 |
| EFP-30 | 10.51±0.27 | 85.34±1.05 | 24.14±0.51 | 11.8±0.05 | 14.21±0.18 |
| EFP-50 | 6.16±0.14 | 31.27±0.83 | 12.01±0.09 | 20.91±0.07 | 8.11±0.21 |
| EFP-100 | 2.55±0.08 | 0.86±0.03 | 4.86±0.05 | 6.8±0.04 | 6.05±0.08 |
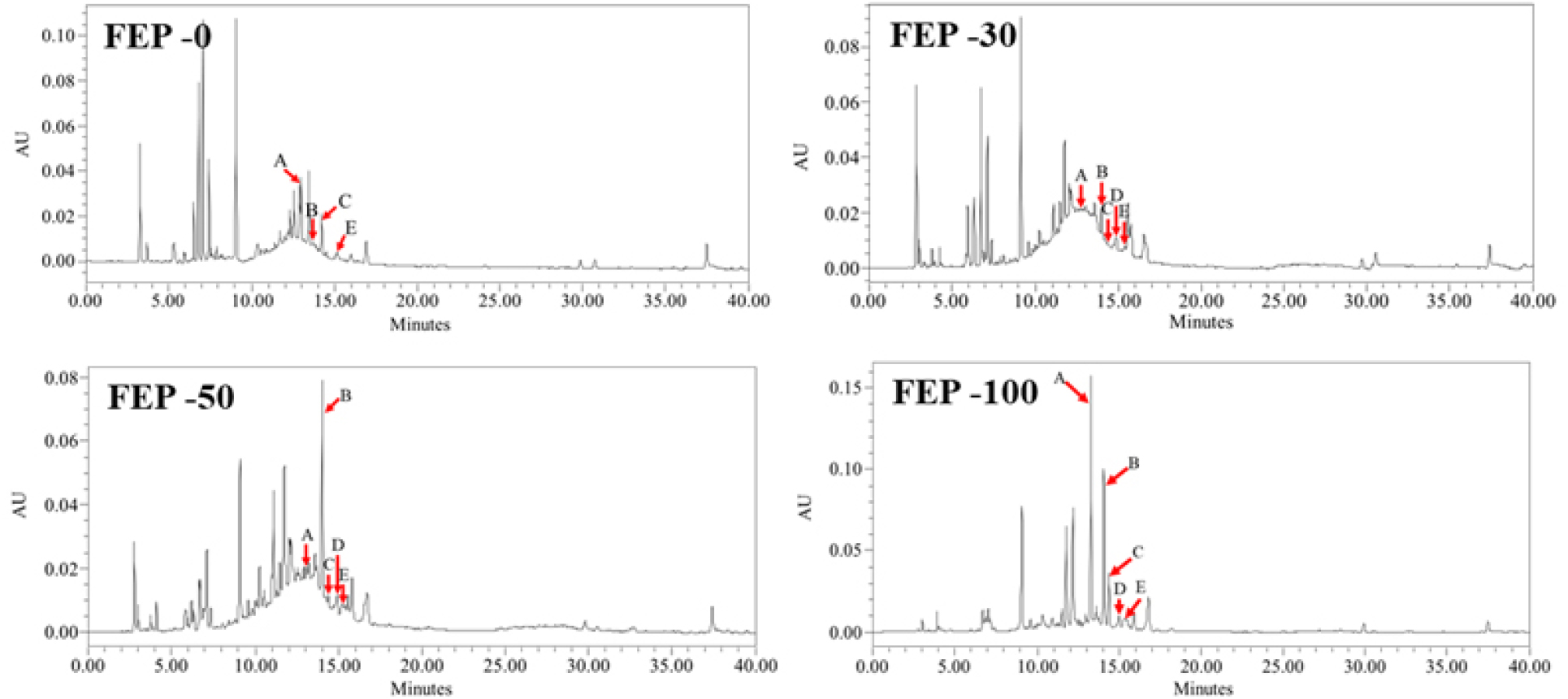
Fig. 2.
HPLC chromatograms of Abeliophyllum distichum flower extracts (FEP) obtained with different ethanol concentrations (0, 30, 50, and 100%). The peaks indicated by arrows represent major functional compounds identified in the extracts. A; Caffeicacid, B; Rutin, C; Acteoside, D; Isoquercitrin, and E; Isoacteoside.
EFP-30에서 다양한 phenylpropanoid 및 flavonoid 계열 성분(rutin, isoquercitrin, acteoside 등)이 동시에 검출된 점은 해당 용매 조성이 극성 및 반극성 물질 모두를 용출할 수 있는 분획 조건인 것으로 판단된다. 즉, rutin·caffeic acid와 같은 극성 페놀은 수용성에 기반하여 물 또는 저농도 에탄올에서 용출되며, 반면 isoquercitrin·isoacteoside는 구조 내 당 결합을 포함하더라도 상대적으로 높은 용해도를 가지는 반극성 계열로 보고되어 중간 농도 용매에서 용출이 증가하는 경향과 부합하는 것으로 판단된다. 이러한 결과는 식물 유래 polyphenol 계열의 용매 극성 의존적 분획 특성과 동일한 패턴을 보이며 기존 연구 보고와도 일치한다(Bravo 1998; Do et al., 2014).
동일 시료군에서 측정된 TPC 및 TFC 함량과 비교할 때, EFP-50 및 EFP-100에서 TFC가 상대적으로 증가한 점은 isoquercitrin, isoacteoside 등의 플라보노이드 함량 증가와 일치하는 경향을 보였다. 또한 항산화활성(DPPH 및 ABTS)에서도 저농도 조건에서 EFP-50 및 EFP-30 분획이 우수한 활성을 보였으며, 이는 HPLC 기반 유효성분 및 TPC·TFC 결과와 상관성을 지지하는 것으로 판단된다. Polyphenol 계열 성분이 라디칼 소거 기반 항산화 능력을 나타내고 지표 기능성 성분으로 활용되는 대표적인 바이오마커라는 점이 기존연구들과 동일한 결과를 나타낸다(Heim et al., 2002; Kang et al., 2024; Rice-Evans et al., 1996).
따라서 미선나무 꽃 추출물은 용매 조성에 따라 유효성분 유형 및 비율이 상이하게 분획되며, 이는 활용 목적에 따라 기능성 기반 맞춤형 추출 전략 설계가 가능함을 의미한다. 특히 30~50% 에탄올 조건은 항산화 기반 건강기능성 소재 개발에 적합한 추출조건으로 판단된다.
세포 생존율 평가
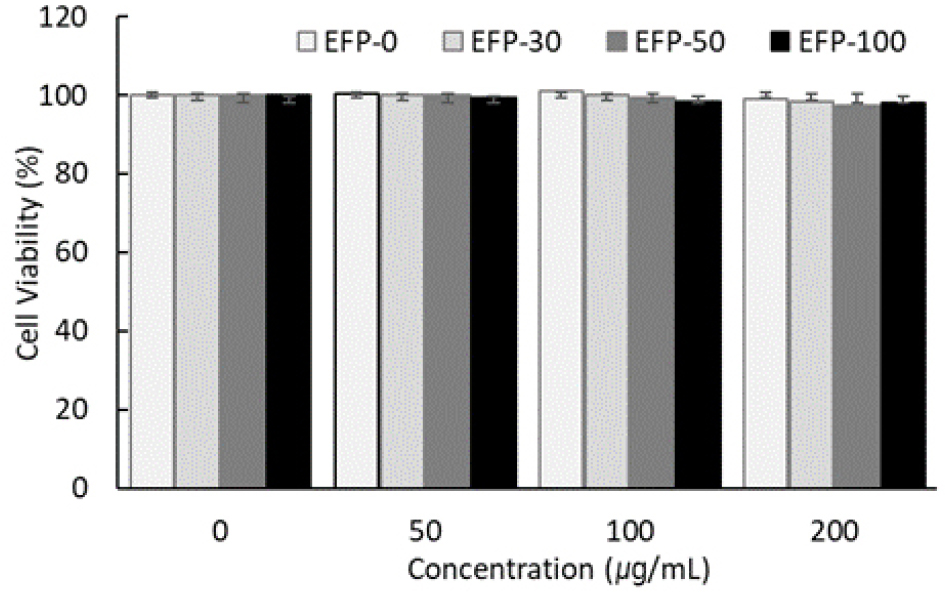
RAW 264.7 세포에 미선나무 꽃 추출물(EFP-0, EFP-30, EFP-50, EFP-100)을 각각 0, 50, 100, 200 ㎍/mL 농도로 24시간 처리한 뒤 MTS assay를 이용하여 세포 생존율을 평가하였다(Fig. 3). 모든 추출물 처리군에서 200 ㎍/mL의 최고 농도에서도 세포 생존율이 약 95~102% 범위 내에서 유지되었으며, 대조군과 비교하여 유의적인 감소는 관찰되지 않았다. 이는 미선나무 꽃 추출물이 해당 농도 범위 내에서 RAW 264.7 macrophage 세포에 급성 독성을 유발하지 않음을 의미하며, 세포 손상으로 인한 secondary effect 없이 LPS 유도 염증 반응 실험을 수행할 수 있다는 점을 확인하였다.
NO 생성 억제 효과
추출 용매별 미선나무 꽃 추출물의 항염증 활성 가능성을 평가하기 위해 LPS 자극에 의해 RAW 264.7 대식세포에서 유도되는 NO 생성량을 추출물 농도별로 비교하였다. NO 생성 억제 시험은 대식세포 기반 염증 모델에서 항염증 후보물질의 가능성을 스크리닝하는 대표적인 기법으로 널리 활용되고 있다(Bondet et al., 1997; Ryu et al., 2019).
각 추출물 100 ㎍/mL 농도로 처리한 다음 NO 생성량을 확인한 결과(Fig. 4), EEFP-0 및 EFP-30 처리군은 대조군과 비교하여 NO 생성량의 변화가 낮았으며, LPS에 의해 유도된 염증 반응을 효과적으로 억제하지 못하는 것으로 나타났다. 즉, 두 추출물은 NO 생성 억제율이 매우 낮은 수준에서 유지되었으며, 이는 항염증 기능성 성분이 극성이 높은 수용성 분획에 상대적으로 적게 존재함을 시사한다. 반면 EFP-50 및 EFP-100은 대조군 대비 NO 생성량이 유의적으로 감소하였으며, EFP-50에서 가장 큰 억제 효과가 확인되었다.
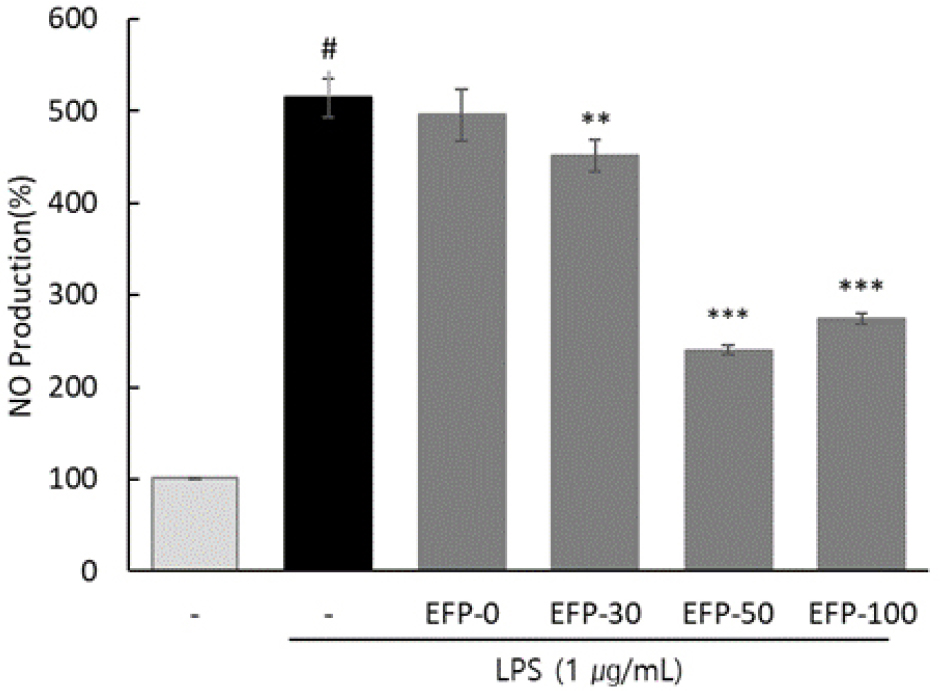
Fig. 4.
Suppression of LPS-induced Nitric Oxide (NO) production by FEP in RAW 264.7 cells. The levels of NO in the culture medium were determined. LPS-induced NO production was significantly reduced by FEP treatment in a concentration-dependent manner, particularly at 50 and 100 μg/mL. Each bar represents the mean ± SD (n=3).
이러한 결과는 phenolic 및 flavonoid 계열 성분이 중극성 용매에서 높은 회수율을 보인다는 기존 식물추출 연구들과 일치하며(Bravo, 1998; Do et al., 2014), 본 연구에서 측정된 총페놀(TPC), 총플라보노이드(TFC) 및 HPLC 기반 활성 성분 분석 결과와도 높은 연관성을 나타냈다.
iNOS 및 COX-2 단백질 발현 억제 효과
추출 용매별 미선나무 꽃 추출물의 항염증 활성 가능성 평가를 위해 LPS를 처리에 의한 RAW 264.7 세포에서 iNOS 및 COX-2 단백질 발현을 분석하였다. iNOS와 COX-2는 염증성 매개인자의 생성과 밀접하게 연관된 효소로서 nitric oxide (NO) 및 prostaglandin E2 (PGE2)의 합성을 유도하는 대표적인 염증 biomarker로 알려져 있다(Tsatsanis et al., 2006).
Western blot에 의한 단백질 발현을 분석한 결과, LPS 처리군에서 iNOS 및 COX-2 단백질 발현은 정상 대조군에 비해 유의적으로 증가하였다. 반면, EFP 처리군에서는 농도 의존적으로 감소하는 경향을 보였다(Fig. 5). 특히 EFP-50 및 EFP-100 처리군에서 발현 억제가 뚜렷하며, LPS 대조군 대비 각각 약 45% 감소(EFP-50) 및 75% 감소(EFP-100) 수준으로 나타났다. 반면, EFP-0 및 EFP-30 처리군은 LPS 단독군 대비 발현 수준이 다소 감소하였으나 억제 효과가 제한적이었으며, iNOS 및 COX-2 발현의 명확한 저해 효과를 확인하기에는 충분하지 않았다.
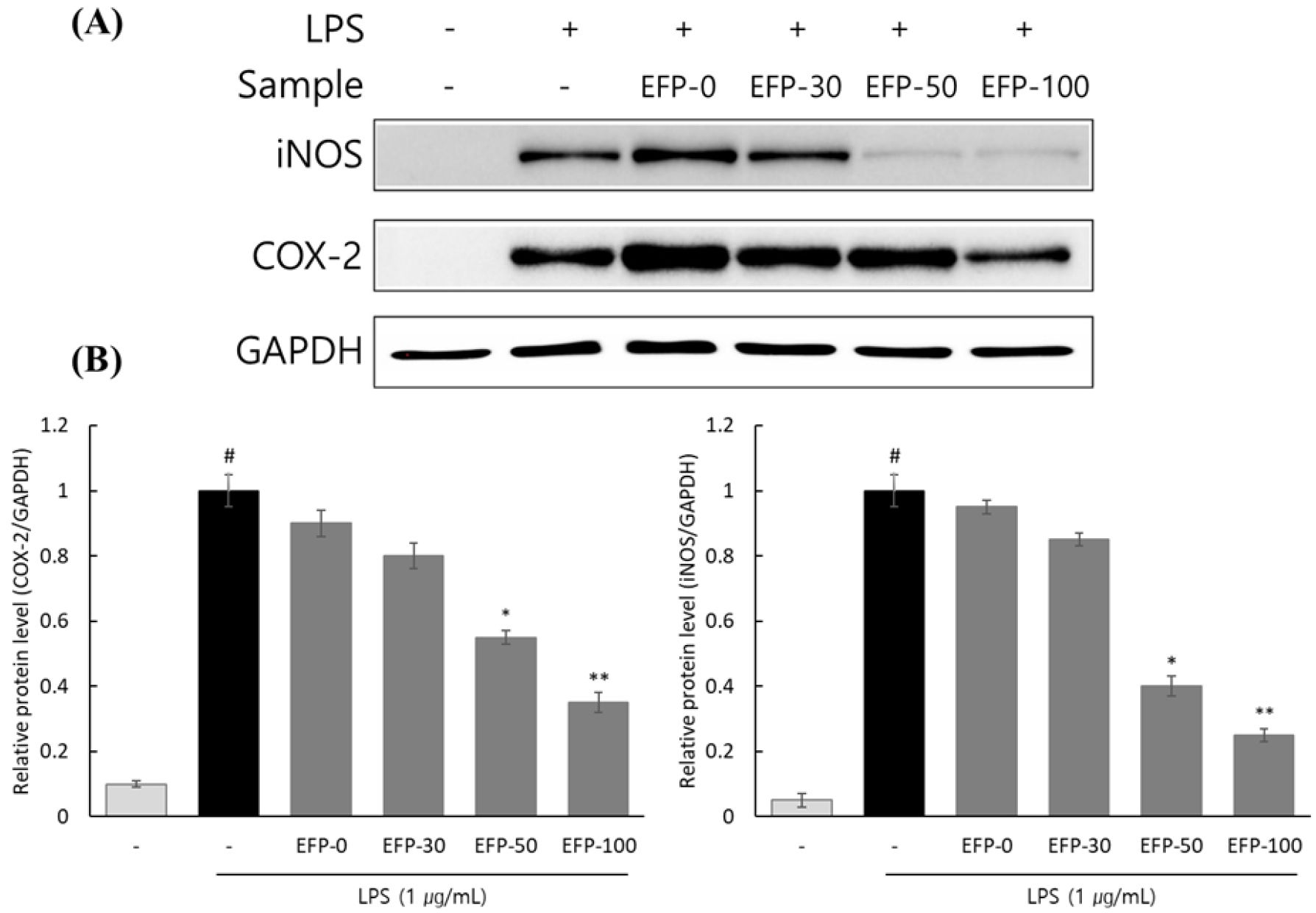
Fig. 5.
Effects of EFP on the protein expression of iNOS and COX-2 in LPS-stimulated RAW 264.7 cells. (A) iNOS and COX-2 protein levels were determined by Western blot. GAPDH was used as an internal loading control. (B) Relative band intensities were quantified using ImageJ software and normalized to GAPDH. Data are presented as mean ±SD (n=3). #p < 0.05 versus the untreated control group; *p < 0.05 and **p < 0.01 versus the LPS-treated group.
iNOS 및 COX-2 발현 억제는 polyphenol 기반 식물 유래 항염증 소재에서 흔히 관찰되는 기전으로 알려져 있으며, 그 작용은 NF-κB와 MAPK 신호전달 축 조절을 통해 이루어지는 것으로 보고되어 있다(Kim et al., 2004; Surh et al., 2001). 상기 NO 생성량 분석 결과에서도 주정의 농도의존적으로 NO 생성이 억제되는 경향을 보였다는 점에서 발현 조절이 기능적 결과로 이어짐을 지지한다. 즉 단백질 발현 데이터와 기능적 매개물 데이터가 일관되게 나타난다는 점에서 항염증 활성 가능성이 높음을 의미한다.
추출 용매 특성 관점에서는 미선나무 꽃에서 폴리페놀 및 플라보노이드 계열의 용매 극성 의존적 추출 특성이 보고된 바 있으며, 이는 항염증 및 항산화 활성과 높은 상관성을 갖는 것으로 알려져 있다(Bravo, 1998; Cai et al., 2004). 이러한 현상은 phenolic 계열 물질의 구조적 친수성 및 방향족 환 구조로 인한 용매 친화성에 기인하는 것으로 해석된다. 결과적으로 본 연구에서의 농도 의존적 발현 억제는 미선나무 꽃 내 phenolic/flavonoid 기반 활성물질의 생리활성 작용 패턴을 반영하는 것으로 판단된다.
적 요
본 연구에서는 미선나무(Abeliophyllum distichum) 옥황1호 꽃의 주정 농도별 추출물(EFP-0, EFP-30, EFP-50, EFP-100)의 항산화 및 항염증 활성을 평가하였다. 각 추출물은 50, 100, 200 ㎍/mL 농도에서 DPPH 및 ABTS radical 소거 활성을 측정한 결과, 50~100 ㎍/mL에서도 높은 항산화 활성을 나타냈으며, 200 ㎍/mL에서는 모든 시료가 95% 이상의 항산화 효과를 보여 반응이 포화되는 경향을 확인하였다. 특히, EFP-30과 EFP-50은 극성 및 반극성 성분을 동시에 용출하여 낮은 농도에서도 우수한 radical 소거 활성을 보였다. 이러한 결과는 추출물 내 폴리페놀 계열 성분의 용매 극성 의존적 용출 특성과 일치하며, DPPH 및 ABTS 활성과 밀접한 상관성을 나타냈다.
총페놀(TPC) 및 총플라보노이드(TFC) 함량 분석 결과, TPC는 EFP-50에서 가장 높은 함량(63.24 ㎎ TAE/g)을 나타냈고, EFP-100에서는 다소 감소하였으며, TFC는 주정 농도가 증가할수록 증가하여 EFP-100에서 17.86 ㎎ RE/g로 최대치를 보였다. HPLC 분석에서는 EFP-0에서 rutin, caffeic acid, acteoside가 가장 높게 검출되었고, EFP-30과 EFP-50에서는 isoquercitrin과 isoacteoside가 함께 검출되어 다양한 극성 계열 성분이 혼합 용매에서 효율적으로 용출됨을 확인하였다. 이러한 TPC/TFC 및 HPLC 기반 유효성분 분석 결과는 항산화 활성과 일관되게 나타나 미선나무 꽃 추출물의 폴리페놀 및 플라보노이드 성분이 항산화 활성을 유도하는 주요 성분임을 시사한다.
세포 생존율 평가에서 RAW 264.7 세포는 0~200 ㎍/mL 농도 범위에서 95~102% 수준으로 유지되어 미선나무 꽃 추출물이 급성 독성을 유발하지 않음을 확인하였다. 또한 LPS 유도 염증 모델에서 NO 생성 억제 실험을 수행한 결과, EFP-50과 EFP-100은 대조군 대비 NO 생성량을 각각 40~45% 및 70~75% 감소시켰으며, EFP-0과 EFP-30은 억제 효과가 제한적이었다. 그리고 iNOS 및 COX-2 단백질 발현 분석에서는 EFP-50과 EFP-100 처리군에서 발현이 감소하여, NO 생성량 감소 결과와 일치하는 항염증 효과를 확인하였다. 이러한 결과는 미선나무 꽃 추출물의 폴리페놀 및 플라보노이드 성분이 NF-κB 및 MAPK 신호전달 조절을 통해 항염증 활성을 나타냄을 뒷받침한다.
이상의 결과를 통해 본 연구에서는 미선나무 꽃 추출물이 용매 조성에 따라 유효성분 구성과 항산화 및 항염증 활성에서 차이를 보임을 확인하였으며, 특히 30~50% 주정 혼합 용매는 다양한 극성 계열 성분을 동시에 용출하여 항산화와 항염증 활성이 가장 균형 있게 나타나는 최적 추출 조건임을 제시하였다. 이러한 결과는 미선나무 꽃 추출물이 건강기능성 소재 개발에 활용될 수 있는 중요한 기초 자료를 제공하며, 향후 기능성 식품 및 건강기능식품 개발에서 맞춤형 추출 전략 설계에 기여할 것으로 기대된다.